星标“医工学人”,第一时间获取医工交叉领域新闻动态~

植入式电子设备正在从“大型手术专属”走向“微创甚至无创”。2026年4月15日,由美国芝加哥大学Pengju Li & Bozhi Tian等团队共同完成这篇发表于《Nature Materials》的综述,题为“Minimally invasive bioelectronic implants”(微创生物电子植入物),系统梳理了从神经探针到心脏起搏器的技术跃迁:利用形状记忆合金、可编程聚合物和动态致动器,研究者正将设备做到足够小、足够软、足够智能,使其通过血管或自然腔道精准抵达目标区域。这不是未来的想象,而是已在猪、犬等大动物模型中验证的现实。

当“救命”与“创伤”成为同一枚硬币的两面
植入式电子设备——无论是用于深部脑刺激的神经探针,还是维持心律的心脏起搏器——在过去几十年里拯救了无数生命。但它们有一个长期无法回避的代价:高度侵入性的外科手术。
开胸手术(thoracotomy)和开颅手术(craniotomy)是这类设备的常规入场券。患者不仅要承受巨大的生理创伤,还需要面对数月的恢复期、显著的感染风险,以及植入物与机体组织之间的机械不匹配问题——硬质电子器件与柔软生物组织之间的摩擦,往往导致慢性炎症、纤维包囊,甚至设备失效。
更棘手的是,不同组织的再生能力差异巨大:皮肤表皮每两周更新一次,而骨骼的修复周期长达3至6个月。这意味着,对骨组织进行任何不必要的损伤,其后果远比皮肤切口严重得多。此外,血管和神经网络在体内的交错分布,使得任何一根“走错路”的导管都可能造成不可逆的功能损伤。
对于儿科和胎儿患者而言,问题更加严峻。成长中的身体意味着植入物不仅要“适应当下”,还要“适应未来”——一个刚出生的婴儿植入的起搏器,几年后可能就变成了机械意义上的“紧身衣”。
正是这些临床痛点,驱动了微创生物电子植入物的诞生。目标是清晰的:让设备像一根细软的导管一样进入体内,然后在目标位置“变”成一个功能完备的电子系统。
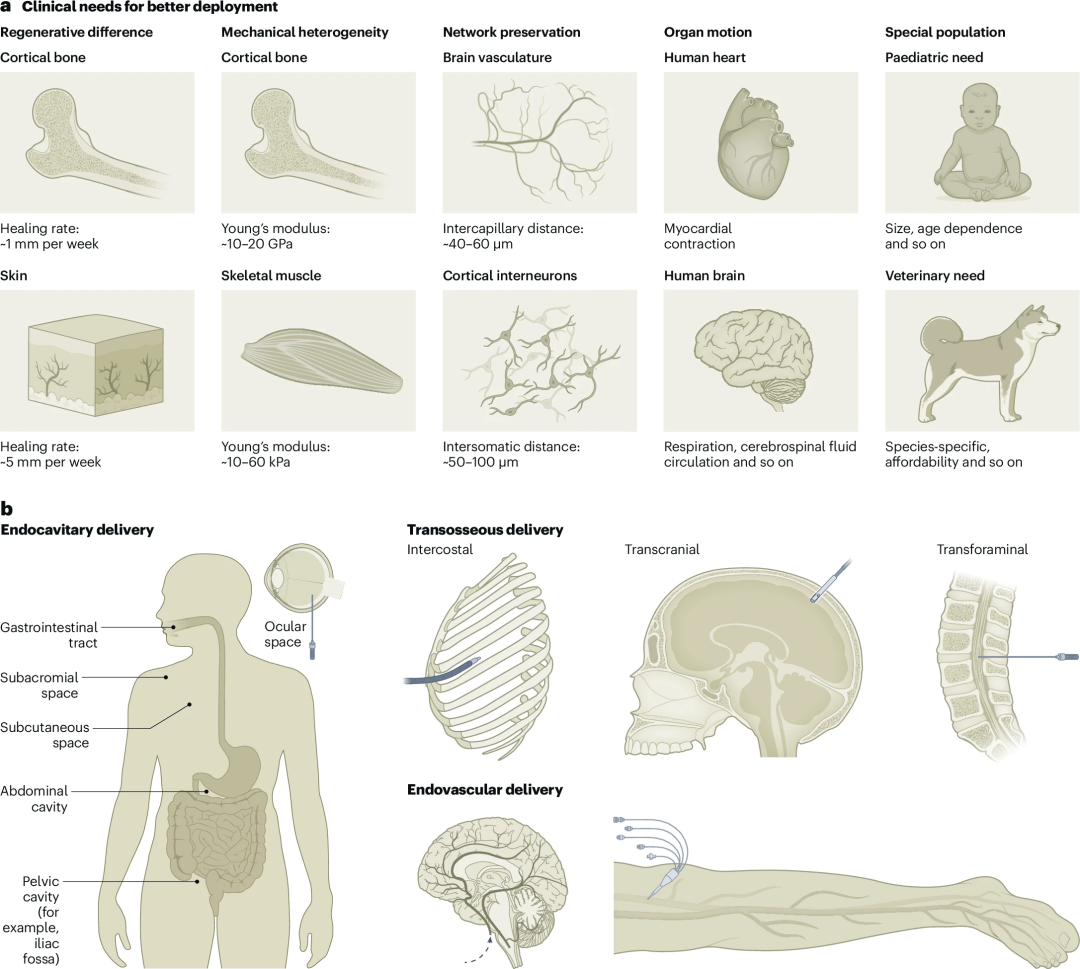
图 1 | 微创生物电子设备部署系统的临床需求。
从支架手术中汲取灵感:紧凑输送 + 原位重构
微创生物电子植入物的核心技术逻辑,其实源于一个我们并不陌生的临床工具——血管支架。支架在输送时是直径1-2毫米的紧凑圆柱体,通过导管送达狭窄血管后,通过球囊扩张或形状记忆合金的自膨胀,变成2.5-5毫米的功能形态。
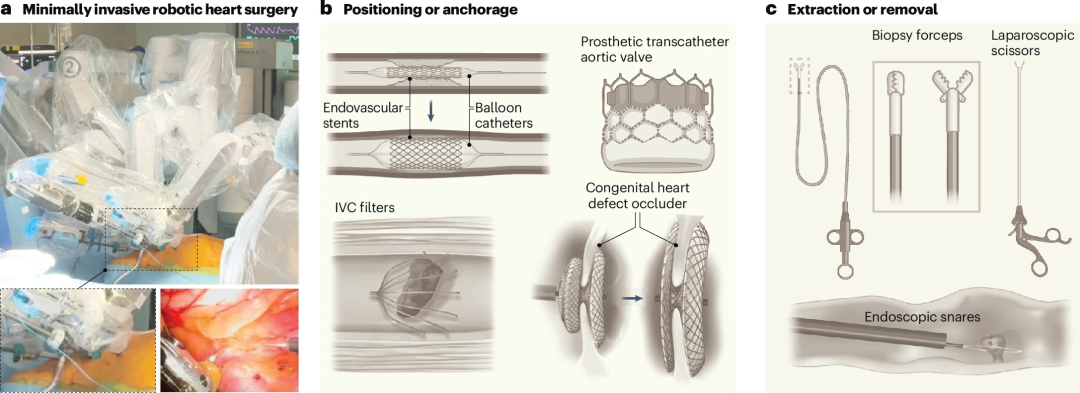
图 2 | 可扩展手术工具的示例。
生物电子植入物沿用了这一思路,但远不止于此。它们不仅要在尺寸上“变小”,还要在功能上“变强”——同时实现电生理记录、光遗传刺激、药物递送和实时信号处理。
新材料:让“变”成为可能
实现这一切的关键,是一系列先进材料的协同工作:
|
材料类别 |
代表材料 |
功能作用 |
|
形状记忆合金 |
镍钛合金(Nitinol) |
体温触发形变,实现自膨胀锚定 |
|
可编程聚合物 |
聚乳酸-羟基乙酸共聚物(PLGA)、聚己内酯(PCL) |
可控降解,临时支撑,无需二次取出 |
|
动态致动器 |
水凝胶、电化学活性聚合物 |
pH/温度响应性膨胀或收缩,实现按需形变 |
|
超柔性导体 |
PEDOT:PSS、碳纳米管、MXene |
低阻抗、高电荷注入能力,匹配软组织力学模量 |
|
平均误差 |
较高 |
3.78° |
|
使用前校准 |
需 |
无需(即戴即用) |
一个关键公式:为什么“薄”就是“好”?
文献中给出了一个衡量机械匹配程度的简化公式:
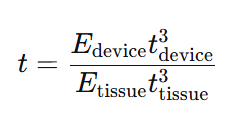
其中 E 为弹性模量,t 为厚度。这个比值越小,器件与组织之间的机械应变越小,长期生物相容性越好。
换句话说,做薄,是实现“无感植入”的数学基础。
这也是为什么像 MEV(微米尺度血管内)神经探针这样的设备,其弯曲刚度可以低至 10⁻¹⁰ N·m⁻¹,比自由状态的血管(10⁻⁶ N·m⁻¹)还要低四个数量级。
三类核心设备对比
|
设备类型 |
部署方式 |
关键创新 |
应用场景 |
|
超柔性血管内神经探针 |
微导管输送,血管内导航 |
网状结构,可进入<100μm的微血管 |
皮层神经记录,无需开颅 |
|
光电子心脏起搏器 |
肋间小切口(<1cm),内镜辅助 |
4μm厚硅膜,光控无基因起搏 |
急性心脏临时起搏 |
|
生物粘附性起搏导线 |
鞘管+球囊导管递送 |
NHS-胺共价键粘附,可pH触发取出 |
临时心外膜起搏,无缝合 |
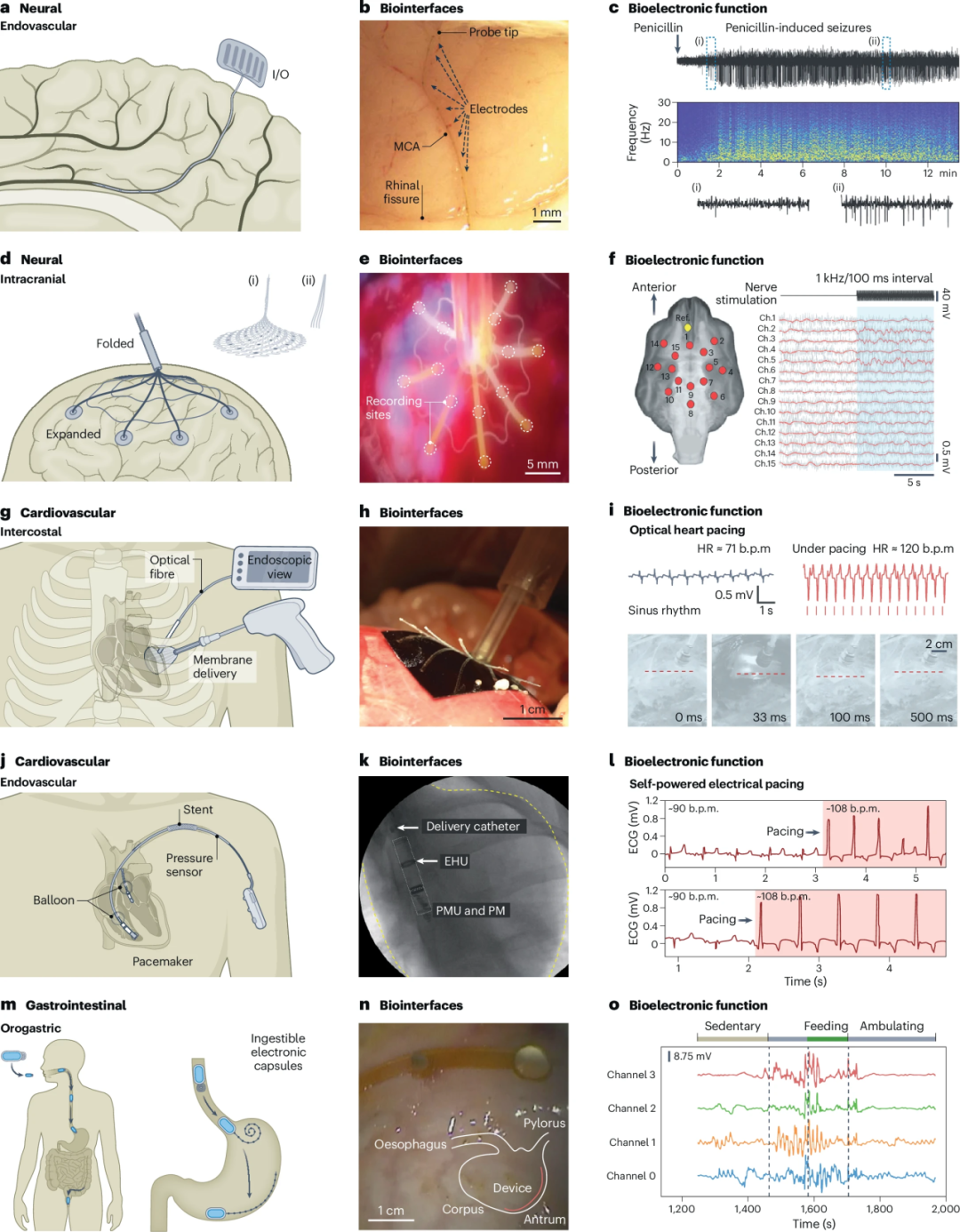
图 3| 当前微创生物电子接口。
神经界面:血管里的“电子蜘蛛网”
最令人印象深刻的实验之一,来自芝加哥大学团队开发的超柔性血管内探针(MEV)。该设备通过微导管进入大鼠大脑的中 Cerebral Artery(直径<100μm),在导管撤回后,网状结构自然展开并贴附在血管内壁上。
关键数据:
-
成功记录局部场电位(local field potentials)和单单元峰电位(single-unit spikes)
-
在青霉素诱导的癫痫模型中,清晰捕捉到发作期频谱演化
-
植入后炎症反应显著低于传统硬质探针
心脏界面:4μm厚的“光控贴片”
在猪模型中,研究团队通过肋间小切口(<1cm)将一张厚度仅4μm的硅膜输送到心脏表面,通过内镜耦合的光纤进行光刺激。
关键数据:
-
心率从71 bpm被精确调制至120 bpm
-
实现了多点位心外膜起搏,无需基因改造
-
无明显的组织损伤或热效应
胃肠道界面:吞下一台“胃电图仪”
MIGUT胶囊是一个更接近消费级想象的产品。患者吞下胶囊(约9.5×12.5×40mm)后,胃液溶解水溶性粘合剂,释放一根25cm长的聚酰亚胺电极带,自动展开并贴附于胃黏膜。
关键数据:
-
能够稳定记录胃慢波活动(gastric slow-wave activity)
-
在大型动物模型中持续工作数天
-
为胃动力障碍疾病的诊断提供了全新的非侵入式工具
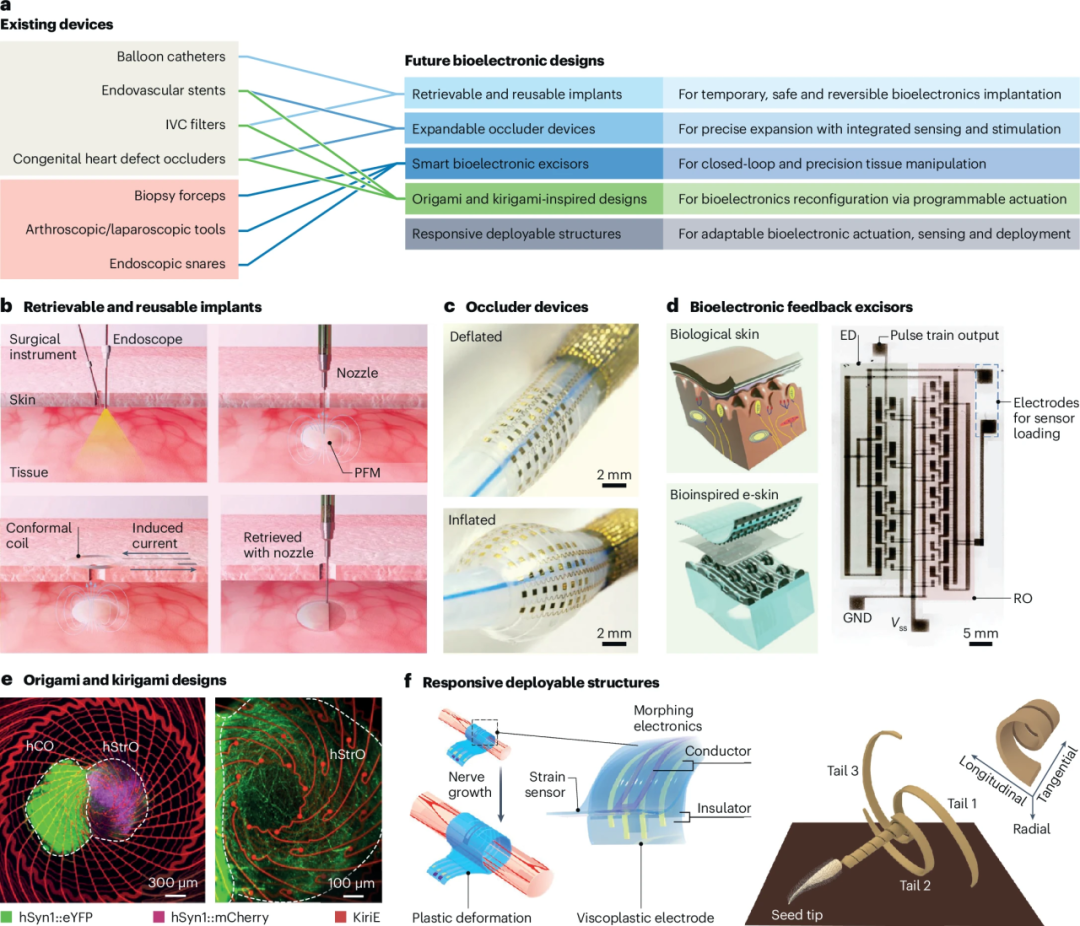
图 4 | 整合适应性仿生架构与先进电子功能的变革性设计。
对行业意味着什么?
这项综述所描绘的,并不仅仅是几个实验室的“炫技”。它指向了一个更本质的范式转移:植入式医疗正在从“开放手术时代”走向“介入式电子时代”。
对于医疗器械公司而言,这意味着:
-
新的产品管线:可回收神经探针、自供电心脏起搏器、智能封堵器
-
新的商业模式:临时植入、按需降解、无需二次取出,降低了长期并发症风险和医疗成本
-
新的技术壁垒:材料科学、微纳加工、无线供能的多学科融合能力将成为核心竞争力
未来五年值得关注的方向
文献中提出了几个极具前瞻性的设计方向:
-
可回收与可重复使用植入物
受下腔静脉滤器启发,未来的植入物可以在完成任务后通过磁场或化学触发方式无损取出,甚至消毒后重复使用。
-
膨胀式封堵器
利用形状记忆合金和4D打印弹性体,实现对血管、心脏缺损的动态封堵,同时集成电生理传感功能。
-
折纸与剪纸(Origami/Kirigami)电子学
将二维薄膜通过折叠结构实现三维形态转变,从狭小的骨孔进入后展开成大面积的皮层电极阵列。
-
响应式可部署结构
受Erodium种子自钻入土机制启发,湿度驱动的形变结构可以在体内自主完成锚定和部署,无需外部动力。
技术很美,但路还很长
尽管这篇综述展示了令人振奋的进展,但我们必须保持冷静。从实验室到大面积临床应用,仍有几个关键鸿沟需要跨越。
-
长期稳定性与疲劳失效
可形变器件在反复的机械运动(如心跳、呼吸、胃肠蠕动)中,折叠点、铰链区域容易出现材料疲劳、分层甚至微裂纹。目前大多数研究仅验证了数周到数月的稳定性,而慢性植入需要的是数年甚至数十年的可靠性。
-
无线供能的几何困境
形变器件最大的尴尬在于:它变形的过程,也是其能量接收界面不断变化的过程。一个在植入后展开、扭转、膨胀的设备,其与外部供能线圈的电磁耦合效率会随之大幅波动。目前尚无成熟的解决方案。
-
生物污损与免疫应答
更复杂的几何结构意味着更大的表面积和更多的“死角”,这些地方容易成为蛋白质吸附、细胞粘附和纤维包囊的起点。如何在这些可变形表面上实现长效抗污,仍是一个开放问题。
-
从动物到人的缩放挑战
猪和犬的解剖结构与人类存在显著差异。一个在大鼠脑血管中顺利展开的网状探针,在人类更曲折、更坚硬的血管网络中可能根本无法到达目标位置。需要大量的计算模拟和定制化设计。
-
成本与可及性
目前这些设备大多在超净间中手工组装,成本极高。如果无法实现自动化、规模化的制造工艺,微创生物电子植入物将长期停留在“富人的医疗”层面。
最后一个值得深思的问题:当我们可以通过一根细小的导管将智能电子设备送入大脑、心脏和胃肠道,并让它们在完成任务后悄然降解或无损取出——这是否意味着,未来的医疗将不再区分“植入物”和“非植入物”?或许,真正的未来不是更小的手术切口,而是不再需要“手术”这个概念本身。
[1]Li, P., Hibino, N., Shi, L.L. et al. Minimally invasive bioelectronic implants. Nat. Mater. (2026).
https://doi.org/10.1038/s41563-026-02576-9
END
编辑 | 郝娅婷
排版 | 张艳青
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
npj flexible electronics | 隐形眼镜不只能“看”,还能“感”:早稻田大学团队将眼压监测灵敏度推至47.31 Ω/mmHg
点击关注医工学人 直播预告

本篇文章来源于微信公众号: 医工学人