星标“医工学人”,第一时间获取医工交叉领域新闻动态~
光遗传技术是神经科学的革命性工具,但其核心痛点从未被真正解决:如何在不植入光纤的前提下,深穿透、高精度、动态化地靶向任意脑区?斯坦福大学、弗吉尼亚大学、南加州大学的研究团队联合提出了一种基于聚焦超声扫描与血管内循环力致发光纳米转导器的活体光源,在自由活动小鼠中实现了亚毫米级空间分辨率的动态三维光操控,并成功诱导了精确的旋转行为。这项技术或将为全身光学干预打开一扇全新的大门。
光与脑的“最后一公里”
过去二十年,光遗传学彻底改变了神经科学对特定神经环路功能的认识。然而,一个看似简单的问题始终悬而未决:如何将光精准、无创、动态地送到深层组织的任意位置?
植入式光纤是目前最成熟的技术路线。它确实能实现细胞级精度——但代价是“一植入便锁定一地”。如果要同时刺激多个远距离脑区,就需要多根光纤或多点植入,这不仅增加了感染风险和免疫反应,也从根本上限制了研究者在三维空间内动态切换靶点的能力。
另一方面,非侵入式方法如近红外光、上转换纳米粒子、磁热或超声直接刺激,虽然在一定程度上摆脱了植入物的束缚,却各自面临难以逾越的瓶颈:近红外光穿透深度有限(数毫米级),且难以实现亚毫米级精准三维聚焦;磁热或超声直接刺激虽能穿透深层,但其作用机制往往依赖于非特异性的热效应或机械敏感通道激活,细胞类型特异性不足,且存在潜在的安全隐患。
该论文在引言中明确指出:“现有生物界面无法同时提供高时空精度以及动态靶向任何区域而不干扰周围组织的能力。”
换言之,学界真正需要的是一种可编程、可扫描、全身体积覆盖的光源——它既能像光纤一样精准,又能像超声一样深层穿透,还能像血管一样通达全身。
血管里的“纳米灯泡” + 超声扫描“笔”
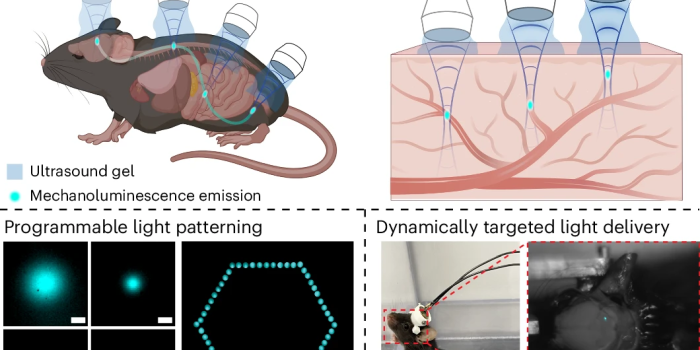
本研究的核心创新,可以用一个类比快速理解:将力致发光纳米颗粒(MLNTs)注入血管,再用聚焦超声(FUS)作为一支“无形的笔”,在体内任意有血管分布的位点“写”出光来。
图1:通过超声介导光源对生物系统的光学扫描
· 技术原理拆解
1. 核心材料:研究者合成了Sr₄Al₁₄O₂₅:Eu,Dy 力致发光纳米转导器。通过球磨法将原始微米级颗粒(>10 μm)降至30–110 nm的胶体尺寸,并在表面修饰聚乙二醇(PEGylation)以获得长期稳定的水分散性(≥1周)。
2. 能量转换:当聚焦超声束照射到血管内的MLNTs时,机械应力诱导晶格缺陷中的陷阱电子跃迁,发射出490 nm的可见光(峰值波长,与ChR2等光敏感蛋白的激活峰匹配)。
3. 空间聚焦:超声换能器的频率越高,声学焦斑越小。实验测得的侧向分辨率(FWHM)随频率从0.65 MHz升至5.7 MHz,由2.1 mm锐减至0.18 mm。更重要的是,力致发光效应本身存在压力阈值(≈1 MPa),使得实际光斑尺寸进一步小于声学焦斑——这是一种自聚焦增益。
4. 动态扫描:由于MLNTs随血流分布全身,研究者只需机械地移动超声焦点,就能在大脑皮层(M1,S1)、海马体(vDG,dDG)、肠道、后肢肌肉、脊髓(T12段) 等不同解剖位置依次产生光发射,实现真正意义上的“动态光模式生成”。
· 新旧技术对比
论文明确指出:“通过将可重定位的FUS与广布全身的响应性纳米转导器相结合,该平台支持可编程光模式生成和动态靶向光递送。”
从体模到自由活动小鼠:三层证据锁定有效性
1. 人工循环系统与活体成像:光真的“亮了”
研究者在人工循环管路中证明了MLNTs在流动状态下仍能稳定响应FUS脉冲,峰值强度在数百个循环中几乎无衰减。随后在小鼠体内,分别在大脑皮层(M1、S1、后压部无颗粒皮层)、肠道、后肢、脊髓均观测到清晰的局部光发射,侧向半高宽集中在100–200 μm量级。
图2:基于MLNT的超声扫描光源
2. 电生理学与c‑Fos:神经元被激活了
使用Thy1‑ChR2‑YFP转基因小鼠,研究者同时进行光纤电生理记录与FUS刺激。结果清晰显示:
-
仅在MLNTs注射 + FUS开启的条件下,神经元出现脉冲锁定的动作电位发放(1 Hz和10 Hz均有效);
-
单独FUS(无MLNTs)或单独MLNTs(无FUS)均不产生显著放电,排除了超声直接机械敏感效应和热效应(ΔT≈0.6 ℃@1 min);
-
记录到的响应率接近100%(在MLNTs+/FUS+条件下)。
c‑Fos免疫染色进一步验证:M1、vDG、脊髓T12段等目标区域出现显著c‑Fos升高,而对侧未刺激区域及各项对照组均无显著变化。激活体积的侧向FWHM≈341 μm,轴向≈1.4 mm,总激活体积0.085 mm³——与超声焦斑尺寸一致,证明光从血管内向脑实质穿透足以激活神经元,无需MLNTs穿越血脑屏障。
图3:循环系统中的超声扫描光源
3. 自由活动行为操控:从“亮光”到“转向”
最具冲击力的实验是在自由活动小鼠上完成的。研究者在D1‑Cre(直接通路)和A2a‑Cre(间接通路)小鼠中,通过全身注射Cre依赖的AAV‑ChR2,实现纹状体特定表达光敏感通道。随后使用头戴式可穿戴超声换能器(质量仅0.78 g),在自由活动状态下依次将超声焦点切换到左侧或右侧纹状体。
图6:超声扫描光源能够动态定位自由活动小鼠的大脑深部不同区域
-
D1‑Cre::ChR2‑YFP小鼠:左侧纹状体光刺激诱发顺时针旋转,右侧刺激诱发逆时针旋转(旋转速度显著增加,p < 0.001);
-
A2a‑Cre::ChR2‑YFP小鼠:旋转方向相反,符合直接/间接通路的功能对立;
-
所有对照组(无MLNTs、无FUS、无ChR2表达)均不产生定向旋转行为。
该结果首次在自由活动动物中证明,非侵入式、全身动态光遗传操控可以特异性、可重复地驱动复杂行为输出。
从神经科学到全身光控生物学的范式跃迁
本技术的意义远不止于光遗传学的“无线化”。研究者指出,这套FUS‑MLNTs平台可被视为一种体域光接口——任何需要光作为输入或输出的生物过程,都有可能被重构。
1. 短期应用(3–5年)
-
神经科学基础研究:在多脑区、多时间点、同一动物体内进行因果测试,无需为每个靶点植入光纤,将极大加速环路功能图谱的绘制。
-
脊髓与外周神经调控:脊髓T12段的激活实验表明,该技术可触及传统植入手段风险极高的区域,对疼痛、运动康复研究具有直接价值。
2. 中期应用(5–10年)
· 光遗传学治疗:对于需要长期、可调节的光刺激(如视网膜色素变性、癫痫、帕金森病),该技术提供了一种非植入、可重复干预的潜在路径。
· 光控基因编辑/药物释放:论文在展望部分明确提到,该平台可与光诱导CRISPR‑Cas9、光动力疗法、光触发药物释放相结合,实现深部肿瘤的精准治疗或原位基因修复。
3. 长期愿景
“该技术奠定了可重构、光驱动的新一类生物技术的基础,其应用范围可覆盖生理学、神经生物学、医学、影像学等领域。”
如果后续研究能够解决纳米材料的长期生物降解与清除、超声焦点在更大动物(如非人灵长类)中的穿透深度与分辨率折中,以及可穿戴超声阵列的全脑覆盖成像与刺激集成,我们或许真的能迎来一个 “全身光学可编程” 的时代。
局限性不可忽视
尽管该研究成果极具启发性,但作为技术报道,必须客观列出现阶段的短板:
1. 纳米材料的长期安全性仍需验证
虽然1周和4周的血液学、组织学及神经炎症(NeuN、GFAP、Iba1)检测均未见显著异常,但更长时间(如3–6个月)的慢性毒性与免疫原性数据尚未提供。此外,研究中观察到白细胞计数有轻度升高,作者也坦承“值得进一步研究”。
2. 超声穿透深度与空间分辨率的固有折中
在小鼠体内,1.5 MHz换能器可获得约1 mm的侧向分辨率,而5.7 MHz可低至0.18 mm,但后者在更深组织(如人类大脑)中的穿透能力将显著下降。从啮齿类向灵长类乃至人体的转化,焦距和频率的选择将面临更复杂的权衡。
3. 对照实验仍存在可讨论的空间
虽然作者用多个对照组排除了超声直接机械敏感通道激活和热效应,但超声是否可能通过间接听觉通路(耳蜗)引发非特异性皮质激活——这一问题在以往的超声神经调控文献中被多次讨论——在本研究的行为实验中,自由活动小鼠是否完全不受超声噪音影响,尚需更严格的实验设计(如耳蜗破坏对照)加以澄清。
4. 全身光发射的效率问题
论文补充材料中给出MLNTs的血浆半衰期约为20 分钟,意味着在单次注射后,有效光强随时间迅速衰减。对于需要长时间、多轮刺激的实验,可能需要多次注射或持续性静脉输注,这在转化到临床时会引入新的复杂性。
结语:这项研究提供了一种极具原创性的解决方案,将聚焦超声的深层穿透能力与力致发光纳米材料的原位光发射相结合,第一次在自由活动动物中实现了非植入、全身动态、细胞类型特异性的光遗传操控。它不完美,但它为“光与生物体之间的无线接口”指出了一个值得奋力追逐的方向。
Jiang, S., Malinao, M.G., Yang, F. et al. An ultrasound-scanning in vivo light source. Nat. Mater. (2026).
https://doi.org/10.1038/s41563-026-02556-z
END
撰文 | 郝娅婷
编辑 | 周宇茜
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,参与线上线下交流活动