星标“医工学人”,第一时间获取医工交叉领域新闻动态~
在生物医药研发的漫长征途中,临床试验一直被视为最昂贵且最易失败的环节。长期以来,科学家们对患者状况的评估依赖于“快照式”的点状采样——即患者每隔数周前往医院进行一次短暂的检查。然而,正如一张静态照片无法完整讲述一场电影的剧情,这种稀疏的监测往往会遗漏药物在真实世界环境中的瞬时效应、副作用以及长期的行为变化。
现在,一场无声的革命正在发生。随着传感器、柔性电子学和人工智能算法的协同突破,可穿戴技术正在将临床试验从“诊所中心化”推向“患者中心化”的实时监测时代。根据发表在《自然·药物发现》(Nature Reviews Drug Discovery)上的最新综述,研究人员对2001年至2025年间注册的1021项干预性临床试验进行了系统分析,揭示了可穿戴设备如何从早期的探索性工具,演变为现代药物开发协议中的结构化组件。这不仅是硬件的升级,更是一次关于“临床有效性”定义的深层重塑。
要理解这场革命,首先需要解析可穿戴设备是如何将人体的物理与生理信号转化为“数字终点”的。可穿戴技术的核心在于生物计量监测技术(BioMeTs),它们利用多样的传感器模态,捕捉那些曾经难以量化的生命体征。
惯性测量单元(IMU)是目前临床试验中部署最广泛的传感器。通过集成三轴加速度计和陀螺仪,设备能够捕捉线加速度和角速度。在临床中,这些原始信号经过降噪和特征提取,可以计算出步数、步态速度、步频变异性、震颤振幅、姿态转换等关键指标。
这些指标在神经退行性疾病(如帕金森病和多发性硬化症)的药物试验中具有不可替代的价值。例如,传统的帕金森病评估依赖于UPDRS评分量表,这带有强烈的主观性且易受“白大褂效应”影响;而IMU传感器能够24小时记录患者在居家环境中的震颤和运动迟缓情况,提供更高分辨率的药效学数据。
光电容积脉搏波(PPG)是智能手表和贴片中的核心技术。它利用LED(通常是绿光用于心率,红光和近红外光用于血氧)向皮肤组织发射光束,并由光电二极管测量光强的变化。这种波形反映了心脏搏动导致的微血管血容量变异。
通过对PPG信号的处理,可以衍生出心率(HR)、心率变异性(HRV)和外周血氧饱和度(SpO2)。 然而,光学传感在临床应用中面临一个关键挑战:皮肤色素沉着偏差。深色皮肤会吸收更多的红光和近红外光,可能导致SpO2估值产生约1.5%的系统性偏差。这一技术细节正促使监管机构要求药企在验证数字终点时,必须考虑人群多样性和公平性。
心电图(ECG)传感器通过皮肤电极测量心脏电活动。相比于腕式设备的点测,贴片式ECG(如Zio贴片或Vivalink系统)支持长达数周的连续监测,能够精确测量PR、QRS和QT间期。这对于评估新药的心脏毒性——特别是可能引起心律失常的QT间期延长效应至关重要。
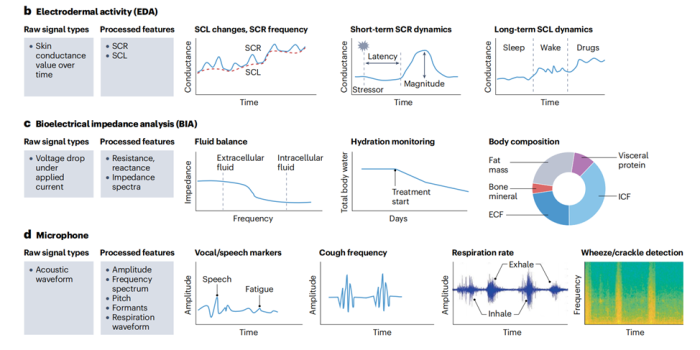
此外,皮肤电活动(EDA)传感器则通过测量汗腺分泌引起的皮肤电导变化,反映交感神经系统的激活水平。这在疼痛管理、焦虑症以及重度抑郁症的临床研究中,被用作评估药物改善患者应激反应的客观生物标志物。
下表总结了目前临床试验中主流传感器的技术原理及应用领域:
对1021项临床试验的分析揭示了可穿戴设备在药物研发协议中的五大功能原型。这一分类反映了数字工具在试验设计中角色的不断深化。
这是最基础也最普遍的范式(约占试验总数的74%)。在这种模式下,可穿戴设备作为非侵入性的观察工具,捕捉患者对干预药物的生理或行为反应,而其数据不直接改变治疗决策。
早期的标志性研究如2004年的NCT00084669,利用腕式活动仪评估抗抑郁药文拉法辛对睡眠效率的影响。设备揭示了传统量表无法捕捉到的细微睡眠碎片化现象,证明了高分辨率数据在发现“隐形成效”或副作用方面的优势。到了2025年,罗氏(Roche)等巨头已广泛在癌症试验中使用智能手表监测患者的疲劳、活动度和睡眠模式,作为衡量药物耐受性和生活质量的数字终点。
在此原型中,可穿戴设备产生的数据直接决定或调整药物剂量。这标志着“闭环医疗”的初步实现。典型的例子是人工胰腺系统(如NCT00797823)。通过实时获取连续葡萄糖监测(CGM)数据,算法会自动调整胰岛素泵的输出速率,从而实现比手动给药更精准的血糖控制。这一范式正扩展到其他领域,如利用传感器监测血液中的药物浓度或生理指标,动态调整化疗药物或免疫抑制剂的用量,以最小化副作用。
药物不依从是导致临床试验失败的主因之一。新型依从性工具包括可吞服的“数字药片”(Digital Pill)。当带有微型传感器(如无线射频标签)的药片进入胃部并与胃酸接触时,它会向佩戴在身上的贴片发送信号。在针对严重精神疾病患者的NCT03568500试验中,研究人员利用这种技术实时追踪抗精神病药物的服用情况。这使得依从性不再是一个依赖患者回忆的模糊统计值,而是一个精确的时间戳变量,从而极大地减少了量效模型中的噪声。
在这种情况下,可穿戴设备本身即为给药系统。例如,一次性胰岛素贴片泵集成了压力和流量传感器,能够实时记录每一次基础给药和推注动作。 此外,一种创新的柔性光疗贴片(NCT02735187)正被用于银屑病的治疗,它通过嵌入的LED直接对病灶施加光疗,同时记录皮肤温度和辐照能量,确保剂量的精确输送。
在此原型中,药物剂量是固定的,但通过可穿戴设备生成的标准化终点来比较不同的给药途径(如吸入vs注射)、给药时间或制剂配方。
尽管可穿戴设备的部署量呈爆炸式增长,但将其生成的指标正式认证为药物审批的“主要终点”依然面临极高的准入门槛。一个数字测量值要转化为合格的临床终点,必须经历“验证-分析验证-临床验证”(V3)框架。
步速第95百分位数(SV95C)是数字终点发展史上的一个里程碑。它由佩戴在踝部的IMU传感器产生,用于衡量杜氏肌营养不良症(DMD)患者在真实世界中能达到的最高步态速度。
2019年,EMA首先将其认证为次要终点,随后在2025年前后正式升级为主要终点。这是全球首个获得监管正式资质的、基于可穿戴设备的步行能力指标。这一资质不仅缩短了DMD药物的开发周期,还使得像Sarepta的Elevidys基因疗法和Dyne Therapeutics的DYNE-251研究能够利用更具代表性的真实世界数据来证明疗效。
长期以来,糖化血红蛋白(HbA1c)是糖尿病试验的金标准。然而,HbA1c仅能反映过去三月的平均水平,无法捕捉严重的低血糖或剧烈的血糖波动。
基于CGM数据的“范围内时间”(TIR,血糖处于70-180 mg/dL的时间占比)正迅速获得认可。虽然尚未在所有地区完成正式的终点资质认证,但FDA已在其指南中明确认可TIR作为有效的替代终点,并已允许将其纳入药品标签中。
可穿戴终端的应用并非坦途。在Bellerophon公司针对肺动脉高压的REBUILD试验中,FDA曾破天荒地允许将中高强度体力活动(MVPA)作为主要终点。然而,该试验在三期阶段因未能在MVPA指标上观察到显著差异而以失败告终。
这一失败提醒研发者:即使终点在技术上是可测量的,它是否对治疗方案的变化足够敏感,以及如何排除患者生活习惯等外界噪声的干扰,仍然是数字化临床试验的核心挑战。
随着材料科学和微型化的突破,原本属于大型实验室的检查正在缩小并贴在皮肤上。这不仅增加了患者的便利性,更为“数字表型”的构建提供了前所未有的深度。
传统血压计需要充气袖带,无法实现24小时的连续自然监测。瑞士公司Aktiia的G0监测系统(Hilo Band)已获得FDA的510(k)认证,这是首个获得此类认证的OTC无袖带设备。它利用手腕PPG波形的形态学分析,结合人工智能模型,能够估算出收缩压、舒张压和平均动脉压。在抗高血压药物的试验中,这种设备可以揭示药物是否能有效控制夜间血压波峰(Nocturnal Dipping),这对于降低心肌梗死和中风风险具有极高的预测价值。
葡萄糖监测只是开始。新兴的微丝贴片正瞄准更复杂的分析物,如乳酸、皮质醇、电解质以及抗生素浓度。
Biolinq Shine:
2025年获得FDA De Novo认定,是全球首个“无针”葡萄糖传感器。它利用比传统针头浅20倍的微丝阵列,几乎无痛地监测组织间液。更重要的是,它是首个将代谢(血糖)、活动和睡眠数据集成在单一贴片中的产品,为2型糖尿病药物的研发提供了多维度的评估视角。
Xsensio Lab-on-Skin:
这家瑞士初创公司开发的模块化芯片能够同时捕捉皮质醇(应激)、雌二醇(女性健康)以及万古霉素等窄治疗窗药物的浓度。这为临床试验中的实时药效学(PD)分析打开了新窗口。
不同于依赖LED的光学传感器,中红外光谱能够直接检测特定分子的振动特征模式。Rockley Photonics利用硅光子学技术开发的微型MIR光谱仪,已经展示了在手腕上非侵入性监测心脏肌钙蛋白I(cTnI)的能力。 肌钙蛋白是急性冠脉综合征的金标准生化标志物,能够连续监测其微量变化,意味着我们可以在患者感到胸痛之前就预测到潜在的心脏损伤。
这是目前最前沿的研究方向。传统超声体积庞大且依赖专业操作。现在,利用柔性压电聚合物和微机电系统,研究人员开发出了超声贴片。
● MIT 赵选贺团队开发的水凝胶杂化贴片,可实现长达48小时的内部器官、血管及心脏的连续成像。
● iSono Health ATUSA:这种可穿戴式3D乳腺超声系统已获得FDA批准。它采用操作员无关的设计,能够在几分钟内完成乳腺全扫描,极大降低了基层医疗进行高质量肿瘤筛查的门槛。
● Sonus Microsystems:该公司正与Providence HealthCare合作验证一种用于心力衰竭监测的超声贴片。该贴片能够自动记录射血分数和心脏杂音的变化,从而在心衰患者病情恶化导致住院之前发出警报。
这项技术的普及不再仅限于学术实验室。2026年3月,Alphabet旗下的Verily宣布与三星电子达成里程碑式的合作,将三星Galaxy Watch 8的硬件能力与Verily的Pre临床证据平台进行端到端整合。
这次合作的关键在于,三星首次向药企开放了手表的“原始传感器信号”(Raw Device Signals),包括未经处理的PPG和运动原始数据。 此前,药企只能获取厂家算法处理后的步数或心率平均值,这就像是只能看剧情梗概而不能看电影样片。通过获取原始数据,药企可以开发自己的专有算法,挖掘与特定药物反应相关的微小信号,极大地加速了定制化数字终端的开发。同时,Apple也在通过其“Apple Health Study”持续深化其在心血管、认知健康和听力领域的真实世界证据收集。 这种由科技巨头构建的底层设施,正在大幅降低临床试验招募和远程监测的经济成本。
尽管愿景宏大,但要让可穿戴技术在药物开发中达到与“血液检查”同等的地位,仍需解决三大核心挑战。
可穿戴设备产生的数据量是天文数字级的。一秒钟的IMU数据可能包含100个采样点,一天的连续记录就是数千万行数据。如何从海量噪音中提取出具有临床意义的特征?目前行业仍缺乏标准化的特征定义。不同品牌的手表计算“步数”的算法各异,这给跨中心、多设备支持的全球化试验带来了巨大挑战。
一个极其精确但必须每天佩戴12小时、每晚充电且会引起皮肤过敏的设备,其“真实世界效度”几乎为零。研究显示,老年痴呆症患者对具有美学设计感且Symbolize“赋能”而非“残疾”的设备依从性更高。 未来的趋势必然是“不可见”的技术——如集成在日常服装中的智能织物,或者能维持数月续航的微型戒指。
正如前文提到的皮肤肤色对PPG精度的影响,数字终点可能由于算法训练数据的单一性,导致对某些族裔或特定体型人群的药效评估失真。此外,如果临床试验的数据上传依赖于昂贵的高端智能手机,那么这将在无意中排除中低收入国家的患者,加剧全球健康不平等。
我们正在步入一个“软件即药物”(SaMD)与传统分子药物深度融合的时代。未来的临床试验将不再是单一的干预,而是“药物+监测+实时反馈”的闭环系统。
通过部署可穿戴超声贴片、生化微针以及MIR光谱仪,药物研发者将不再需要猜测药物在患者体内的表现。他们将拥有一个数字化的“透明人体”图谱。这不仅能通过早期识别“无反应者”来降低临床试验的失败率,更能帮助开发出真正个性化的给药方案。
从杜氏肌营养不良症患者踝部感应到的微弱加速度,到血糖波动曲线中隐藏的代谢密码,可穿戴技术正在将人类健康的无声语言,翻译成科学研发的精准指针。这不仅仅是工具的进步,更是人类对生命奥秘理解方式的一次彻底重校。
https://www.nature.com/articles/s41573-026-01403-9
END
撰文 | 赵亚军
排版 | 王可豪
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动