星标“医工学人”,第一时间获取医工交叉领域新闻动态~
一项发表于《自然》的研究分析了50万成年人的睡眠数据与23种生物衰老时钟,发现每天6-8小时睡眠与较低的早逝和疾病风险相关。但研究同时揭示:不同器官——心脏、大脑、肾脏——对睡眠时长的“最优解”各不相同,且因人、因性别而异。这为“睡眠作为可干预的抗衰老工具”提供了迄今最全面的量化依据,但也暴露了一个核心悖论:我们离个性化睡眠处方还有多远?
关于睡眠时长与健康的关系,过去几十年里,公众接收到的信息可谓众说纷纭。有人宣扬“8小时定律”,有人鼓吹“短睡基因”的优越性,更有大量商业化睡眠追踪设备输出着各自为政的“睡眠评分”。
问题的核心在于:传统的流行病学研究大多依赖自我报告的睡眠时长和粗略的健康结局(如死亡或特定疾病诊断)。这种方法存在两个致命缺陷:
第一,因果关系难以厘清。是睡眠不足导致了衰老,还是衰老(及其伴随的慢性疼痛、夜尿频繁、焦虑情绪)破坏了睡眠?
第二,缺乏器官层面的分辨率。人体并非一个均质的整体——大脑的老化速度可能快于心脏,而肾脏可能又另有节奏。仅仅用一个“生物年龄”指标来评估睡眠的影响,无异于用平均温度描述一个房间的热点与冷点。
正如哥伦比亚大学计算神经科学家、同时也是本文第一作者的Wen Junhao所言:“睡眠可能更多地受环境影响,而不是由基因决定。”这一判断本身就带有强烈的实用主义色彩——如果睡眠主要是可变的,那么它就是可干预的。问题在于:干预的目标究竟是什么?
这项研究的核心武器,并非新的临床试验或睡眠实验室数据,而是一个庞大且成熟的数据库——UK Biobank,涵盖超过50万人的长期健康追踪数据,包括生活方式问卷、脑影像、血液样本等。
研究团队没有止步于单一的“生物年龄”指标,而是使用了23种不同的生物衰老时钟,分别对应17个器官或系统。这些时钟的构建方式包括:
-
蛋白质组学时钟:基于血液中特定蛋白的浓度变化
-
代谢组学时钟:基于代谢物谱
-
影像学特征时钟:基于医学影像中的结构性指标
| 关键发现:并非所有器官的“最佳睡眠时长”都相同。
根据文中数据:
|
器官/系统 |
时钟类型 |
最佳睡眠时长 |
解读 |
|
心脏 |
蛋白质组学时钟 |
6小时 |
低于或高于此值均与加速老化相关 |
|
大脑 |
蛋白质组学时钟 |
8小时 |
与心脏存在显著差异 |
|
整体健康 |
综合多种时钟 |
6-8小时区间 |
U形曲线的最低点在此范围内 |
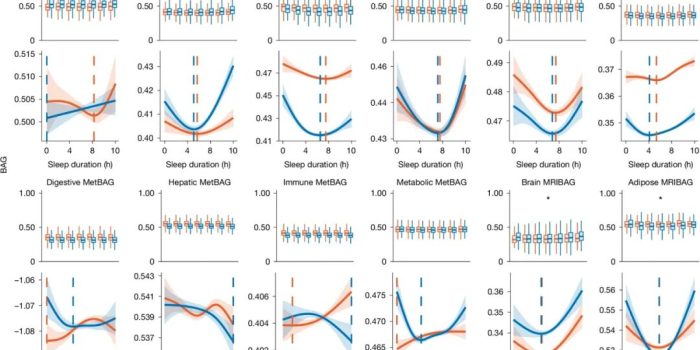
图1:睡眠图表划分了睡眠时长与生物老化时钟之间的U型模式。
更为微妙的是,这种“最优时长”在男性和女性之间也存在差异——尽管论文没有给出全部性别分层数据,但已明确指出“在某些情况下,最佳睡眠时间因性别而异”。
这种器官特异性的发现,颠覆了以往“一刀切”式睡眠建议的科学基础。它暗示:一个人可能需要为保护大脑而睡足8小时,但同样的时长对心脏而言可能已进入“过量”区间——这是一种内生的、需要权衡的生物学矛盾。
Wen本人对此持谨慎态度。他在接受《自然》采访时坦言:“我个人认为这是双向的。”
这一判断并非客套,而是反映了生物衰老研究中的一个根本性难题:纵向观察研究无法真正剥离因果方向。
-
一种解释(因果正向):睡眠时长通过影响炎症水平、代谢调控、神经元修复等通路,直接加速或延缓生物老化。
-
另一种解释(反向因果):某些潜在的衰老过程——例如亚临床的心血管病变或早期的神经退行性改变——会通过改变睡眠调节中枢的功能,反过来缩短或延长睡眠。
研究团队对此的处理方式是坦诚的:他们没有声称发现了因果机制,而是提供了一个高分辨率的关联图谱。这张图谱的价值在于,它可以为后续的机制研究和干预试验提供精确的靶点假设。
|正如未参与该研究的Karolinska Institute神经流行病学家Abigail Dove所言:“睡眠影响身体的每一个器官,而且睡眠在一定程度上是可以调整的。这是一个可能有帮助的工具。”
注意专家的用词——“可能有帮助”。这不是科学家的保守,而是对现有证据强度的如实描述。
这项研究的技术贡献可以归纳为三个层面:
第一,方法论层面。 它展示了如何利用大规模生物银行数据和多维度“衰老时钟”来解析一个常见暴露因素(睡眠时长)的复杂效应。这种方法框架本身可以迁移到饮食、运动、社会关系等其他“生活方式药物”的研究中。
第二,公共卫生层面。 6-8小时的“黄金区间”虽然不适用于每一个个体,但在群体层面提供了迄今最可靠的参考范围。对于睡眠医学临床实践中的“正常范围”界定,这是一个重要的循证更新。
第三,产业层面。 可穿戴设备市场(Apple Watch、Oura Ring、Whoop等)长期以来缺乏基于器官特异性衰老时钟的睡眠建议算法。这项研究提供的23个时钟框架,有可能催生下一代个性化睡眠推荐引擎——不再是简单地告诉你“睡了7小时,不错”,而是根据你的心脏蛋白谱、脑影像特征(如果能获取)给出针对性建议。
但商业化道路上的障碍同样显著:
-
数据门槛:蛋白质组学和影像学数据目前无法通过消费级设备获取。要真正实现器官层面的睡眠个性化,需要成本极低的生物标志物检测方案。
-
个体差异:研究发现的“U形曲线”在不同时钟、不同性别、不同器官之间位置不同。如何为一个具体的人整合这些相互冲突的“最优建议”?这需要更复杂的决策算法。
-
干预证据缺失:目前的数据仍然是关联性的。要证明“调整睡眠到最佳时长能逆转或延缓生物老化”,需要随机对照试验。
杜克大学生物医学工程师Alexandra Badea的评论颇为传神:“这就像我祖母告诉我的——‘你必须照顾好自己的整体健康,这些系统是相互对话的。’”
换言之,睡眠不是孤立的杠杆,而是嵌入在一个复杂的生理网络中的节点。调整它会有影响,但影响的方向和幅度取决于网络的其他部分。
行文至此,有必要列出这项研究的几个关键局限性:
-
人群偏倚:主要基于UK Biobank参与者。该队列总体比英国普通人群更健康、白人占比更高、社会经济地位更高。结果不一定能直接推广到其他种族、地区或社会经济群体。
-
睡眠时长的测量方式:研究主要依赖基线时的自我报告或简化的问卷数据。没有使用多导睡眠图(PSG)或长期可穿戴设备追踪,因此无法区分睡眠连续性、睡眠阶段分布、睡眠规律性等同样重要的维度。
-
时钟的生物学意义:23个生物衰老时钟虽然在预测健康结局方面有不同程度的验证,但“时钟加速”并不等同于“疾病发生”。它是一个风险指标,而非诊断指标。
-
混杂因素:尽管研究控制了多种混杂因素,但睡眠时长与衰老之间的关联仍可能受到未被测量的变量(如慢性压力的持续时间、轮班工作史、社会孤立程度)的影响。
|最终,这项研究给出的最有力信息或许不是“你应该睡X小时”,而是:关于睡眠与衰老的关系,我们已经可以提出器官级别、性别特异性、可量化的科学问题了。而提出正确问题,往往是解决它的第一步。
The MULTI Consortium., O’Toole, C.K., Song, Z. et al. Sleep chart of biological ageing clocks in middle and late life. Nature (2026). https://doi.org/10.1038/s41586-026-10524-5
END
撰文 | 郝娅婷
编辑 | 吴苡齐
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动