星标“医工学人”,第一时间获取医工交叉领域新闻动态~
哺乳动物无法感知近红外光,因为其能量太低、热噪声太高。2026年4月13日发表于《Nature Electronics》的一项研究,展示了一款厚度仅360纳米滤光片、搭配液态金属三维微电极的植入式人造视网膜。该器件在盲鼠体内成功诱导出对近红外的皮层响应和行为反应,且完全不干扰原有的可见光视觉。
人类视觉的“光谱边界”是由进化设定的。视蛋白的光吸收特性决定了我们只能感知400–700纳米的可见光。近红外波段(如900纳米)的光子能量更低,若要感知它,需要更低能垒的视蛋白——但这会带来极高的热噪声,使得近红外视觉在生物进化上“不划算”。因此,迄今为止,没有任何哺乳动物具备感知700纳米以上光线的天然能力。
然而,失明人群的需求改变了这一问题的优先级。
在视网膜疾病(如色素性视网膜炎、年龄相关性黄斑变性)中,外层的光感受器细胞逐渐退化,但内层的神经节细胞和双极细胞往往仍然完好。这意味着:如果能绕过退化的光感受器,直接用电子器件刺激存活的神经元,就有可能恢复视觉功能。
现有的视网膜假体(如Argus II)采用的是电刺激阵列,但其问题显而易见:刚性电极与柔软视网膜之间的机械失配(杨氏模量相差3个数量级以上),容易造成组织损伤;而且它们通常只提供单一的人工视觉通道,无法与患者残余的自然视觉共存。
更关键的是,这些器件大多仍工作在可见光波段,而可见光本身就正是退化光感受器“失灵”的波段——这就像在一个已经坏掉的收音机上继续调频,方向本身就值得商榷。
这项研究的核心贡献,可以用一句话概括:在不干扰可见光感知的前提下,为视网膜增加一个近红外通道。
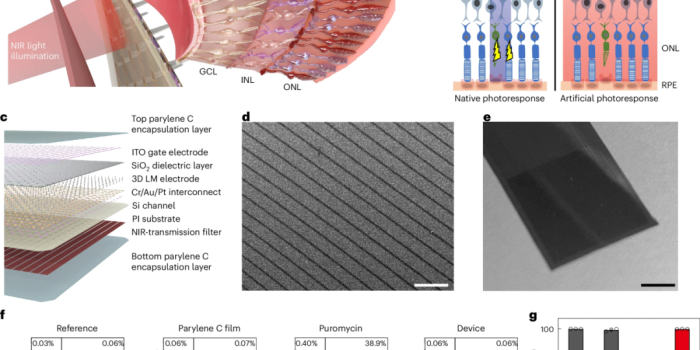
图1 | 近红外感知人工视网膜。
实现这一目标,需要同时解决三个工程问题:光谱分离、柔性电荷注入、以及共存式器件架构。
1. 光学层:360纳米厚的近红外透射滤光片
研究团队设计了一个由非晶硅和二氧化硅交替堆叠的7层滤光片,总厚度仅360纳米。其光学设计基于Herpin等效折射率,中心波长设在520 nm。实测表明:
-
可见光波段(440–600 nm)被有效阻断;
-
900 nm附近的近红外光可以透过,到达下方的光电晶体管。
这意味着:可见光只能通过滤光片之间的间隙(间距40微米)到达天然光感受器,而近红外光则专门驱动电子通道。两者在空间上被编码在同一器件中,互不干扰。
2. 传感层:硅基光电晶体管阵列
器件采用单晶硅沟道(厚度1.5微米)的场效应晶体管结构,在900 nm近红外照射下,漏极电流随光强线性变化(0–1.2 mW/cm²),响应/恢复时间均为10 ms。
关键参数:
-
迁移率:166 cm²/V·s
-
开关比:4.41×10⁶
-
阈值电压:4.08 V
该性能足以产生1–20 µA的刺激电流,恰好落在视网膜神经元有效响应区间内。
3. 电极层:液态金属3D微柱
这是整个器件在生物机械匹配上的最大亮点。
传统刚性电极(如铂、金、碳)的杨氏模量在GPa级别,而视网膜组织仅为数百kPa。这种差异会导致微动损伤和胶质疤痕形成。本研究采用液态金属EGaIn(镓铟合金)打印出直径20 µm、高60 µm的3D微柱电极,其有效杨氏模量仅236 kPa,与巩膜、角膜和视网膜组织相当。
在电化学性能上:
-
1 kHz阻抗:210 kΩ(电极面积32.1 µm²)
-
阴极电荷存储容量:34.28 mC/cm²
-
电荷注入容量:9.35 mC/cm²
-
加速老化10天(模拟生理条件下约10个月):阻抗仅从234.6 kΩ升至253.6 kΩ,电荷注入容量基本稳定
图2 | 光电和电化学特性。
铂纳米团簇仅沉积在电极尖端,进一步降低了阻抗,并将电场聚焦在尖端,比平面电极刺激效率更高。
|
参数 |
传统刚性电极 |
本研究液态金属电极 |
|
杨氏模量 |
~GPa |
236 kPa |
|
与组织匹配度 |
差(机械损伤风险) |
接近(低应力) |
|
1kHz阻抗 |
较高 |
210 kΩ(优化后) |
|
尖端结构 |
平面或微加工 |
3D打印微柱+局部Pt |
|
长期稳定性 |
依赖封装 |
10天加速测试稳定 |
“液态金属电极增强了与视网膜神经节细胞的接近度,提供了有效的电荷注入,同时由于其低杨氏模量,最大限度地减少了组织损伤。” —— 论文原文
离体验证:健康与盲鼠视网膜均产生响应
研究团队分别取健康小鼠(C57BL/6J)和视网膜退行性小鼠(rd1)的离体视网膜组织(4×4 mm),直接放置在器件上,使3D液态金属电极朝向神经节细胞层。
图3 | 视网膜反应的体外评估
在器件不工作的情况下:
-
健康视网膜对可见光(470 nm)产生92 µV的响应;
-
对近红外(900 nm)几乎无响应。
在器件工作的情况下:
-
健康视网膜对近红外产生86 µV的电诱发电位,与可见光下的自然响应(88 µV)几乎相同;
-
盲鼠视网膜在近红外照射下也产生了类似的电活动,且发放率随光强增加而增加(0–1.2 mW/cm²)。
结论:该器件能够将近红外输入转化为与天然可见光响应相当的神经活动,且健康与盲鼠之间的发放率无显著差异——因为两者都对近红外没有天然响应,都依赖人工刺激。
在体验证:皮层记录与行为学双重确认
在活体小鼠中,研究团队同时植入视网膜器件和脑深部探针(靶向初级视觉皮层V1第4层,该层信号最强)。
图4 | 体内诱导RD1和WT小鼠的近红外视力。
-
盲鼠(rd1):光感受器已完全退化。不开启器件时,无论可见光还是近红外,均无皮层响应。开启器件后,仅在近红外照射时出现显著的皮层发放活动。
-
健康鼠(WT):开启器件后,对可见光和近红外均产生稳健的皮层响应,且两者发放率相当。
更关键的是行为学实验:在水限制条件下,小鼠被训练将光脉冲与水奖励关联。结果显示:
-
植入器件的盲鼠对近红外提示产生明显的预期舔水行为,且舔水率随近红外光强增加而增加;
-
未植入器件的对照鼠对近红外无任何行为反应;
-
植入器件的健康鼠对可见光和近红外均产生行为反应。
这证明:该器件不仅产生了电生理信号,而且真正被小鼠感知并用于指导行为。
对医疗领域的意义
这项技术的直接目标人群是光感受器退行性失明患者(如晚期色素性视网膜炎)。他们的内层视网膜(神经节细胞、双极细胞)仍然完好,是电刺激的理想靶点。
与现有视网膜假体相比,这套方案有三个显著差异:
-
光谱分离:不干扰残余自然视觉。临床研究已表明,AMD患者可以同时使用假体中心视觉和自然周边视觉,本文的设计将这一理念推向了更精细的波长层面。
-
机械匹配:液态金属电极的低模量大幅降低了长期植入的组织损伤风险。6个月的组织学分析未发现胶质增生或微胶质激活。
-
近红外通道:在暗环境下,患者可以通过外部近红外光源“看见”环境,而无需依赖可见光——这对于夜盲症患者尤其有价值。
商业化距离
目前仍处于动物模型验证阶段(小鼠)。进入人体临床试验之前,还需要解决以下几个关键问题:
-
长期稳定性:10天加速老化测试相当于约10个月,但人体植入需要数年乃至数十年的可靠性。液态金属在长期电化学环境中的稳定性仍需进一步验证。
-
器件微型化与功耗:当前器件采用单晶硅沟道,仍有一定刚性。未来可替换为柔性、高近红外响应的半导体纳米材料,进一步降低功耗、增强结构柔顺性。
-
背景噪声抑制:太阳光中也有近红外成分。研究团队提出了多层光学滤波策略(频率滤波、带宽调谐、角度选择性),可将透射峰控制在950–1050 nm窄带内,并在入射角超过10°时将透射率降至0.5以下。这些设计需要在真实户外环境中验证其抗干扰能力。
更远的可能性
作者在论文末尾指出:通过改变光电晶体管的沟道材料或滤光片结构,这套机制可以扩展到紫外或其他波段。这意味着,“人造光谱扩展”可能成为一个通用技术平台——不仅仅是恢复失去的功能,而是赋予生物体原本不具备的感知能力。
这篇论文的技术完成度很高:从材料表征、离体电生理、在体皮层记录到行为学验证,证据链条完整。影响因子40.9和Nature Electronics的刊发也印证了其学术价值。
但我们需要警惕几个容易被忽略的问题:
第一,小鼠与人类视网膜的尺度差异。 小鼠眼球直径约3 mm,人类约24 mm。电极高度(60 µm)在小鼠中恰好到达神经节细胞层,但在人类视网膜中,这一距离会显著不同。器件结构需要重新优化,而这可能影响其电荷注入效率和选择性刺激能力。
第二,行为学实验的时间尺度。 研究中的行为测试是在短期内完成的。长期植入后,组织是否会形成纤维包裹?液态金属是否会泄漏?铂纳米团簇是否会脱落?这些问题需要更长时间的动物实验来回答。
第三,伦理与“增强”的边界。 这项技术本质上是感官增强,而不仅仅是医疗修复。如果它能安全地让健康人也获得近红外视觉,那么我们是否应该允许?这类讨论在脑机接口和感官替代领域已经存在,而本文的进展将使其更加紧迫。
这项研究最值得关注的,不是它“做了”什么,而是它“打开了”什么——一个可以独立于自然视觉、由工程设计决定的光谱通道。这不再是修复,而是定义。
[1] Chung, W.G., Jeong, I., Lee, EJ. et al. An implantable epiretinal device for near-infrared light perception. Nat Electron (2026).
https://doi.org/10.1038/s41928-026-01601-8
END
撰文 | 郝娅婷
排版 | 张艳青
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,参与线上线下交流活动