星标“医工学人”,第一时间获取医工交叉领域新闻动态~

引言:心脏起搏器的终极疆域——从“寿命受限”到“生命共生”
目前的商用无导线起搏器,如 Micra AV2 或雅培(Abbott)的 Aveir 系列,虽然其电池寿命通过超低功耗电路和高级算法已延长至 15 到 20 年,但对于中青年患者或长寿老人而言,这依然意味着在其生命周期内需要进行多次高风险的更换手术。考虑到无导线起搏器直接通过镍钛合金挂钩(Tines)或螺旋(Helix)锚定在心肌深处,取出旧器械的操作极具挑战性且伴随血栓或心肌损伤风险,而简单地在心脏内“堆积”报废器械显然不是长久之计。因此,如何跨越电池能量密度的物理极限,实现起搏器的“终身服务”(Lifelong Service),成为了生物医学工程领域公认的“终极疆域”。
2026 年 1 月,由中国科学院北京纳米能源与系统研究所李舟研究员、王中林院士与阜外医院华伟教授团队共同研发的“共生经导管起搏器”(Symbiotic Transcatheter Pacemaker, STPM)在《自然·生物医学工程》(Nature Biomedical Engineering)正式亮相。这项研究提出了一种革命性的“能源共生”范式:通过在极其有限的体积内集成基于磁悬浮能量缓存结构的电磁感应发电机,STPM 能够将心脏跳动的机械能直接转化为电能,不仅满足了起搏器运行的“临界能量条件”,更在猪类大动物模型中实现了长达一个月的完全自主运行和心律失常治疗。这标志着心脏起搏器正从一个纯粹的“消耗性电子产品”转变为一个与人体生命节律深度融合、能源自给的“人造器官”。

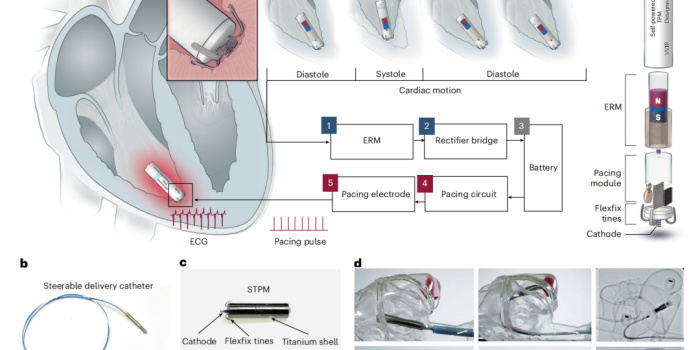
心脏内空间的极其有限性要求自供电起搏器必须在保持微型化(通常小于1㎤)的同时,集成发电机、整流桥、储能单元、感知电路以及起搏电极。STPM 采用了一种“全合一”(All-in-one)的设计逻辑,将能量再生模块(ERM)置于起搏器的核心,这一创举打破了以往自供电系统体积庞大、难以介入输送的瓶颈。
STPM 的物理外壳采用了生物兼容性极高的钛合金外壳,其外部尺寸经过精密设计,以确保能够适配标准的 26 Fr 介入鞘管。其内部结构可以划分为四个核心子系统:
1.能量再生模块(ERM):这是设备的心脏,由一组精密缠绕的感应线圈(约 2300 圈)和磁悬浮结构的活动磁铁组成。
2.电源管理单元:集成微型全波整流桥(KMB14F)和可充电锂离子电池(ML621),负责将发电机产生的交变电流转化为稳定的直流电并储存。
3.起搏控制单元:采用超低功耗的 MSP430 微控制器,负责监测心房/心室电信号并根据预设算法发放起搏脉冲(如 98 bpm,脉宽 0.4 ms)。
4.接口与锚定系统:正极(Anode)为钛壳暴露部分,负极(Cathode)为顶端的柔性镍钛合金弹簧。设备通过四根 Flexfix 镍钛合金勾齿固定在右心室心尖部心肌。
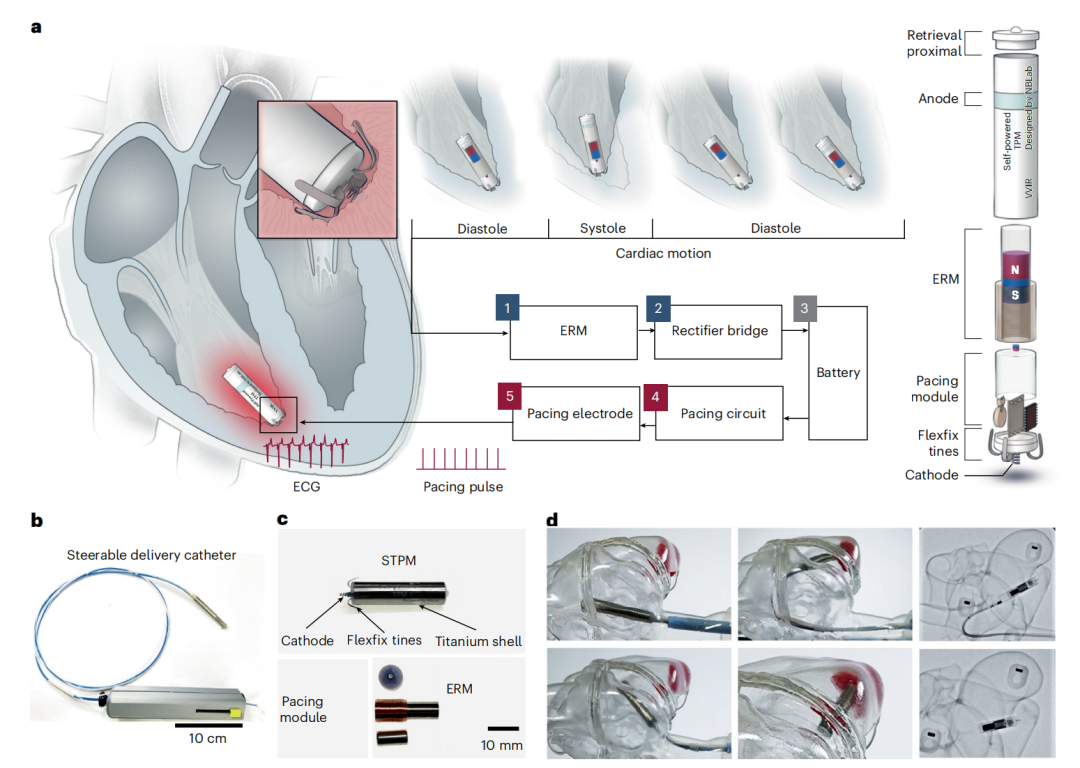
STPM 的设计充分考虑了现有的心脏电生理手术流程。通过可调控的介入导管,医生可以将 STPM 经股静脉、三尖瓣送入右心室心尖部。实验显示,Flexfix 勾齿在推力大于 2 N 时展开,拉力大于 2.6 N 时回缩,确保了植入过程中的位置可调性及术后的稳固锚定(锚定力≧1N)。这种对成熟介入路径的适配,降低了该前沿技术转化为临床应用的门槛。
在微型能量采集器的设计中,最大的敌人并非能量的稀缺,而是摩擦带来的损耗。心脏的跳动频率极低(1-2 Hz),且位移幅度通常不足 10 毫米,传统的摩擦式发电机或带有机械支点的发电机在如此微弱的激励下,往往会因为静摩擦力而无法启动。
研究团队提出了一种“磁悬浮能量缓存结构”(Magnetic Levitation Energy Cache Structure),在该模块中,一个圆柱形活动磁铁(5 mm × 10 mm,N52 钕铁硼)被置于抛光的钛合金管内。管底部固定有一个极性相反的微型磁铁(1.5 mm × 1 mm),利用磁排斥力平衡掉重力,使活动磁铁处于悬浮状态。
这种设计在物理上实现了以下突破:
1.近零启动阈值:由于磁铁与导管壁之间不存在刚性接触,且底部的磁斥力提供了一个非线性的弹性势能梯度,任何轻微的心脏收缩都能打破磁铁的平衡位移,诱发感应电流。
2.动能回收效率最大化:根据法拉第电磁感应定律,感应电动势与磁通量变化率成正比。磁悬浮结构消除了由于机械碰撞产生的能量耗散,使得单次心跳的能量转换效率(Efficiency,η)从普通非悬浮结构的不足 0.1% 猛增至 24% 。
其能量转换效率的计算公式遵循:
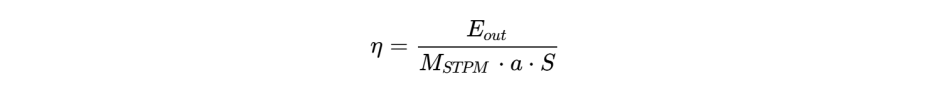
其中,Eout 是 ERM 的输出能量,MSTPM 为设备质量(4.2 g),a为心脏加速度,S为活动磁铁的最大位移距离(约 8.6 mm)。
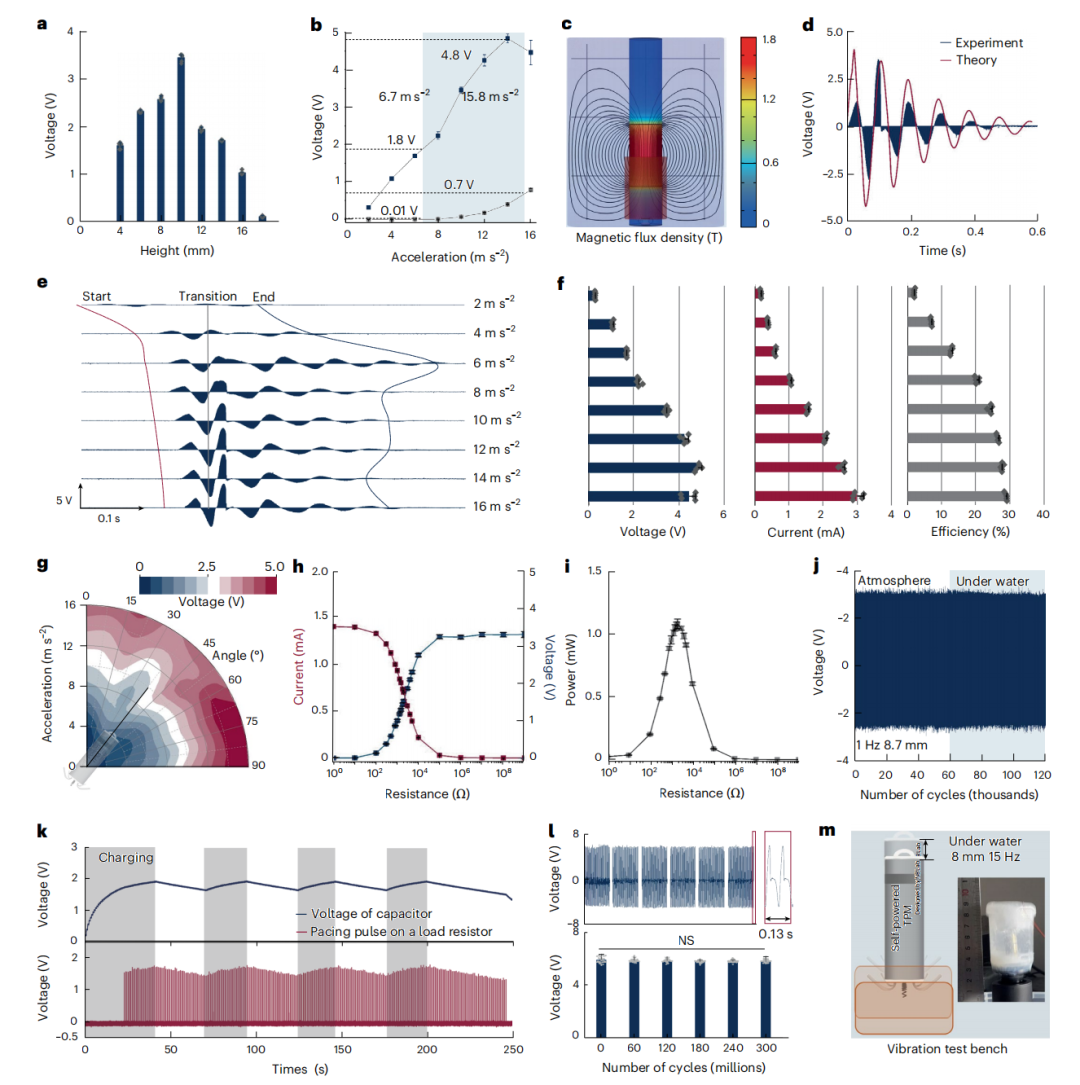
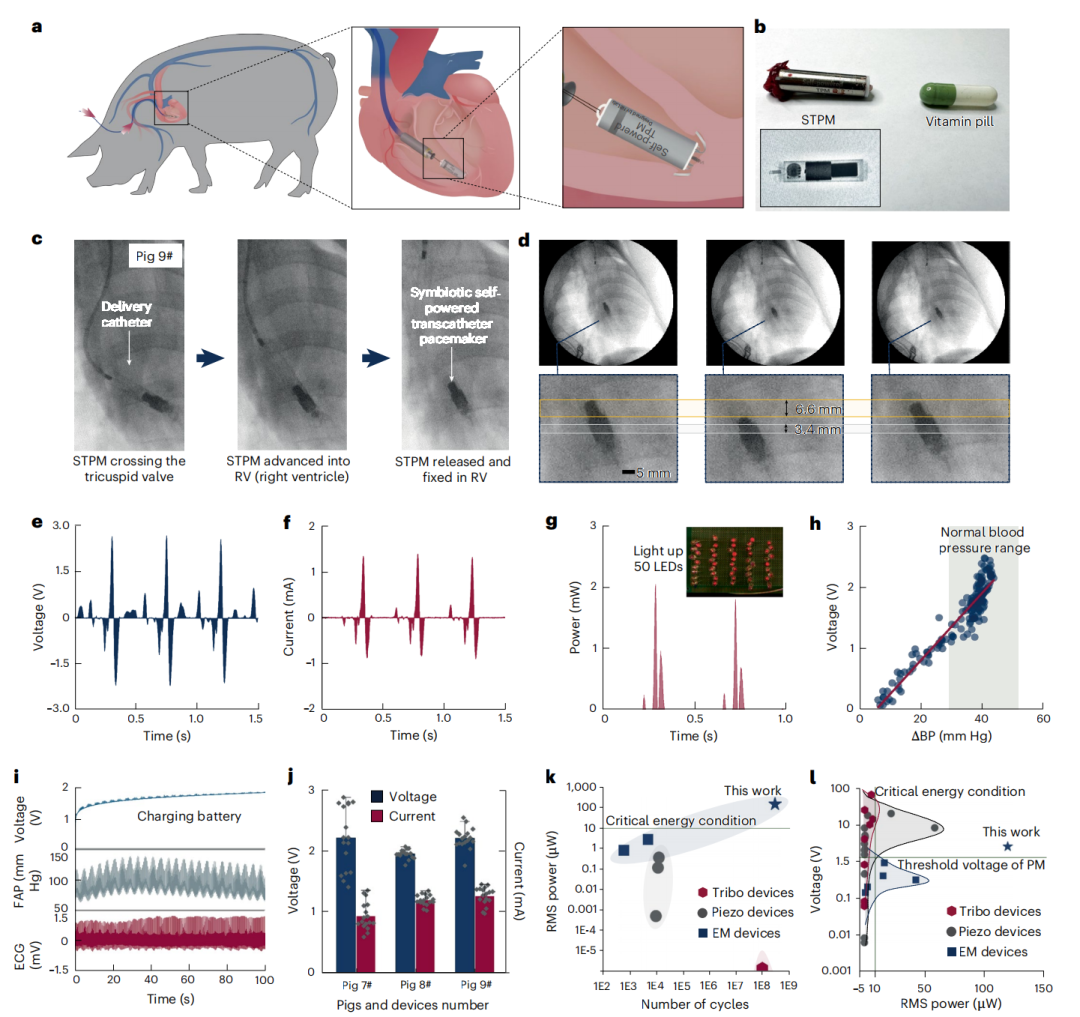
利用直线电机模拟心脏运动参数,STPM 的 ERM 模块表现出了惊人的电力输出。在典型的模拟参数下,开路电压可达 3.5 V,短路电流 1.5 mA,峰值功率达到 1.1 mW(负载 1300Ω)。
更为关键的是,作为植入心脏内部的动态部件,耐用性决定了其能否真正实现“终身”。研究团队将 ERM 置于磷酸盐缓冲液(PBS)中,在 15 Hz、8 mm 振幅下进行了长达 3 亿次的加速疲劳测试(相当于在 60 bpm 心率下运行 10 年)。测试结果显示,输出电压在测试前后未见显著衰减,磁悬浮结构的非接触特性有效地避免了磁体和线圈外壳的物理损耗。
实验室的受控环境无法完全模拟心脏内部复杂的流体动力学、变频的心率以及不规则的解剖结构。STPM 的体内验证(In Vivo)是本研究最具说服力的部分。
研究人员在 11 头约克夏猪(70-90 kg)中进行了植入实验。结果发现,STPM 的输出电压与收缩期/舒张期的血压差(Blood Pressure Difference)呈现出高度的线性相关性。这意味着随着心脏收缩力的增强,能量再生的功率也会随之提升。
这一 RMS 功率(120㎼)是一个极具震撼力的指标。此前,基于摩擦纳米发电机(TENG)或压电材料(PENG)的自供电起搏器研究,其 RMS 功率通常在 1 – 50㎼之间摆动,且往往需要复杂的机械杠杆或较大的受力面积。STPM 仅靠电磁感应就在微型封装内达到了 120㎼,不仅满足了起搏(Pacing)的基本需求,还为未来的感知(Sensing)、无线通讯,甚至 AI 处理芯片预留了充足的“能量带宽”。
由于人体存在姿态变化(卧位、立位、运动等),重力对磁铁位移的影响曾是自发电机的一大难题。STPM 的磁悬浮结构通过优化底座磁场分布,使得活动磁铁即使在倾斜 0-90 度的全量程范围内,输出电压仍能保持在 2.5 V 至 3.3 V 之间。这确保了起搏器在患者日常生活的各种生理姿态下都能稳定补能。
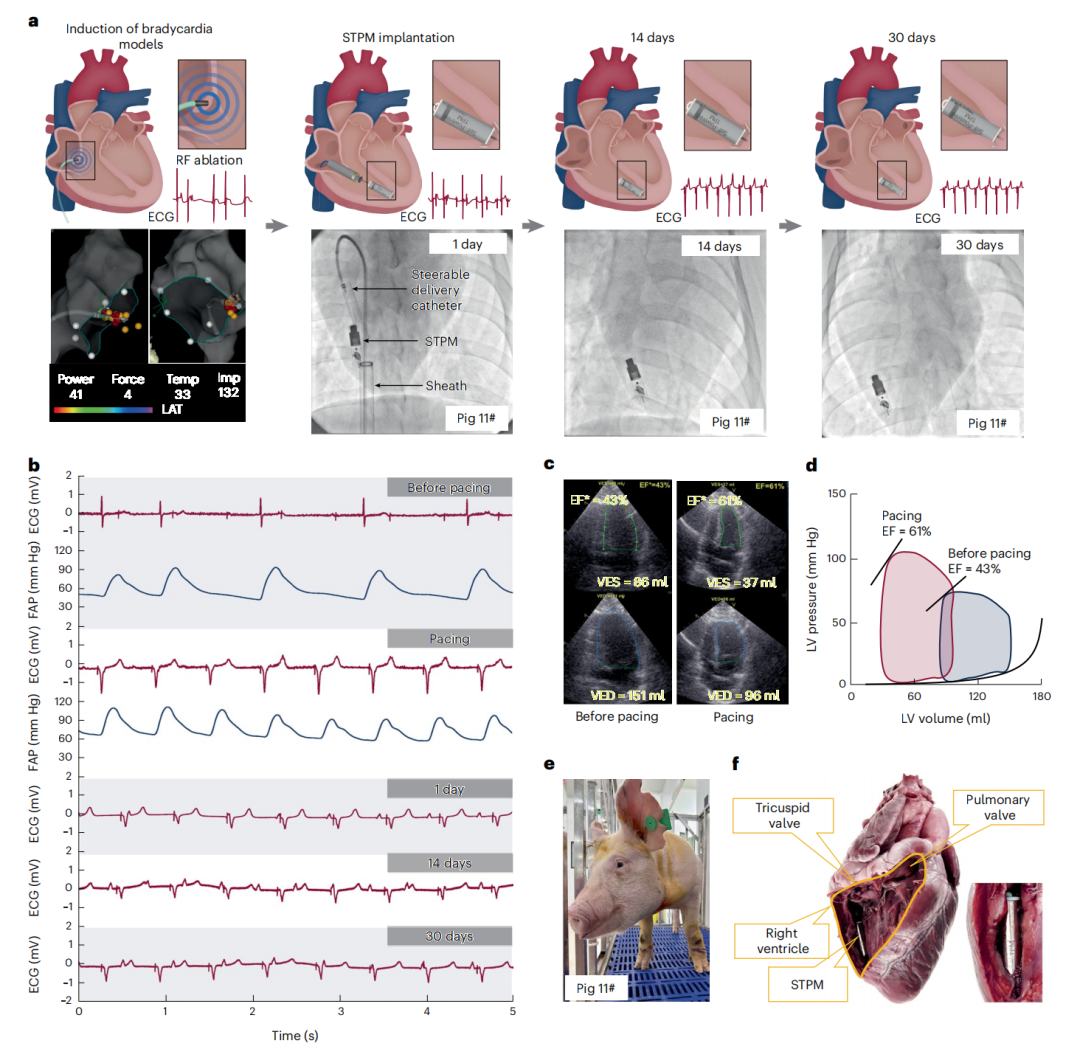
一项技术能否称为“起搏器”,其终极判据在于其治疗功效。研究团队挑战了临床上极其凶险的房室传导阻滞(AV Block)模型。
在猪模型中,研究人员利用放射频率消融(Radiofrequency Ablation)技术精准阻断了房室结房室束电位,制造出三度房室传导阻滞。此时,猪的心率骤降至 47 bpm(且极不规整),血压跌至 85/45 mmHg,左心室射血分数(EF)低于 45%,生命体征处于极其不稳定的状态。
STPM 植入并激活后,系统展现了完美的治疗响应:
1.心律重建:心率迅速提升并稳定在预设的 98 bpm,波形整齐。
2.血流动力学改善:平均动脉压恢复至 110/70 mmHg,射血分数从 43% 跃升至 61%。
3.能量闭环:在起搏过程中,发电机产生的电流持续为内置电池补电,充电峰值与起搏脉冲的放电峰值清晰可辨,实现了真正意义上的“能源共生”。
该研究最令人瞩目的数据来自于长达 30 天的活体随访。数字射线影像显示,起搏器在 1、14、30 天后的位置高度稳定,未出现移位或对心脏解剖结构的损伤。 在随访终点,研究团队进行了详尽的组织学分析。通过苏木精-伊红(H&E)染色切片观察,植入部位的心肌组织未见明显的急性炎症浸润或严重的纤维化剥离。钛合金壳体与 Parylene 涂层表现出了卓越的血液相容性,三尖瓣和肺动脉瓣功能在超声心动图评估下均保持正常。这证明了 STPM 不仅在电学上可行,在生物力学交互上也达到了临床安全性的要求。
要评估 STPM 的商业潜力,必须将其置于全球心脏节律管理(CRM)市场的竞争天平上。目前,这一领域由美敦力、雅培和波士顿科学(Boston Scientific)三巨头垄断。
目前的市场格局聚焦于功能的不断叠加和寿命的缓慢增长:
Medtronic Micra AV2:
侧重于算法优化。通过升级的三轴加速度计,Micra 能够更精准地通过震动感知心房收缩,从而在单一心室器械中实现房室同步(VDD 模式),寿命约为 16 年。
Abbott Aveir DR:
侧重于硬件通信。它是全球首个获得 FDA 批准的双腔无导线系统,通过两台分别位于心房和心室的独立设备进行无线通信(i2i 技术),提供更接近生理的起搏模式,寿命预计可达 20 年。
STPM (Symbiotic TPM):
侧重于能源本质。虽然 STPM 目前处于 porcine 原型阶段,其单腔 VVIR 功能在算法成熟度上尚不及商业产品,但其“终身供能”的物理逻辑具有代差优势。它不再需要通过更庞大的电池或更严格的节电模式来维持寿命,这为未来高度耗能的功能(如连续压力传感、自动除颤、云端实时传输)释放了空间。
除了 STPM 这种硬核电磁发电机,行业内还涌现出其他维度的“共生”尝试:
Ceryx Medical (英国):
该公司的 Cysoni 系统关注“频率的共生”。它并非为了发电,而是通过中央模式发生器(CPG)技术模拟人体自然的呼吸性窦性心律。实验显示,这种生物启发式起搏比恒定频率起搏更能保护受损心脏,显著提高心功能。
EBR Systems (美国):
其 WiSE CRT 系统实现了左心室的无导线起搏,其能量来源于体外植入的超声换能器。这种“能量外传”模式解决了能量问题,但患者仍需植入另一个脉冲发生器。
混合能源采集器 (Hybrid Harvesters):
由王中林院士团队此前推动的 TENG+EMG(电磁)混合发电机。这种设备试图利用 TENG 的高电压和 EMG 的高电流互补,通过风力、水流甚至血管脉搏多点采集能量。STPM 实际上是这种思路在心脏内极致微缩化的产物。
尽管 porcine 研究结果令人振奋,但 STPM 距离人类胸腔仍有若干尚未解决的工程挑战。
STPM 内部的核心是高性能 N52 强磁铁。在临床 MRI 扫描仪(1.5T 或 3.0T)产生的强大静磁场和射频场中,这些磁铁会产生巨大的转矩(Torque)和吸力(Displacement Force),不仅可能导致设备脱落,还会造成严重的图像伪影。
1.行业趋势:目前的商用产品已通过精密磁屏蔽和非铁磁性设计实现了“MRI 条件下安全”。
2.解决路径:未来的 STPM 迭代可能需要采用具有“磁阵列平衡”的设计(如 HALBACH 阵列),或者像近期发表的 FORMA 系统那样,使用 1 毫米直径的微磁球阵列,使其能随磁场自由转动从而抵消转矩。
STPM 的质量(4.2 g)是 Micra(1.75 g)的 2.4 倍。虽然 30 天的猪实验未发现明显的机械性损伤,但心脏是一个每分钟跳动 60-100 次、持续数十年不间断工作的泵。更重的部件附着在薄薄的心肌壁上,长期是否会导致心肌肥厚、局部劳损甚至穿孔,需要更长周期(1-2 年)的大动物安全性评估。
目前的 STPM 原型采用了通用的 MSP430 单片机和标准锂电池,其体积仍略大于成熟商用产品。
1.ASIC 开发:要达到商业级的一致性,必须开发高度集成的专用芯片(ASIC),将能量转换管理、微弱电信号感知和高压起搏驱动集成在一起,以进一步压缩体积。
2.双腔同步:未来的进化版 STPM 需要引入雅培的 i2i 这种跨腔体通讯技术,实现心房和心室能量、信号的双重共生。
STPM 的意义远超一个高性能的起搏器。它向我们展示了一个未来医学的雏形:电子设备开始模仿生物的代谢行为。传统起搏器像是心脏里的一块石头,而 STPM 像是一个寄居者,它吸取心脏的“养分”(机械能),同时反哺“生命信号”(电脉冲)。
这种范式的转变将深刻影响心脏病学的临床实践:
终结“报废堆叠”:
如果一个起搏器可以工作 50 年,那么患者一生只需进行一次介入手术。这不仅节省了巨大的医疗成本,也消除了由于多次重复手术带来的感染风险。
开启“数据起搏”:
有了充足的自生电力,起搏器可以成为一台 24 小时在线的高级心肺监护仪,利用 AI 实时分析心律失常的早期苗头并进行预防性干预。
医疗平权:
虽然初期研发成本高,但长期看,减少昂贵的更换手术和术后并发症处理,将使自供电技术成为低收入国家和老龄化社会的经济选择。
正如王中林院士在多篇综述中所强调的,基于纳米发电机的自驱动系统是物联网(IoT)和植入式医疗的必然趋势。STPM 在猪体内的成功运行,是这一愿景从实验室走向手术室的关键一跃。它告诉我们,心脏不仅是生命的发动机,也是维持生命延续的动力源本身。
在不久的将来,当我们再次谈论起搏器时,我们可能不再关心它的电池还剩几年,而是会感叹人类的工程造物终于像真正的器官一样,获得了在心脏律动中“永生”的能力。
Symbiotic transcatheter pacemaker for lifelong energy regeneration and therapeutic function in porcine disease model | Nature Biomedical Engineering
END
撰文 | 赵亚军
排版 | 周宇茜
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
Science Advances | 中山大学团队最新研究:人工智能赋能的“遗传式非侵入性细胞内记录”用于心脏动作电位的长期监测
点击关注医工学人

本篇文章来源于微信公众号: 医工学人