星标“医工学人”,第一时间获取医工交叉领域新闻动态~

尽管人类诱导多能干细胞(iPS细胞)技术已让“迷你大脑”在培养皿中生长,但如何无损、高精度地“读取”这些三维神经网络的电活动,一直是横亘在科学家面前的巨大鸿沟。来自美国西北大学、清华大学等机构的研究团队,通过逆向工程算法与柔性电子技术,打造出一款能近乎全覆盖类器官表面的三维多孔框架。这项发表在《自然·生物医学工程》上的成果,将240个微电极“编织”成一件与类器官完美贴合的“电子外衣”,首次实现了对神经网络在毫米尺度上的高分辨率空间电生理重建,为药物筛选、神经疾病建模乃至“类脑智能”研究提供了前所未有的工具。

2013年,当首个大脑类器官诞生时,科学界为之沸腾。这些由人类诱导多能干细胞(iPS细胞)分化而来的三维神经组织,不仅复现了大脑的细胞多样性,更具备了自发的神经电活动。它们被视为研究自闭症、阿尔茨海默病乃至意识起源的“上帝视角”。
然而,一个巨大的悖论随之而来:我们制造出了复杂的三维“大脑”,却没有能完美读取它的工具。
传统的研究手段主要有两条路,但都存在致命的“盲点”:
二维多电极阵列(MEA):就像强迫一个立体西瓜去贴在一张平板上。类器官是三维的,而MEA是平面的,只能记录到底部接触的那一小部分细胞,绝大部分神经网络的电活动都淹没在黑暗中。
膜片钳技术:虽然能记录单细胞精度,但它好比用一根针去戳,一次只能获取几个细胞的信息,面对类器官中成千上万相互连接的神经元,无异于管中窥豹。
近年来,虽有科学家尝试用可拉伸的网状电子或自折叠结构来包裹类器官,但其覆盖面积和电极密度仍严重受限。正如论文中所指出的,这些方法只能触及整个神经元群体中“相对较小的一部分”。这好比我们想听懂一场交响乐,却只能把麦克风放在音乐厅的某一个角落,永远无法领略全貌。
核心痛点:神经类器官的研究急需一套能实现高覆盖率、高分辨率、三维无损的电生理接口技术,来捕获真正的“网络级”神经活动。
这项研究的突破性在于,它并非简单地将电子元件贴在类器官表面,而是通过一套精密的“逆向设计”与“自组装”流程,让电极阵列主动去适应、包裹、甚至塑造类器官的形态。
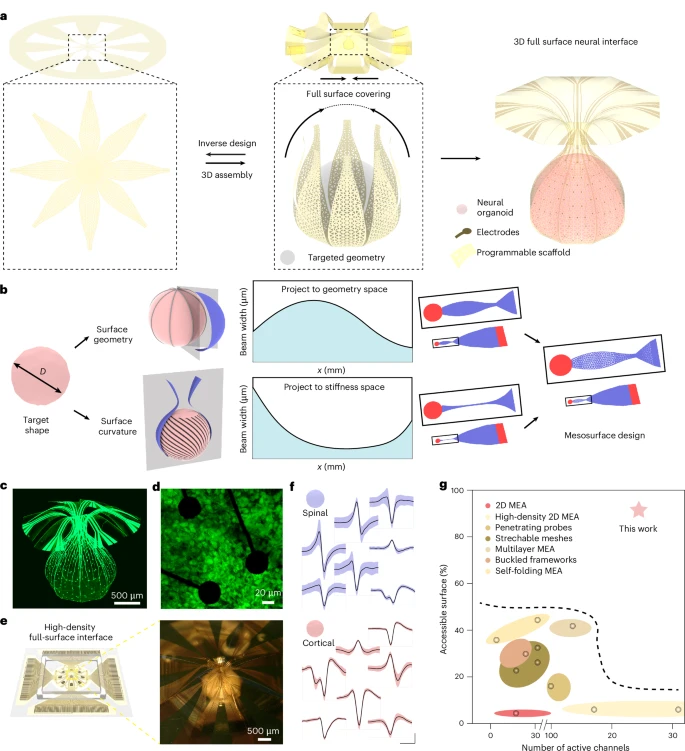
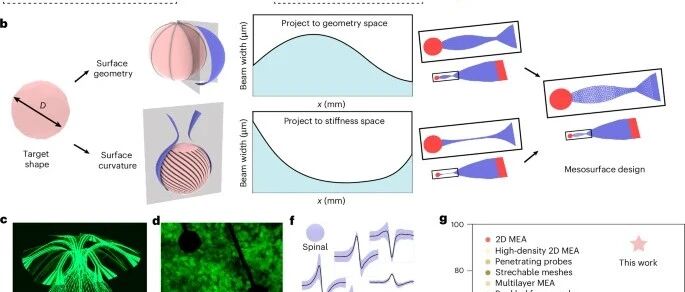
图 1: 具有近乎全表面覆盖的 3D 形状共形神经接口。
a,代表性系统的示意图。在逆向计算建模的引导下,对具有微格点几何结构的二维前体施加工程化机械屈曲方法,可形成所需的三维形状。微格点提供大面积以支持高密度微电极阵列,同时具有足够的孔隙率,允许自然代谢过程所需的扩散传输。
b,同时实现目标表面几何形状和与类器官匹配的 3D 曲率的设计策略示意图。
c,一个接口的微型计算机断层扫描图像,该接口在类器官的球形表面上提供 91% 的覆盖率,并带有 240 个用于测量和/或仿真的独立可寻址电极。
d,微电极阵列与类器官中细胞相互作用的荧光图像,该类器官被插入并在 3D 微格点框架内生长。
e,在此框架内培养的类器官的示意图和图像(插图),带有用于神经记录和刺激的外部连接电路。
f,来自人类脊髓类器官和人类皮层类器官的神经尖峰波形集合。数据表示为每个聚类内所有尖峰的平均值 ± 标准差。比例尺,1 毫秒(水平)和 20 微伏(垂直)。
g,本工作中的 3D 神经接口与其他类器官接口技术的比较,绘制为表面覆盖率和电极数量的函数。数据点根据参考文献估算。
其核心技术逻辑可以拆解为三个环环相扣的步骤:
1. 逆向设计:先有“3D目标”,再算“2D图纸”
研究者们首先通过显微镜确定类器官的三维几何形状。然后,利用基于欧拉-伯努利梁理论的自适应遗传算法进行逆向建模。换句话说,他们要计算出一张平面的、带有特定镂空图案的“剪纸”,在后续受到特定应力时,能恰好弯曲成与目标类器官完美贴合的笼状结构。
2. 微格点设计:给柔性骨架“编程”
为了让平面材料能弯曲成预设的复杂曲面,团队引入了微格点设计。通过在柔性高分子材料(如聚酰亚胺)上刻蚀出大小、密度可变的三角形微孔,实现了对材料局部刚度的精确控制。
– 孔隙率高的区域更软,容易弯折;
– 孔隙率低的区域更硬,保持形状。
这种设计不仅让力学形变可控,还创造了天然的“透窗”,确保了营养物质和氧气的自由扩散,避免影响类器官的健康。
3. 机械引导自组装:从2D到3D的“一跃”
制备好的二维前体结构被暂时粘附在预拉伸的柔性基底上。当基底缓慢释放张力时,平面结构在压缩力的作用下,按照预设的刚度分布,精准地屈曲、弹出,最终自组装成一个与类器官形状一致的三维多孔框架。
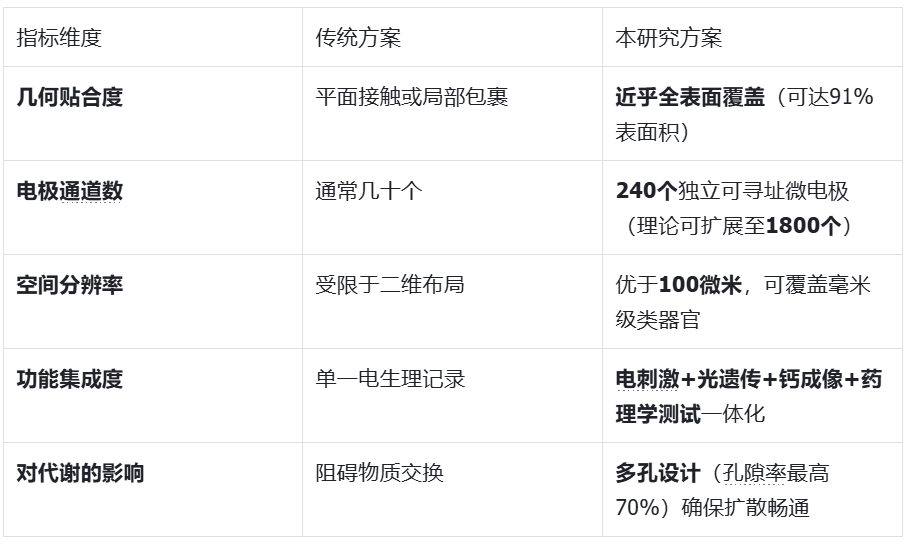
【新旧技术对比】
为了验证这套名为“形状共形多孔框架”的系统的有效性,研究团队在人类皮层和脊髓类器官上开展了一系列堪称完美的实验。
1. 全覆盖记录:240个通道的“交响乐”
当类器官在框架内生长至第87天时,研究人员通过240个通道同时记录了其电活动。数据显示,该系统成功捕捉到了高度同步、周期性强弱交替的神经振荡节律。这与发育中的人脑编码活动模式极为相似,而在以往的二维记录中,这种全局性的网络模式几乎无法被完整捕获。
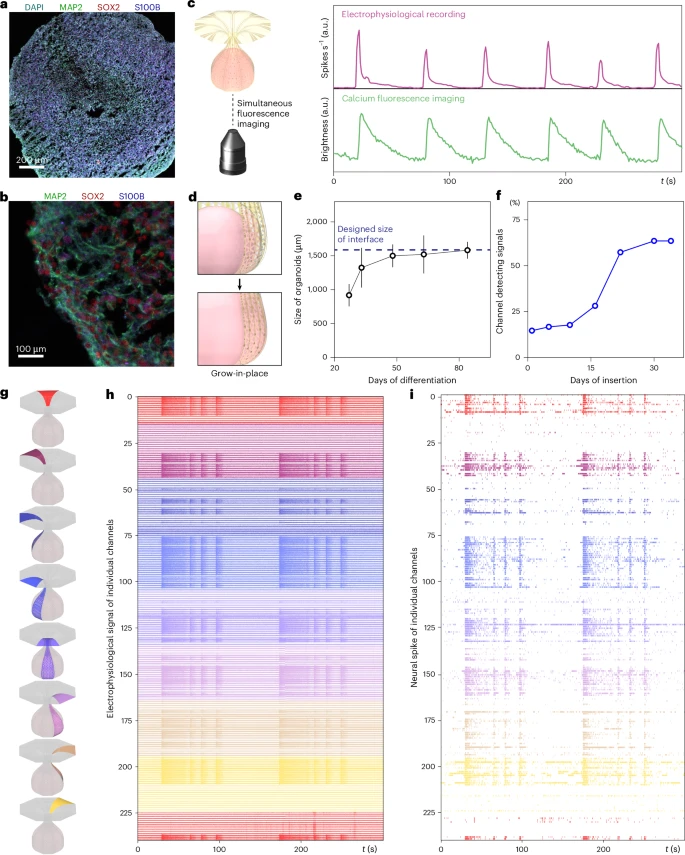
图 2: 神经类器官的集成与高密度记录。
a,分化第 60 天的人类皮层类器官的免疫染色揭示均匀的细胞分布。
b,组织的放大图像,由神经元、星形胶质细胞和神经祖细胞组成。
c,通过电生理学和钙荧光同步记录检测到的人类皮层类器官的神经活动。a.u.,任意单位。
d,”原位生长”策略的示意图,确保神经接口与类器官之间紧密、温和的接触。
e,监测人类皮层类器官的生长曲线,以确定 3D 神经接口的目标尺寸。数据表示为六个不同人类皮层类器官的平均值 ± 标准差。
f,通过”原位生长”过程各个阶段的电生理记录揭示活性通道数量的增加。
g-i,使用具有 240 个独立通道的接口对人类皮层类器官进行的高密度神经记录。
g,接口八个组成梁的示意图,每个梁标有特定颜色。
h,在 240 个电极位点测量的神经电位。
i,记录到的神经活动的光栅图揭示了复杂的振荡节律。
2. 三维重建:让神经信号“立体化”
论文中最具视觉冲击力的部分,是将每个电极记录的信号映射回其三维空间坐标,重构出类器官表面的神经活动图谱(图3d-f)。结果显示,神经活动的强度与发放频率在空间上存在高度相关性,且信号在类器官内的传播具有明确的时序性。例如,下半球先激活,上半球延迟约100毫秒后响应——这首次让我们看到了信息在一个“迷你大脑”中的三维传播路径。
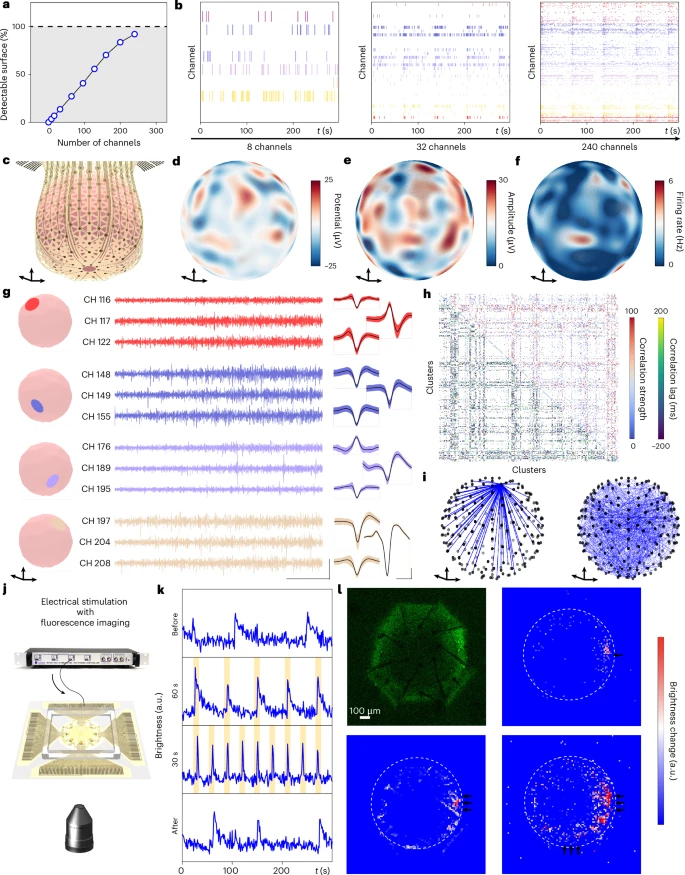
图 3: 3D 空间电生理学。
a,通过假设 100 微米的检测距离,在 91% 的面积覆盖率下,对接口可检测部分作为电极数量函数的建模。
b,基于阵列中 8 个、32 个和 240 个电极子集的数据测量到的人类皮层类器官神经活动,以说明捕捉有意义的网络级神经过程所需的数量。
c,用于神经电生理学 3D 重建的 240 个微电极空间位置示意图。
d,特定时刻人类皮层类器官表面电生理电位的表面分布图。
e,神经尖峰平均幅度的表面分布图。
f,平均发放率的表面分布图。
g,与人类皮层类器官相关的一个同步波内四个不同位置的记录和相应的特征性神经尖峰波形。波形数据表示为每个聚类内所有尖峰的平均值 ± 标准差。电位图的比例尺为 50 毫秒(水平)和 50 微伏(垂直),波形图的比例尺为 1 毫秒(水平)和 20 微伏(垂直)。
h,人类皮层类器官 389 个记录到的神经单元之间的相关性分析。
i,一个示例神经单元的相关单元的 3D 连接图(左),以及与 h 中相同人类皮层类器官所有通道之间的强相关性(右)。
j,电刺激和同步钙荧光成像的示意图。
k,荧光图像的亮度分析揭示了人类皮层类器官在无刺激、60 秒间隔刺激、30 秒间隔刺激和刺激后的神经活动。
l,基线荧光成像以及从单个微电极、一个梁的所有微电极和两个梁的所有微电极传递刺激时的亮度差异图。实验在三个独立的人类皮层类器官中重复进行,结果相似。a.u.,任意单位。
3. 精准调控:局部光遗传与电刺激
借助框架的透明基底和精确的电极定位,研究团队实现了对特定区域的局部光遗传学刺激。蒙特卡洛模拟显示,激光可以精准地只照射到4个电极覆盖的区域,而邻近的电极则记录到未受干扰的自发活动。这证明了该系统在神经回路调控研究中的巨大潜力。
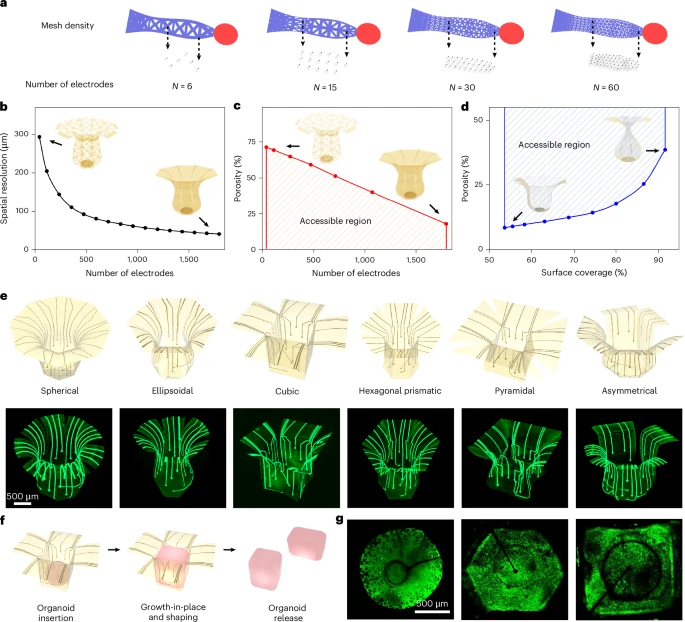
图 4: 3D 结构设计的多样性与具有工程化 3D 形状的类器官生长。
a,计算引导的微格点布局优化过程的示意图,旨在最大化微电极密度,同时保持所需的 2D 几何形状和刚度分布。
b–d,空间分辨率作为电极数量函数的实际可达到水平 (b),孔隙率作为电极数量函数的实际可达到水平 (c),以及孔隙率作为表面覆盖率函数的实际可达到水平 (d)。
e,3D 接口的多样化几何形状及相应的微型计算机断层扫描图像。
f,”原位生长”过程的示意图,以实现由这些 3D 接口定义形状的类器官。
g,具有球形、六边形棱柱形和立方体形状的神经类器官的荧光图像。
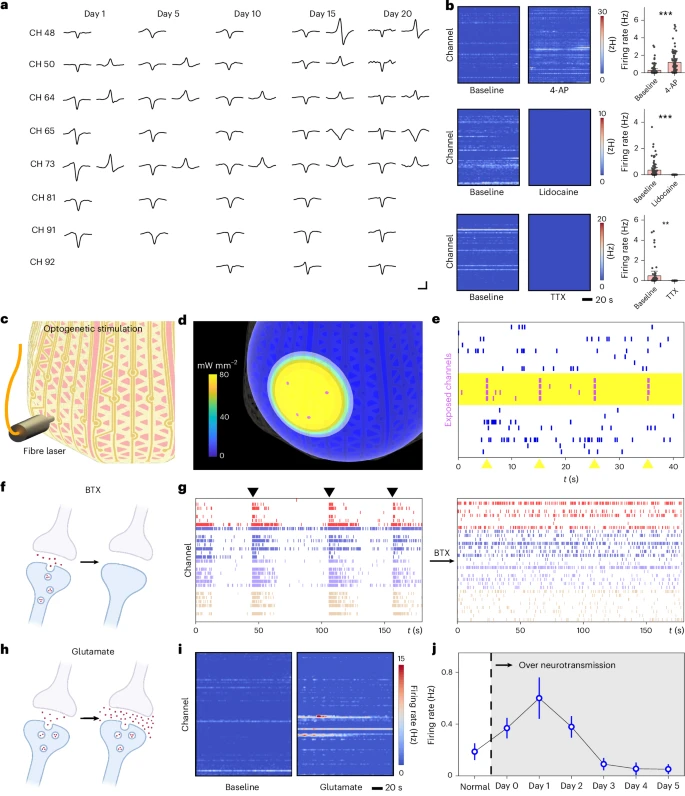
图 5: 在类器官研究各领域的应用展示。
a,神经类器官的纵向监测显示,在类器官插入后的数天内,能够稳定追踪单个神经单元。比例尺,1 毫秒(水平)和 20 微伏(垂直)。
b,从集成的 3D 接口的 ( n = 96 ) 个独立通道记录的神经类器官对暴露于 4-氨基吡啶、利多卡因和河豚毒素的反应,以发放率热图形式呈现,突出显示这些药物应用前后活性的变化。
c,使用位置可调谐光纤激光器进行局部光遗传学刺激的示意图。
d,四个微电极局部光照强度分布的蒙特卡洛模拟。
e,被照射的微电极和几个未照射的相邻微电极响应的光栅图,显示仅在照射电极中存在相位锁定响应。
f,通过暴露于肉毒毒素消除神经递质效果的示意图。
g,代表性通道在暴露于肉毒毒素之前和之后响应的光栅图,与振荡性同步神经活动的消除一致。
h,由于暴露于谷氨酸而增强神经传递的示意图。
i,集成类器官在给予谷氨酸之前和之后发放率的热图,显示出极端的神经元兴奋效应。
j,从集成的 3D 接口对 ( n = 96 ) 个独立通道进行的纵向监测显示,暴露于谷氨酸后 5 天内平均发放率先增加后减少。数据在 b 和 j 中以平均值 ± 平均标准误表示。
这项技术的诞生,其意义远不止于一种新的测量工具。它正在将神经类器官研究从“盲人摸象”的时代,带入“高清三维电影”的时代。
– 重塑药物筛选流程:制药公司可以利用患者iPS细胞来源的类器官,集成该电极框架,高通量地筛选候选化合物,并实时、精准地观察药物对神经网络电活动的干预效果,极大提升药物研发的效率和临床转化率。
– 加速神经疾病模型构建:研究中通过谷氨酸构建的“兴奋性毒性”模型,以及肉毒毒素(BTX)对神经递质释放的抑制实验,首次实现了对疾病表型发生、发展全过程的纵向、高精度电生理追踪。这对于研究癫痫、渐冻症等疾病的动态演变机制至关重要。
– 迈向“类器官智能”:去年“类器官智能”的概念引起热议,其核心在于利用类器官的生物计算能力。而本研究展示的空间选择性电刺激与高密度记录,正是实现类器官与外部电子设备双向信息交互的基石。这种技术有望将类器官真正打造为一种低功耗、可学习的生物计算单元。
尽管这项研究令人振奋,但作为一名科技观察者,我们仍需保持冷静,看到它从实验室走向产业化所面临的挑战:
1. 制造工艺的复杂性:虽然原理已被证明,但将柔性电子、微加工、逆向算法和生物培养如此精密地耦合在一起,其良品率和规模化生产能力仍是未知数。目前论文展示的240通道设计,对微加工精度要求极高,未来能否以低成本量产?
2. 长期生物相容性:论文中进行了长达90天的稳定性测试,但类器官的培养周期往往是数月甚至更长。聚酰亚胺等材料在超长期培养中对细胞微环境是否会产生未知的化学或力学影响,仍需更深入的表征。
3. 数据量的“甜蜜负担”:240个通道的实时高采样率数据,对信号处理算法提出了极高要求。虽然作者开发了伪迹去除算法,但从海量数据中提取有意义的生物学结论,仍是一个巨大的计算挑战。
4. 伦理的隐线:当我们的读取和干预技术越来越精密,当我们能清晰看到“迷你大脑”中信号如何传播,甚至能通过电刺激改变其活动模式时,围绕类器官的伦理边界问题——尤其是关于其“感知”和“意识”的讨论,将变得更加紧迫和复杂。
结语
约翰·罗杰斯(John A. Rogers)团队的这项研究,为神经科学界递上了一把开启三维世界的钥匙。它不仅仅是技术指标的堆砌,更是观察视角的根本性转变。当我们可以从三维空间去审视、去解读一个“大脑”时,我们对神经发育、疾病机制乃至智能本质的理解,或许才刚刚开始。
Liu, N., Shiravi, S., Jin, T. et al. Shape-conformal porous frameworks for full coverage of neural organoids and high-resolution electrophysiology. Nat. Biomed. Eng (2026). https://doi.org/10.1038/s41551-026-01620-y
END
撰文 | 郝娅婷
编辑 | 余帆
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,参与线上线下交流活动

推荐阅读
点击关注医工学人

本篇文章来源于微信公众号: 医工学人