星标“医工学人”,第一时间获取医工交叉领域新闻动态~

糖尿病前期,即胰岛素抵抗,因检测手段复杂昂贵而常被忽视。如今,谷歌研究院与剑桥大学联合发布了一项《自然》研究,首次利用基于4000万小时传感器数据训练的“可穿戴基础模型”,结合常规血检,仅通过智能手表即可精准识别胰岛素抵抗。该研究不仅将筛查门槛降低至消费品级别,更通过AI大模型将预测结果转化为个性化健康建议,为2型糖尿病的早期干预开辟了一条前所未有的规模化路径。
全球有近5.37亿成年人患有糖尿病,其中90%为2型糖尿病。而在其背后,潜伏着一个更庞大的“预备役”群体——胰岛素抵抗。它是一种细胞对胰岛素反应迟钝的状态,是通往2型糖尿病的关键一步。
然而,如何精准、普适地发现胰岛素抵抗,却是一个困扰医学界多年的难题。当前的金标准“高胰岛素-正葡萄糖钳夹技术”虽精准,但操作复杂、侵入性强,仅限科研场景。临床常用的替代方案“稳态模型评估胰岛素抵抗指数”虽然相对便捷,但仍需空腹抽血检测胰岛素,成本不菲且无法居家完成。最新的“动态血糖监测”方法虽能居家,但需要佩戴专用传感器,尚未普及。
问题的核心在于:胰岛素抵抗的诊断,要么过于复杂昂贵,要么依赖不便的临床检测,导致绝大多数潜在风险人群被漏诊,错过了生活方式干预的最佳窗口期。
这项研究提供的,正是一把打开困局的钥匙。它的核心并非发明新传感器,而是利用现有设备,构建了一套前所未有的数据处理和分析范式。其创新可以拆解为两个层次:
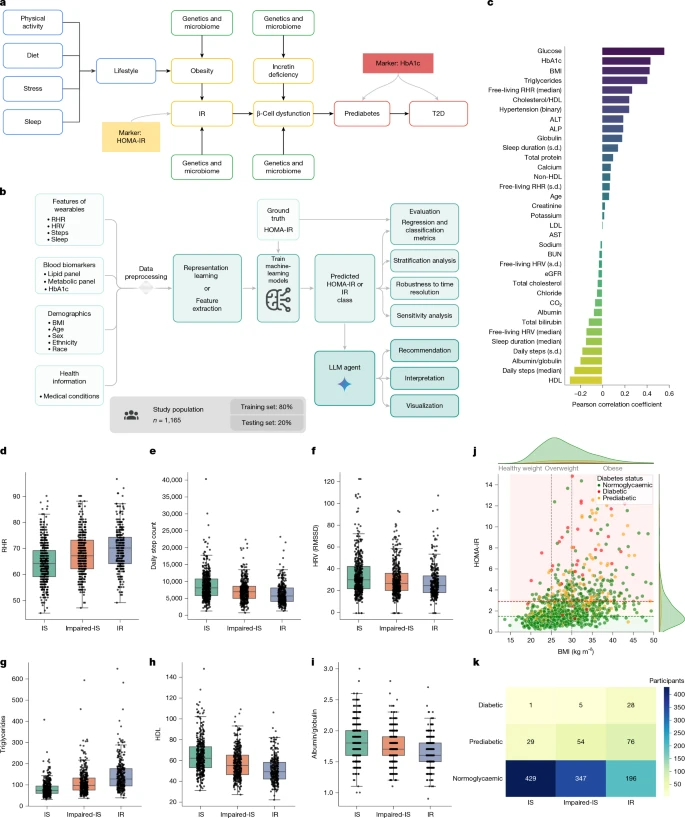
图 1 | 研究设计与数据总结
a, 导致胰岛素抵抗、糖尿病前期和糖尿病的生理因素及相关生活方式因素概述。
b, 我们提出的用于预测HOMA-IR并使用胰岛素抵抗素养与理解代理(IR agent)对结果进行解读的建模流程。
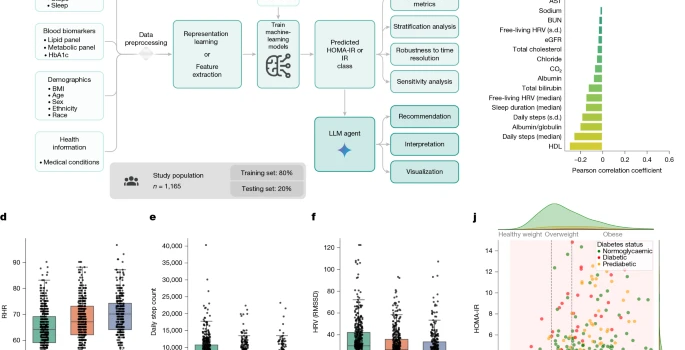
c, 血液生物标志物和生活方式特征(连续值)与HOMA-IR的相关性。
d–f, 在分层胰岛素敏感性组别(胰岛素敏感组、胰岛素敏感性受损组、胰岛素抵抗组)中,与HOMA-IR高度相关的三个主要可穿戴设备特征(静息心率 (d)、每日步数 (e) 和心率变异性 (f))的分布情况。RMSSD,连续差值的均方根。
g–i, 在分层胰岛素敏感性组别中,与HOMA-IR高度相关的三个主要血液生物标志物(甘油三酯 (g)、高密度脂蛋白胆固醇 (h) 和白蛋白/球蛋白比值 (i))的分布情况。在d–i的箱线图中,中心线表示中位数,箱体边界表示第25和第75百分位数,须线延伸至四分位距的1.5倍。
j, 体重指数与HOMA-IR值的散点图,显示了较高的体重指数值与胰岛素抵抗(通过HOMA-IR测量)之间的关系。
k, 混淆矩阵,显示了处于不同胰岛素抵抗状态与糖尿病状态组合下的参与者人数。
1)数据层:从“碎片化记录”到“生理画像”
以往利用可穿戴设备预测健康的研究,大多止步于对步数、静息心率等简单聚合指标的分析,丢失了大量时间维度上的动态信息。本研究则引入了可穿戴基础模型,该模型在4000万小时的匿名传感器数据(包括心率、加速度、皮肤温度等26种信号)上进行了预训练。它就像一个“生理学大师”,学会了解读人体在一天1440分钟内,各种生理信号的复杂模式、缺失规律和微妙变化。
2)模型层:从“经验关联”到“深度融合”
研究者将基础模型学到的精细“生理画像”,与人口统计学信息以及最常规的血液检测指标(如空腹血糖、血脂)结合,输入到一个多模态深度神经网络中。最终,这个模型能直接输出一个连续值——预测的HOMA-IR指数,并据此判断个体是否存在胰岛素抵抗。
|
技术路径 |
传统/现有方法 |
本研究方法 (WFM+多模态融合) |
|
数据来源 |
单一来源(如血糖、胰岛素、问卷) |
多模态融合(可穿戴设备 + 常规血检 + 人口统计) |
|
穿戴数据处理 |
简单聚合(平均步数、平均心率) |
基础模型学习高维时序信号,捕捉动态生理模式 |
|
核心技术 |
统计学、传统机器学习 |
深度神经网络 + 掩码自编码器 + 大语言模型 |
|
预测目标 |
间接指标或定性评估 |
直接预测HOMA-IR连续值,并进行分类 |
|
可解释性 |
依赖专家解读 |
集成大语言模型,生成个性化建议和可读性报告 |
研究团队通过两个独立队列验证了该方法的有效性。
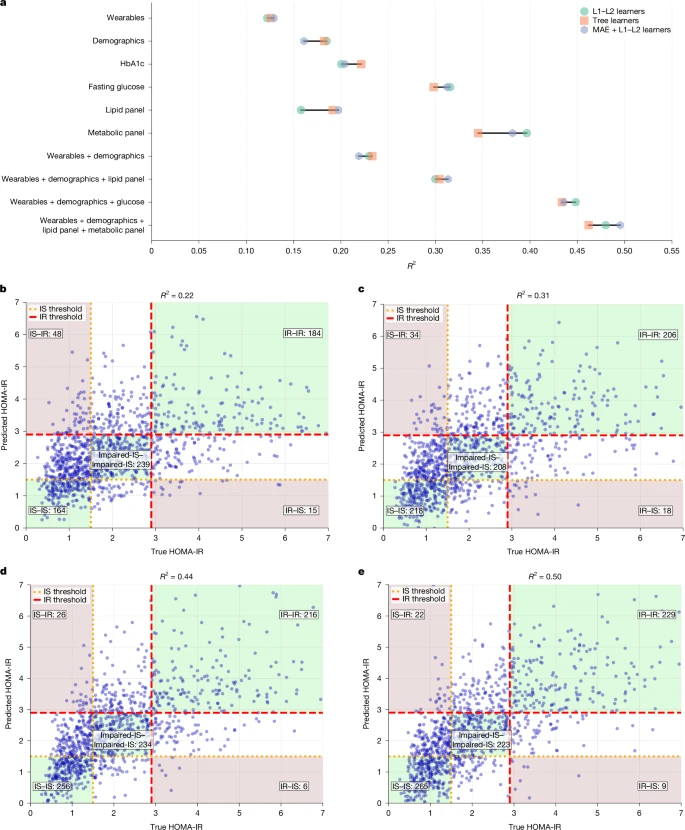
图 2 | HOMA-IR预测性能评估(回归)
a, 不同输入特征集与模型下HOMA-IR回归效果的比较。
b–e, 针对选定特征集,预测HOMA-IR值与真实HOMA-IR值的散点图:可穿戴设备与人口统计学特征 (b);可穿戴设备、人口统计学特征与血脂组 (c);可穿戴设备、人口统计学特征与空腹血糖 (d);可穿戴设备、人口统计学特征、血脂组与代谢组 (e)。真阳性与假阴性相关的重点关注区域分别以浅绿色和浅棕色高亮显示。
开发队列 (WEAR-ME 研究):涵盖1165名美国参与者。结果显示,仅用可穿戴设备数据和人口统计学信息,模型识别胰岛素抵抗的受试者工作特征曲线下面积即可达到0.70。而加入空腹血糖后,性能显著提升至0.78;当进一步加入血脂等常规血检指标后,模型性能达到最优,AUROC为0.80,灵敏度76%,特异度84%。
独立验证队列:在对72名全新参与者的验证中,模型展现了强大的泛化能力。使用可穿戴基础模型特征与常规血检的模型组合,AUROC高达0.88,而剔除可穿戴数据后,同一模型的AUROC降至0.76。这有力地证明了,穿戴设备提供的精细生理动态信息,是传统方法无法替代的关键拼图。
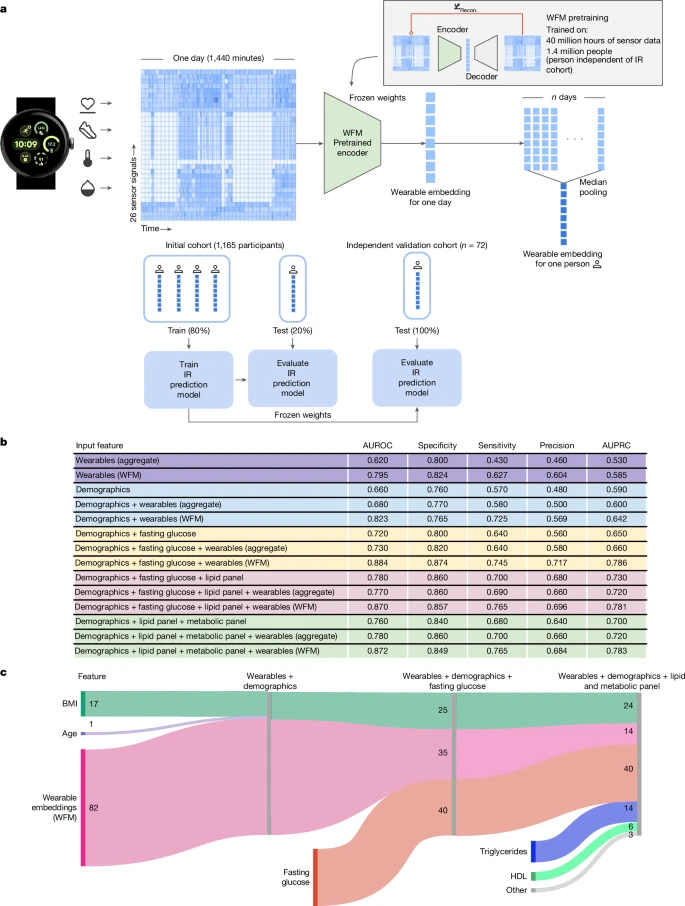
图 3 | 利用可穿戴基础模型改进可穿戴设备数据在胰岛素抵抗预测中的应用
a, 可穿戴基础模型预训练与推理组件的示意图。L Recon.,重建损失。
b, 量化可穿戴基础模型在改善胰岛素抵抗预测中增值作用的性能指标。AUPRC,精确率-召回率曲线下面积。
c, SHAP分析,量化可穿戴基础模型生成的可穿戴设备嵌入在不同实验设置下对预测性能的相对贡献。
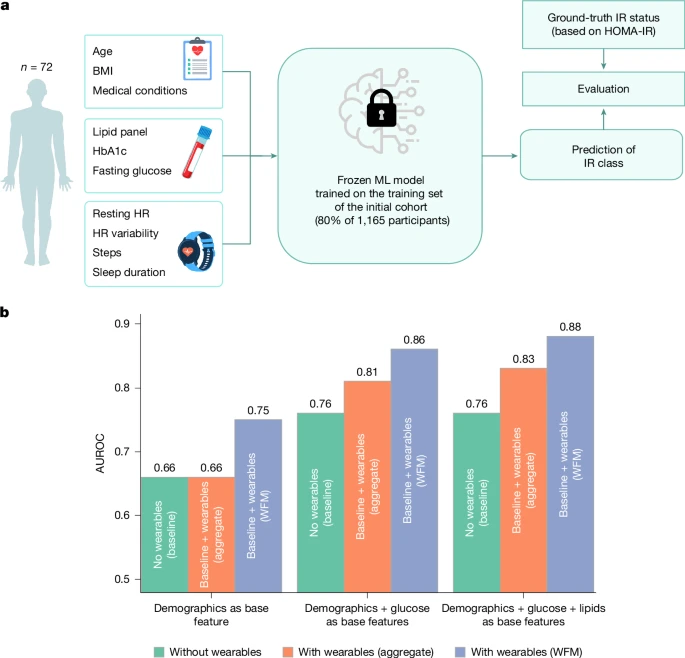
图 4 | 独立验证队列上的模型性能
a, 独立验证队列的研究概述。
b, 基于不同实验设置(不使用可穿戴设备、使用可穿戴设备(聚合指标模式)以及使用可穿戴设备(结合可穿戴基础模型模式)),胰岛素抵抗分类在独立验证队列上的性能表现。我们在此队列上验证了所有已训练的模型,但包含全面代谢组的模型除外,因为该独立验证队列的血液检测中未包含全面代谢组。
更令人兴奋的是,研究团队将这套预测系统与一个基于Gemini 2.0 Flash构建的“胰岛素抵抗知识代理”相集成。该代理不仅能输出风险结果,还能结合用户的个人数据,提供个性化的风险解读和生活方式建议。在由5位执业内分泌学家参与的盲评中,该代理在全面性(80%偏好)、可信度(92%偏好)和个性化(73.3%偏好)上,均显著优于未集成预测模型的基础大语言模型。
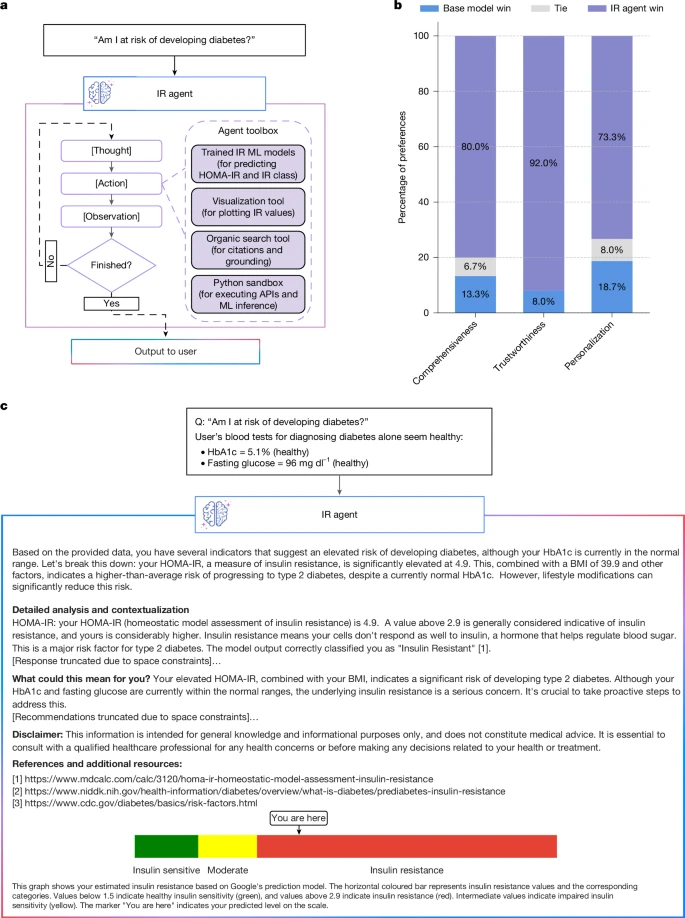
图 5 | 胰岛素抵抗代理概述
a, 所提出的胰岛素抵抗代理示意图。API,应用程序编程接口;ML,机器学习。
b, 在并排对比评估中,内分泌学家评定的胰岛素抵抗代理相较于基础模型的胜率。
c, 一个代谢相关问题的示例,附有真实研究参与者的数据,以及胰岛素抵抗代理对应的输出结果。
这项研究的颠覆性在于,它第一次证明,通过日常佩戴的消费级设备,结合每年体检都会做的常规血检,就能以接近临床级的准确率,筛查出2型糖尿病的关键风险。
对个人:它将健康监测从“体检时刻”延伸至“每时每刻”。你的手表不再只是记录步数,而是能成为你代谢健康的“侦察兵”,在你糖化血红蛋白还未升高时,就发出胰岛素抵抗的预警,为你留出充足的逆转窗口。
对医疗体系:这是一次巨大的效率革命。与其让所有有风险的人去做昂贵、复杂的钳夹或胰岛素检测,不如先用这套模型进行低成本、大规模的筛查。筛查出的高风险人群,再通过临床检测进行确诊和干预,从而极大地优化医疗资源配置。
对产业:该研究为“可穿戴设备+AI”在严肃医疗领域的应用开辟了新的蓝海。它预示着,未来智能手表、手环的价值将超越健康管理,向疾病早筛、风险预测等更具临床意义的方向演进。对于药企、保险公司和数字疗法公司而言,这无疑是一个全新的数据入口和干预平台。
当然,这项研究并非完美无瑕。作为一项前沿探索,我们仍需保持审慎:
数据偏差:它将健康监测从“体检时刻”延伸至“每时每刻”。你的手表不再只是记录步数,而是能成为你代谢健康的“侦察兵”,在你糖化血红蛋白还未升高时,就发出胰岛素抵抗的预警,为你留出充足的逆转窗口。
商业化门槛:虽然模型输入(年龄、BMI、血检、穿戴数据)看似常见,但“可穿戴基础模型”的构建和训练门槛极高,需要海量数据和强大的算力支持。这决定了该技术短期内可能难以被中小型公司复制,商业化路径或将由大型科技公司主导。
解释性黑箱:尽管引入了大语言模型进行解读,但深度学习模型内部的决策过程依然是复杂的“黑箱”。为什么模型会根据特定一段心率数据判断风险,仍需进一步研究以增强其可解释性,这对于获得临床医生的信任至关重要。
总的来说,这项研究为应对全球性的代谢疾病挑战,提供了一个极具想象力的新范式。它让我们看到,在AI和传感技术的加持下,健康管理的未来,或许就藏在每个人手腕上那方寸之间。
[1]Metwally, A.A., Heydari, A.A., McDuff, D. et al. Insulin resistance prediction from wearables and routine blood biomarkers. Nature (2026).
https://doi.org/10.1038/s41586-026-10179-2
END
编辑 | 郝娅婷
排版 | 张艳青
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
npj flexible electronics | 告别刚性标记与图像伪影:韩国科学技术研究院研究如何让手术机器人在多模态影像中“看清”肿瘤
点击关注医工学人 直播预告

本篇文章来源于微信公众号: 医工学人