星标“医工学人”,第一时间获取医工交叉领域新闻动态~

肝硬化,这个沉默的“杀手”,往往在出现严重并发症时才被发现。如今,科学家们找到了一把新的“钥匙”——利用常规心电图数据训练出的AI模型。在一项覆盖近1.6万名患者的临床研究中,这项技术将肝硬化的初诊率提升了2倍,在高风险人群中更是将检出率提升了4倍以上。这不仅意味着数亿糖尿病、肥胖症患者可能获得一次无痛、低成本的重疾早期筛查机会,更预示着常规医疗数据正在被重新“激活”,成为疾病早期发现的全新战场。

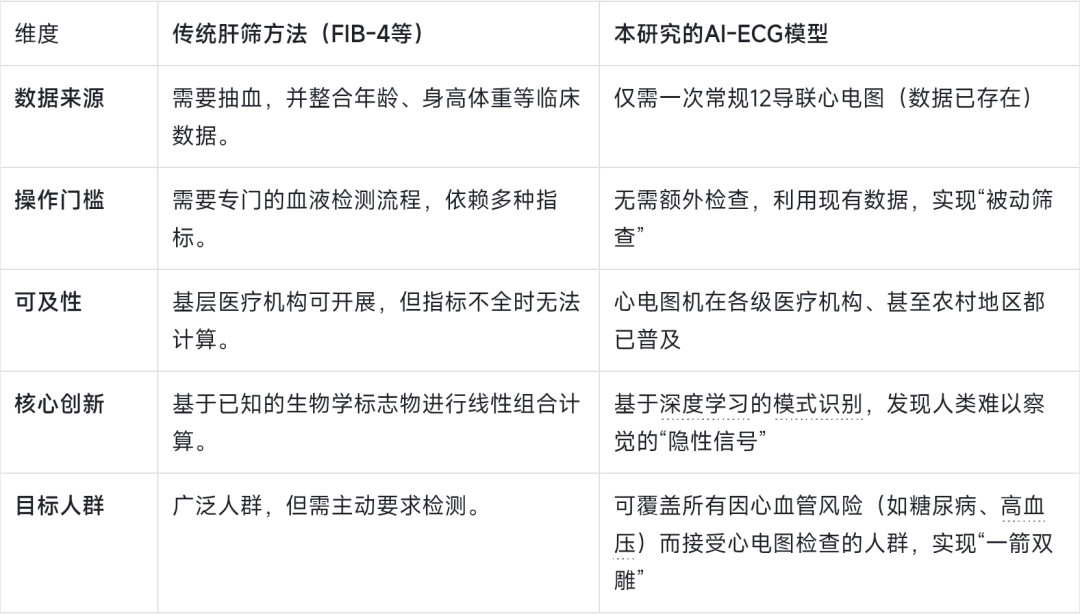
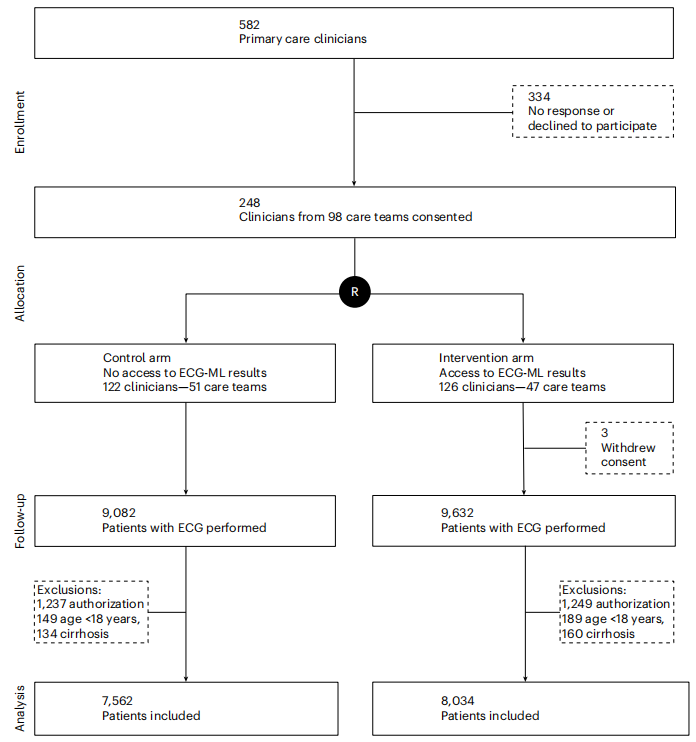
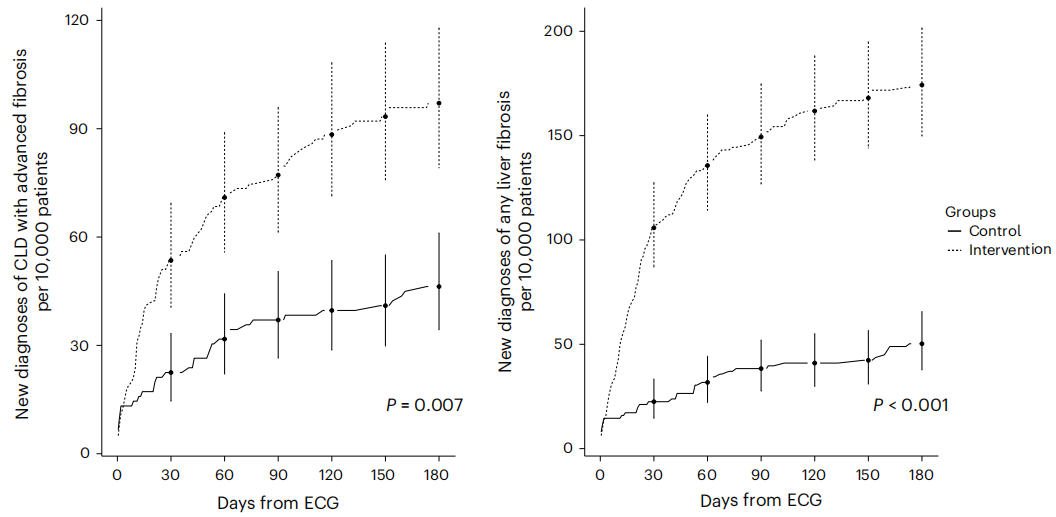
肝脏,人体内最沉默的器官之一。它可以在受损严重的情况下依然维持基本功能,直到出现腹水、消化道出血等致命并发症时,患者才初次就医,而此时往往已错过最佳干预时机。数据显示,全球约有2-5%的人口患有晚期慢性肝病(即肝硬化),但其中很大一部分人对此毫不知情。 肝脏活检:虽是金标准,但存在创伤、出血风险和取样误差,无法作为大规模人群的筛查工具。 影像学检查(如瞬时弹性扫描):设备昂贵,在基层医疗机构和农村地区普及度低。 血液生物标志物组合(如FIB-4指数):虽然相对便捷,但其计算依赖多项指标(如年龄、血小板、转氨酶),且论文数据显示,在实际临床环境中,仅有27%的患者拥有计算FIB-4所需的全部指标,其准确性在低患病率人群中也不尽如人意。 这个困境的核心矛盾在于:我们急需一种可及性极高、成本极低、且能精准锁定高风险人群的“信号弹”,来打破肝病“发现即晚期”的魔咒。 本文研究的核心突破,在于将一种常规、廉价、广泛开展的检查——心电图(ECG),与深度学习技术相结合,实现了对肝脏健康状况的“跨界”感知。 原理并不神秘: 肝硬化不仅仅是肝脏本身的病变,它会引发一系列全身性的生理变化,尤其是在心血管系统。肝硬化会导致心肌收缩力减弱、电活动异常,这些细微的变化在12导联心电图上会留下独特的“印记”。 研究团队利用一个包含77,507人的大型数据库,训练了一个神经网络模型。这个模型学习的目标,不是传统意义上的心律失常或心肌缺血,而是从心电图的波形和时序中,解码出与晚期慢性肝病相关的深层模式特征。 为了验证这个模型在真实临床环境中的有效性,研究团队进行了一项实用性的整群随机对照试验,这在AI医学研究中极具说服力。 图 1 | CONSORT 流程图。 他们纳入了98个基层医疗团队,近1.6万名成年患者。干预组的医生在患者心电图结果为“阳性”(即AI模型提示高肝硬化风险)时会收到提醒,而对照组的医生则看不到这个结果。随后,研究团队跟踪了180天内,两组患者中新确诊晚期肝病的比例。 图 5 | 慢性肝病(CLD)累积诊断随时间的变化。 关键数据: 整体人群:干预组的新确诊率是1.0%,而对照组仅为0.5%。这意味着,仅仅通过一个提醒,就让肝硬化的诊断率提升了2倍(OR 2.09)。 AI阳性人群(高风险人群):效果更为显著。在AI模型标记为高风险的患者中,干预组的新确诊率飙升至4.4%,而对照组仅为1.1%,诊断率提升了近4倍(OR 4.37)。 对任何阶段肝纤维化的检出:同样,干预组检出率(1.7%)远高于对照组(0.5%),尤其是在高风险人群中,检出率从1.1%提升至8.4%,提升了超过7倍(OR 8.03)。 这些数据清晰地表明,AI-ECG模型不仅有效,而且其影响力在高风险人群中呈指数级放大。此外,研究还发现,那些因AI提醒而获得进一步检查并被确诊的患者,其发生肝功能失代偿(肝硬化晚期表现)的比例(8%)远低于未被提醒组的患者(31%),侧面印证了早期发现的临床获益。 这项研究的价值,远超肝病筛查本身。它揭示了一个全新的范式:我们正在从“为特定目的而进行检查”,转向“从已有常规数据中挖掘疾病信号”。 对医疗行业:心电图是糖尿病、高血压等心血管风险人群的常规检查。这意味着,全球数以亿计的“三高”人群,他们的每一次常规心电图检查,都可能在不增加任何成本和负担的情况下,同步完成一次肝病筛查。这极大地提升了基层医疗的“作战能力”。 对商业价值:该模型的算法已被申请专利,并授权给初创公司Anumana。这标志着“AI+常规生物信号”的商业模式正在成型。未来的竞争,将不再仅仅是谁拥有新的影像设备,而是谁能从海量的、未被充分利用的常规医疗数据(心电图、脑电图、甚至生命体征监测数据)中,率先挖掘出高价值的诊断洞察。 对疾病预防:正如论文所言,随着针对肝纤维化的药物(如Resmetirom)获批上市,早期发现不再是“无药可医”的安慰,而是真正开启了逆转病程、降低终末期肝病负担的可能性。AI筛查将成为连接诊断与新型治疗的关键桥梁。 尽管前景光明,作为《麻省理工科技评论》,我们必须以冷静的视角审视这项研究的局限性。 研究显示,尽管AI发出了预警,但仅有约16% 的阳性患者接受了医生推荐的进一步检查。临床判断、患者偏好、行政负担是阻碍落地的三大因素。技术本身无法解决所有问题,如何设计工作流程,让AI建议“无缝”融入医生的决策路径,是商业化落地的第一道坎。 研究队列中,96%的患者为白人。该模型在其他种族和民族(如亚裔、非裔等,这些人群的肝病流行病学特征和心电图模式可能存在差异)中的表现尚属未知。任何模型的普适性都需要在更广泛、更多样化的人群中得到验证。 研究中,许多确诊依赖于无创检查(如FibroTest、弹性成像),而非肝脏活检这一金标准。这虽然符合临床实践伦理,但不可避免地存在一定的假阳性或假阴性风险,可能会影响对AI模型真实效能的评估。 结语: 这项研究是一次精彩的“破壁”尝试,它证明了AI有能力从看似不相关的、海量的常规医疗数据中,解锁新的疾病维度。它并非要取代现有诊断路径,而是为这个路径提供了一个效率更高、覆盖更广的“入口”。未来,我们面临的挑战不再是技术本身,而是如何构建一个能让AI、医生和患者高效协作的生态系统,让这项“心电图上的肝病侦探”真正惠及每一位在沉默中等待发现的病人。
Simonetto, D.A., Rushlow, D., Liu, K. et al. Detection of undiagnosed liver cirrhosis via AI-enabled electrocardiogram: a pragmatic, cluster-randomized clinical trial. Nat Med 32, 160–167 (2026). https://doi.org/10.1038/s41591-025-04058-y END 撰文 | 郝娅婷 排版 | 王可豪 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊, 参与线上线下交流活动
推荐阅读
Nature machine intelligence | 牛津大学开发基于170万个体数据预训练的多模态基础模型,实现跨场景与设备的心脏健康评估

点击关注医工学人 直播预告

本篇文章来源于微信公众号: 医工学人