星标“医工学人”,第一时间获取医工交叉领域新闻动态~

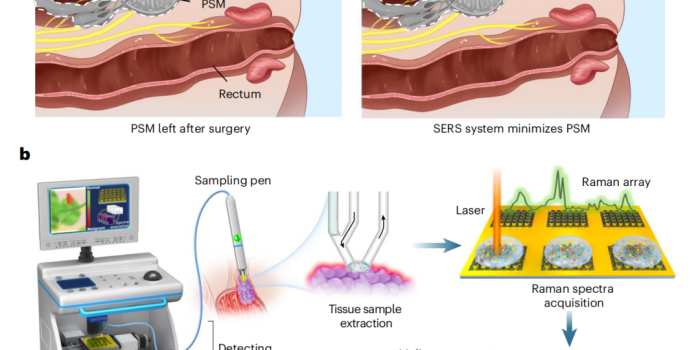
在现代泌尿外科的版图中,前列腺癌(PCa)的手术治疗正处于一场前所未有的范式转移之中。长期以来,外科医生在执行根治性前列腺切除术时,始终徘徊在一种近乎残酷的权衡之间:一方面,为了彻底清除恶性组织,必须确保足够的切缘;另一方面,前列腺紧邻控制排尿和性功能的精细神经血管束,过度切除将不可避免地导致患者术后出现尿失禁或勃起功能障碍等生活质量危机。统计数据显示,切缘阳性(PSM)的发生率在临床上高达26%,这意味着超过四分之一的患者在经历手术痛苦后,依然面临肿瘤残留的风险。
传统的术中诊断手段,如冰冻切片分析(IFS),虽被称为金标准,却暴露出明显的时代局限性。它不仅耗时长达30至60分钟,更在很大程度上依赖于病理医生的主观经验,且采样范围极其有限,难以覆盖复杂的肿瘤边界。如今,这种“实验室滞后”的模式正在被一种基于表面增强拉曼散射(SERS)和人工智能(AI)的实时导航系统所打破。
2025年11月18日,由复旦大学李聪教授团队领衔,联合中国科学院深圳先进技术研究院郑海荣院士、杨慧研究员团队以及复旦大学附属中山医院王航教授等,在《自然-生物医学工程》(Nature Biomedical Engineering)发表了一项具有里程碑意义的研究。他们开发了一套无标记导航系统,通过在分子水平上同时捕捉组织酸碱度(pH)和前列腺特异性抗原(PSA)的酶活性,实现了对原位肿瘤恶性程度(特别是Gleason分级组 GG≥3)的精准识别。这不仅是一次传感技术的升级,更是一场将生化逻辑直接植入手术刀的医疗革命。
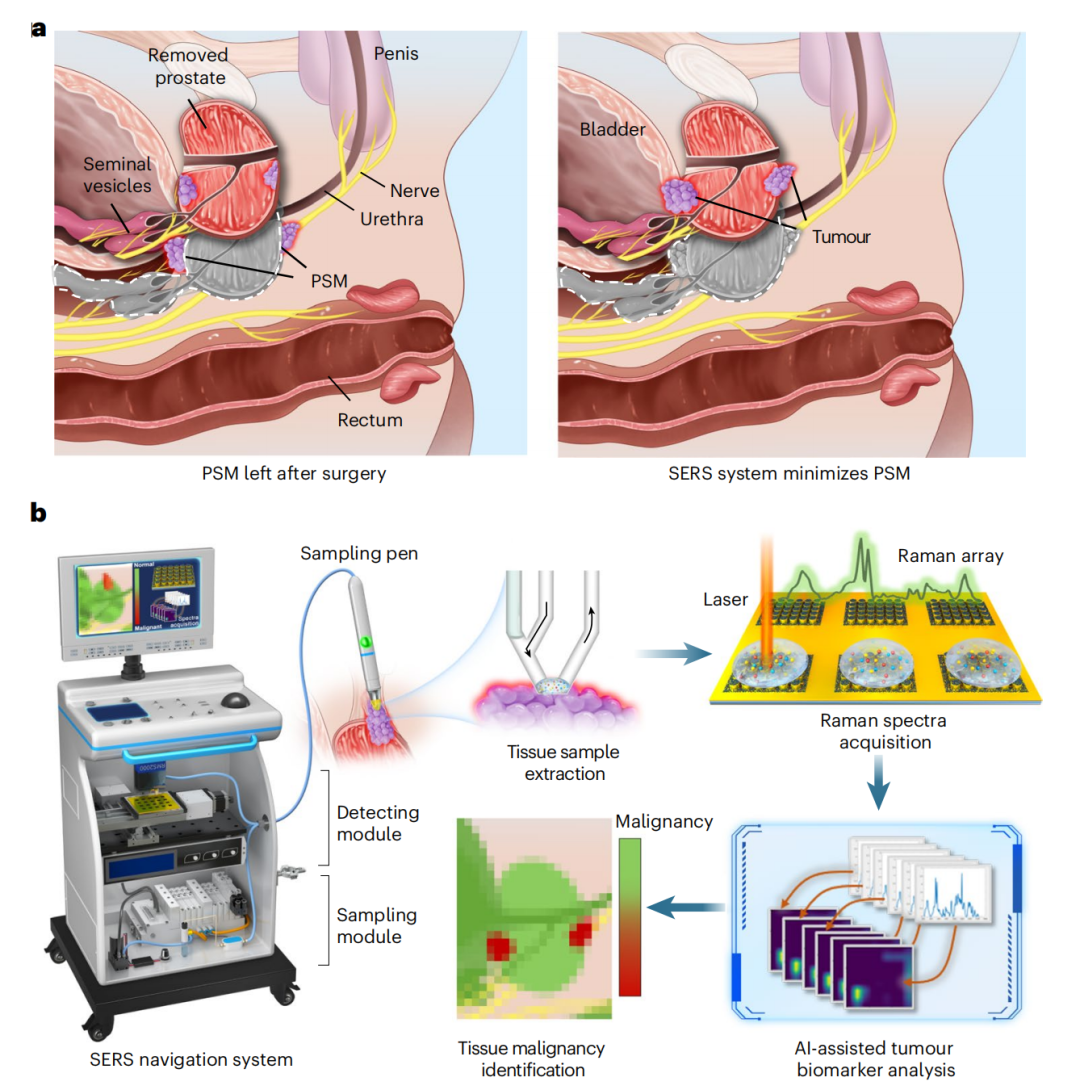
前列腺肿瘤的恶性程度评估在临床上主要依赖于Gleason分级系统(GG)。对于GG≥3的高危病灶,能否精准切除直接决定了患者的无进展生存期(PFS)和总体死亡率。研究团队并未盲目追求单一标志物的灵敏度,而是深入肿瘤代谢的本质,构建了pH与PSA的双指标评价体系。
作为癌症的一个保守特征,恶性细胞普遍经历从氧化磷酸化到糖解途径的转变,即瓦博格效应。这种代谢重塑导致乳酸的大量产生和细胞外环境的酸化。研究表明,细胞外液的酸度与前列腺癌的侵袭性呈正相关,恶性程度越高的GG亚型,其微环境越酸。然而,pH值作为单一指标存在“伪阳性”隐患:炎症反应同样会导致局部酸化,而低度恶性肿瘤的酸化程度可能并不显著。
前列腺特异性抗原(PSA)不仅是血清筛查的关键,其在组织内的浓度比血清高出四个数量级。当正常的前列腺腺上皮细胞发生恶性转化时,其分泌PSA的功能会由于上皮屏障的破坏和细胞极性的丢失而减弱。这种局部PSA活性的降低,恰恰为区分肿瘤组织与正常腺体提供了极佳的互补维度。通过整合pH(反映代谢强度)与PSA(反映组织功能),系统能够构建出一个更具鲁棒性的诊断矩阵,有效解决了炎症干扰和低度恶性肿瘤的识别难题。
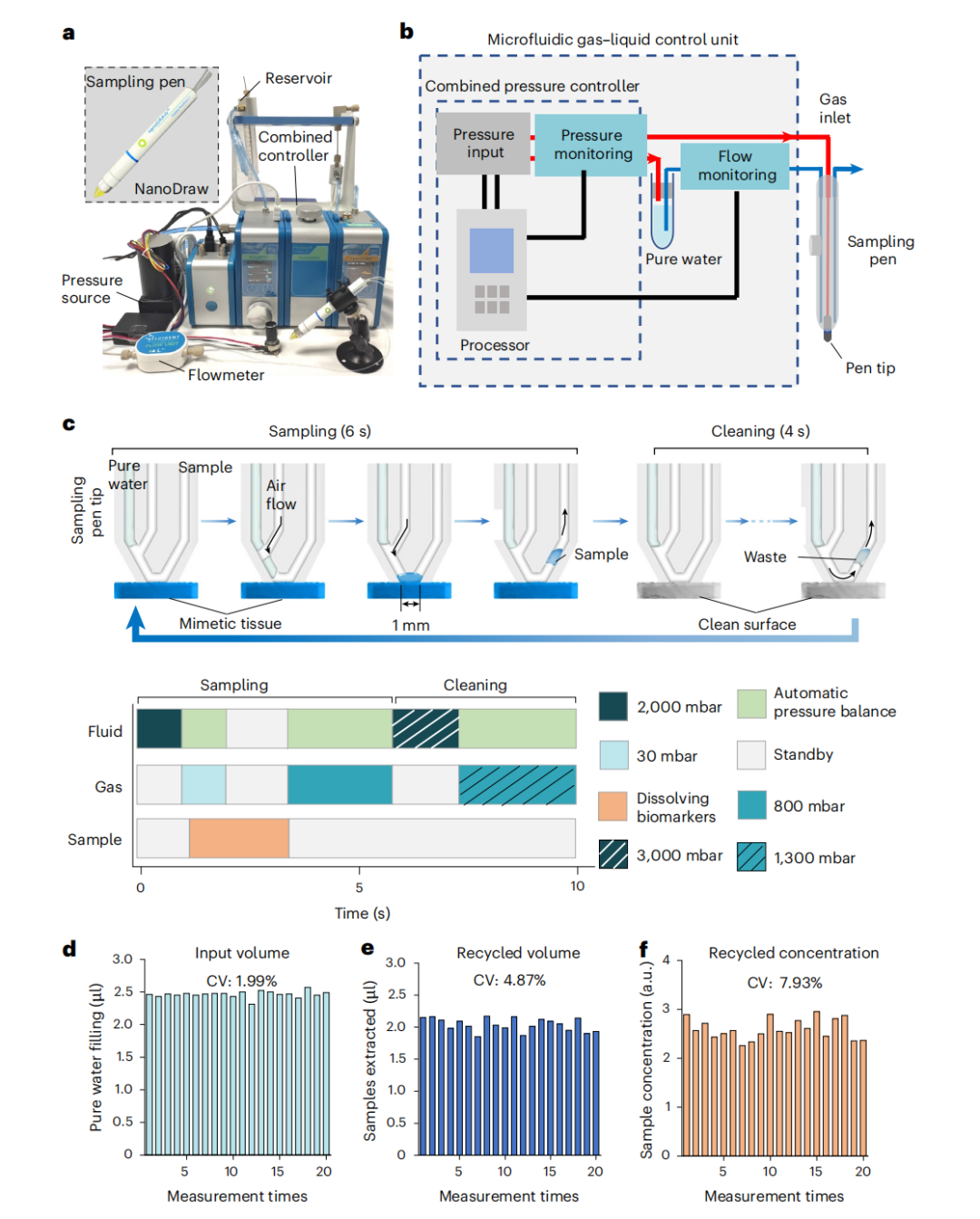
为了在不损伤组织的前提下获取这些生化信息,研究团队开发了一款名为NanoDraw的自动化采样笔。这一设备是整个导航系统的“触角”,其背后蕴含着精密的气液控制逻辑。
NanoDraw的设计突破了传统采样工具的限制。其笔尖集成了流体、气体和样本通道,采用非对称布局。在采样过程中,系统通过微流控单元精确泵入2.5µL的纯水。利用气压(约30 mbar)将水滴分割并推向组织表面,轻触即可溶解表面标志物。
|
性能指标 |
测量均值 |
变异系数(CV) |
|
输入水滴体积 |
2.464 µL |
1.99% |
|
回收样本体积 |
2.038 µL |
4.87% |
|
溶质提取浓度 |
2.60 a.u. |
7.93% |
这种高重复性的采样能力确保了后续SERS检测的稳定性。采样过程仅需6秒,随后系统会自动进入4秒的清洗流程,有效防止了手术过程中的交叉污染。相较于2025年同样备受关注的MasSpec Pen,NanoDraw在水滴分割和防止残留方面展现出了更强的微观流体控制能力。
如果说采样笔是触角,那么纳米压印的SERS阵列则是系统的“生化大脑”。为了实现超灵敏检测,研究团队放弃了均匀性较差的胶体金,转而采用电子束光刻与纳米压印技术在大尺寸硅片上制备了高度规整的金纳米柱阵列。
研究者通过时域有限差分(FDTD)模拟,对纳米柱的高度进行了精细化匹配。实验数据验证了理论预测:当纳米柱高度为105 nm、直径180 nm、间隙30 nm时,在785 nm激发激光下产生的局域表面等离激元共振(LSPR)最强,SERS强度较70 nm高度提升了近百倍。
阵列表面修饰了具有Au-S共价键的特定分子开关:
-
IR7p(pH响应者):利用哌嗪基团的可逆质子化,在酸性环境下增强558㎝-1的峰强,而311㎝-1的参考峰保持不变,实现了不受总浓度干扰的比例计式pH测量。
-
尼罗蓝标记肽(PSA响应者):采用含有HSSKLQ序列的底物肽段。PSA酶会精确切断该肽段,使末端的尼罗蓝(NB)分子脱离金表面,导致其拉曼特征峰(589 和 1173㎝-1)随PSA浓度增加而单调减弱。
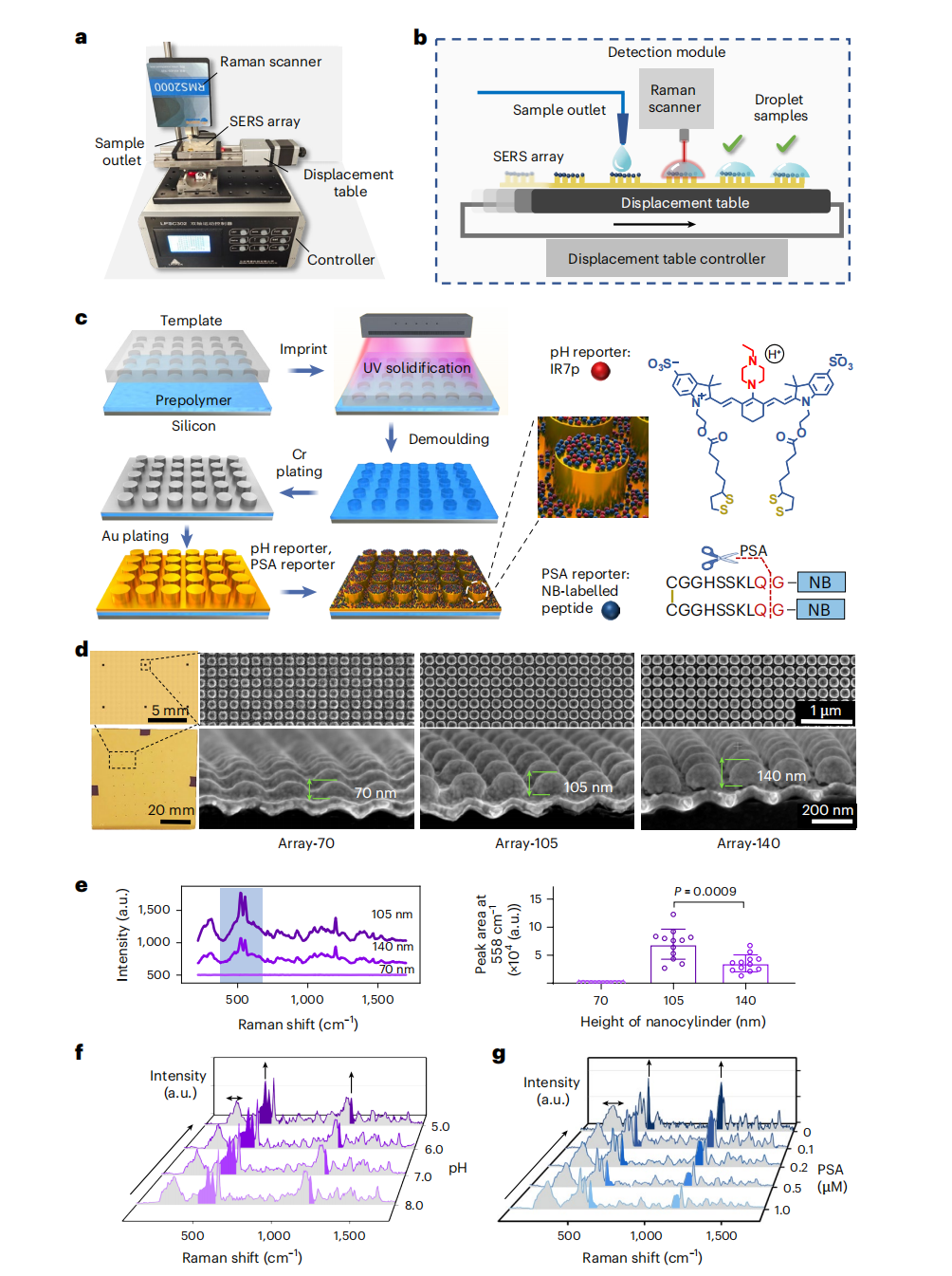
这种将化学敏感性与物理谐振相结合的策略,使得系统能够在2秒内完成对单个样本滴的定量分析,分辨率达到了前所未有的生化级别。
在数据解释层,研究团队并未满足于传统的1D卷积神经网络(1D CNN)。由于拉曼光谱包含复杂的峰位重叠和背景基质干扰,单纯的一维分析往往会丢失分子振动模式之间的非线性关联。
研究者引入了非线性动力学中的循环图变换技术,将1D光谱序列映射为2D矩阵图像。这种变换公式如下:
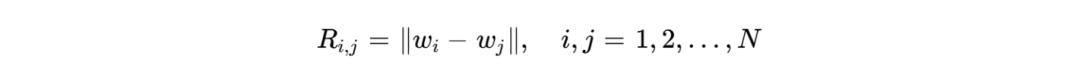
通过这种方式,光谱中的周期性峰值、噪声波动和能量分布被转化为AI更易理解的视觉拓扑特征。
基于ResNet34骨干网络的2D模型在16,229条光谱的数据集上表现卓越。对比测试显示,在关键指标的预测中,2D模型显著优于1D模型。
|
评估指标 |
1D-CNN误差 |
2D-CNN误差 |
提升幅度 |
|
pH 预测 (Mean Error) |
±0.16 |
±0.07 |
56% |
|
PSA 预测 (Mean Error) |
±0.05 |
±0.01 |
80% |
通过Grad-CAM(梯度加权类激活映射)技术,模型甚至向医生“解释”了其判断依据:热图中亮度最高的区域精确对应了报告分子的振动峰。这种可解释性AI(XAI)的应用,显著增强了临床医生对系统自动决策的信任感。
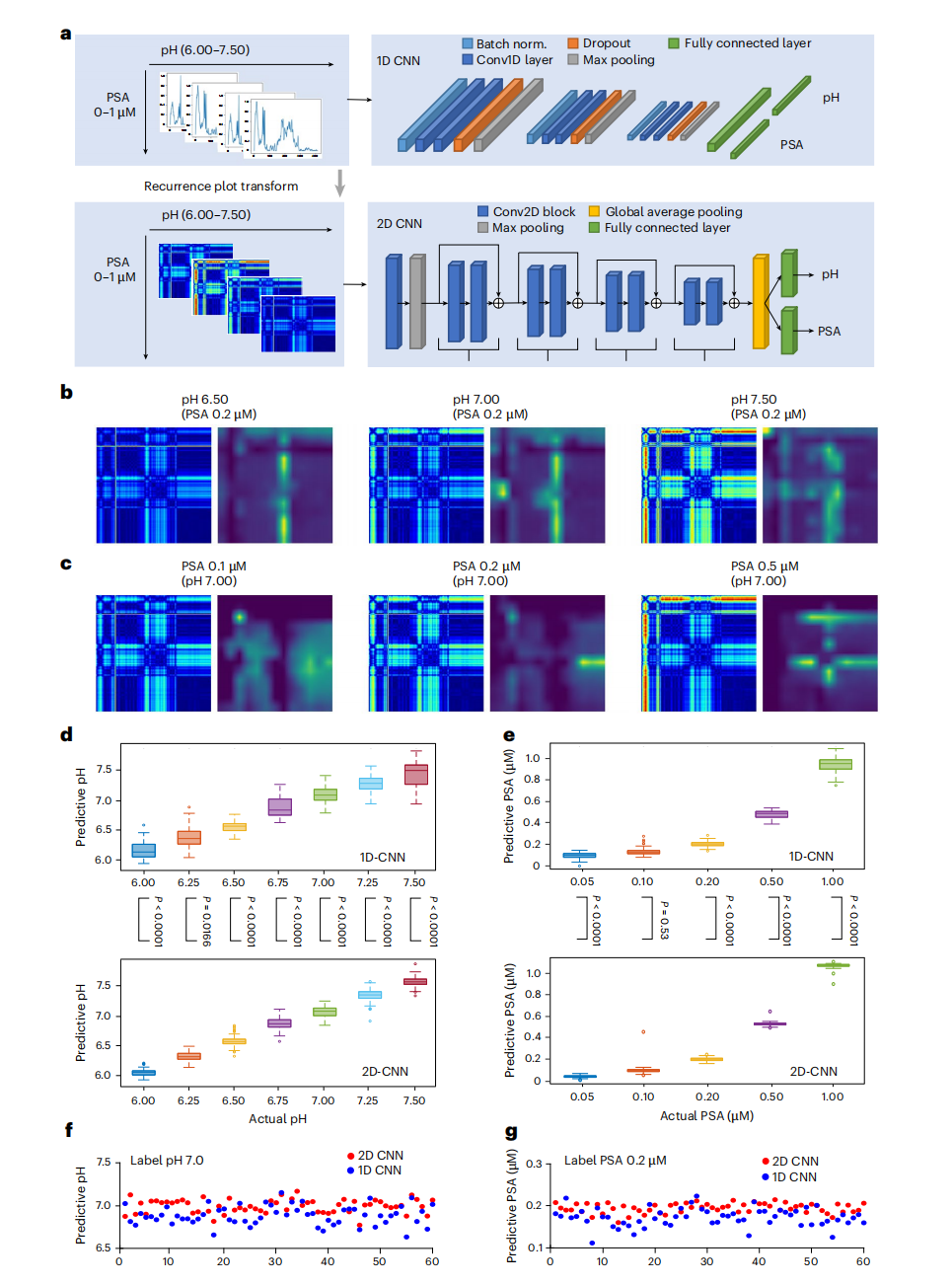
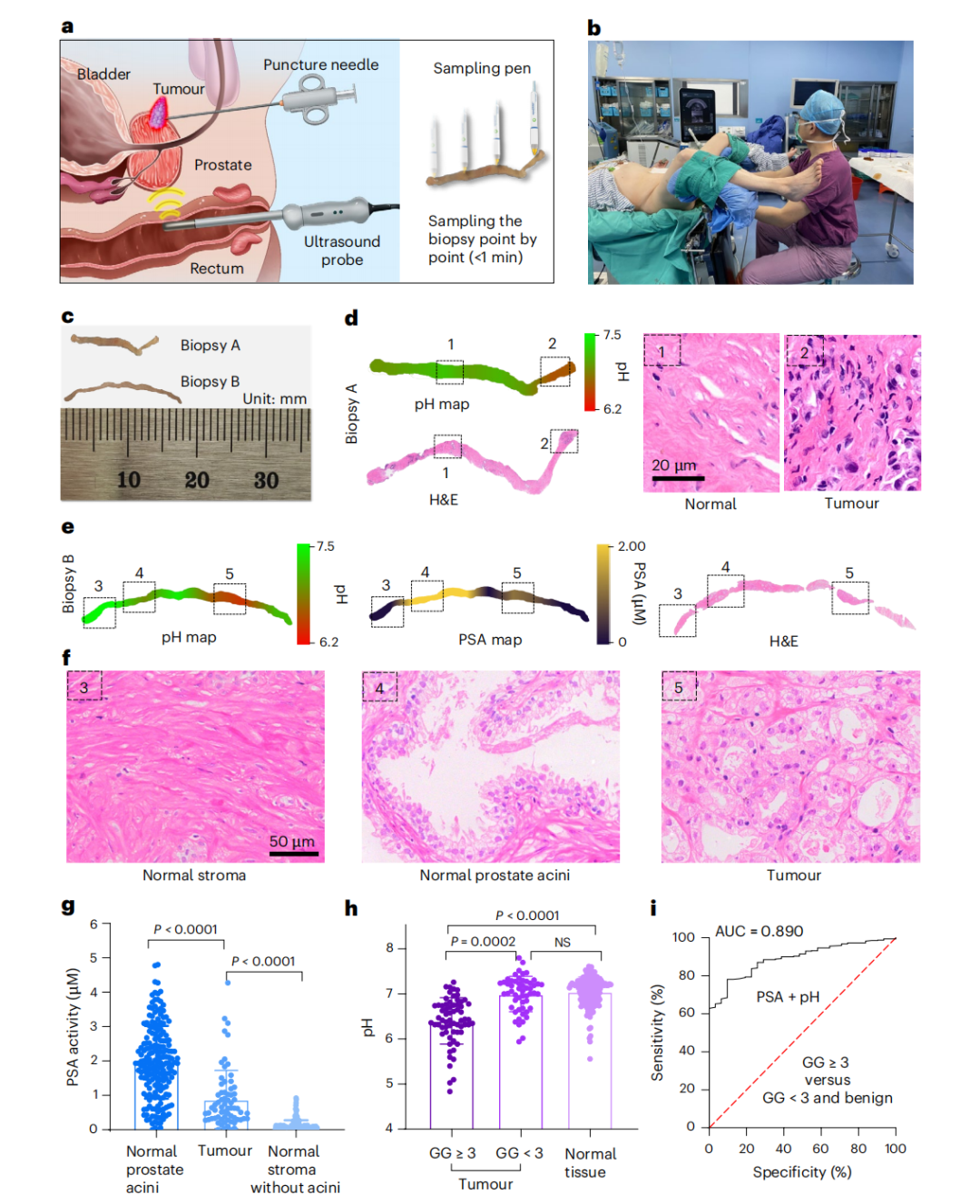
系统的临床价值最终在上海多中心开展的144例前列腺癌患者样本中得到了验证。研究涵盖了从穿刺活检(Biopsy)到术中切除标本(Radical Prostatectomy Specimens)的全场景。
在针对术前穿刺组织条的扫描中,系统通过1.5 mm间隔的逐点扫描,绘制了高分辨率的pH和PSA动态图谱。
● 高恶性病灶识别:病理确认为GG≥3的区域表现出显著的强酸性(pH≈6.39),而低恶性或正常组织的pH约为7.00。
● 组织学相关性:高恶性区域在H&E染色下对应着细胞密度极高、腺体结构消失的侵袭性特征,这与SERS系统的物理化学读数高度吻合。
通过受试者工作特征曲线(ROC)分析,该双指标系统在识别GG≥3的恶性肿瘤方面达到了0.890的AUC,显著超越了目前所有已知的无标记光学检测手段。
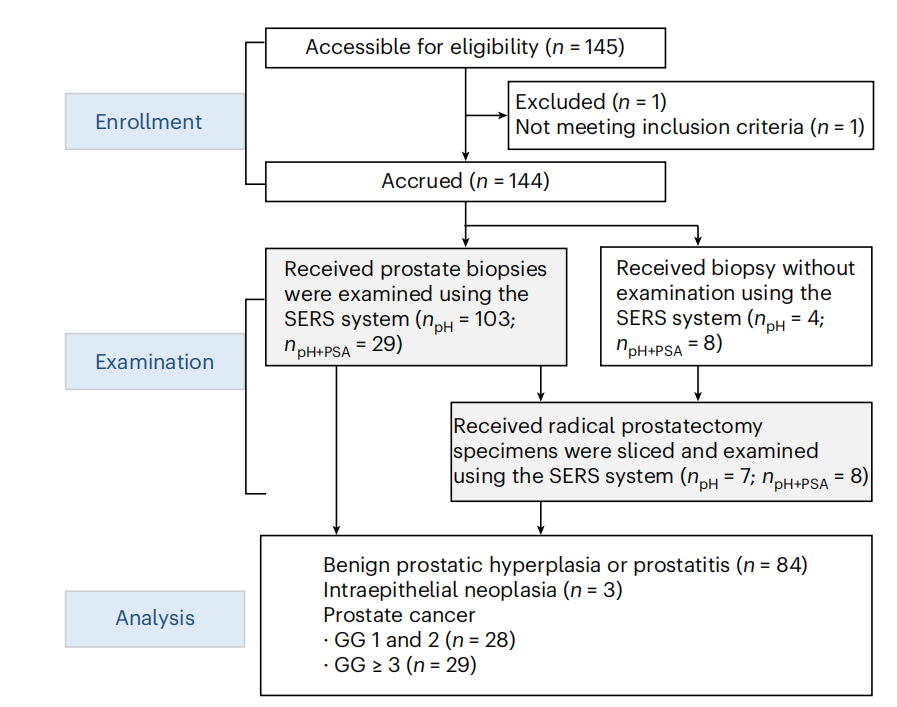
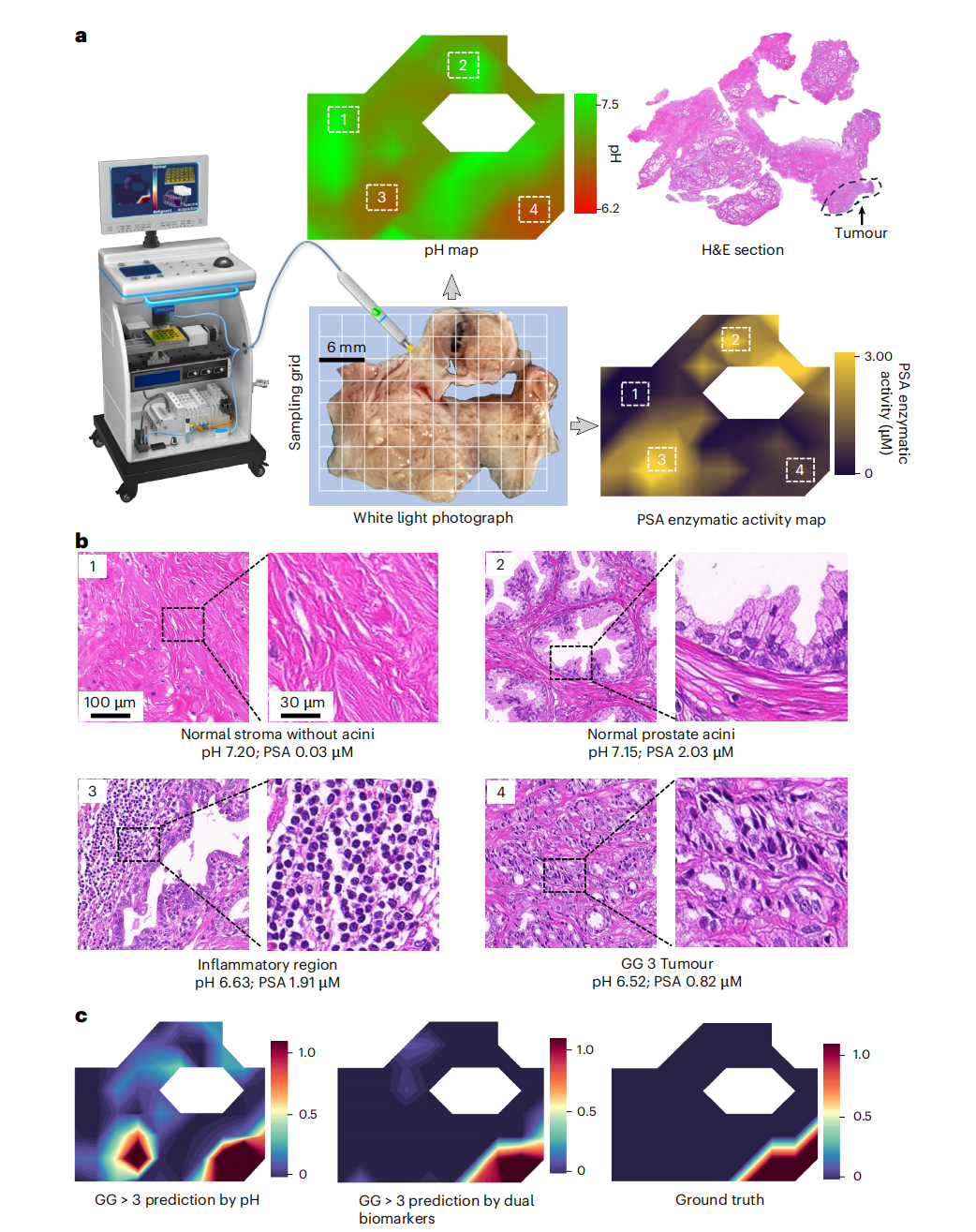
在前列腺切除术中,最令医生头痛的是如何区分癌症与前列腺炎,因为两者在宏观影像上往往难辨。该系统利用PSA活性的反向变化成功解决了这一难题。
在一个典型案例中,系统识别出切片中的两个酸化区域。若仅凭pH指标,两者都会被视为肿瘤。然而,通过融合PSA图谱,系统发现其中一个区域PSA活性极高。病理分析证实该区域是因炎症导致的局部酸化,而非恶性肿瘤。利用这种双指标加权,系统生成的“恶性热图”与标准病理切片的重叠率(IoU)达到了85.71%,实现了对高恶性度孤岛的精准定位。
该SERS系统的成功并非孤例。2025年,全球范围内涌现出多项旨在“消灭切缘阳性”的创新技术,它们正共同塑造着精准外科的未来。
由Livia Eberlin领导的团队在2025年对其MasSpec Pen进行了模块化升级。最新发表在《分析化学》上的研究显示,该系统已能从患者皮肤表面快速筛查阿片类药物。同时,MasSpec Pen正在巴西、美国等多地进行肺癌和甲状腺癌的临床评估。尽管其提供的是全代谢组学指纹,但相较于SERS系统,质谱仪的高昂维护成本和大型化依然是其向基层医疗推广的壁垒。
2025年,靶向PSMA的近红外二区(NIR-II)荧光引导手术(FGS)也取得了重大突破。ICG-PSMA-D5和68Ga-P3等探针相继进入一期临床。这种基于外源探针的方案提供了实时、广阔的视觉引导。然而,SERS系统的核心优势在于“无标记”——无需注射任何化学物质即可通过内源标志物进行分级,这在监管审批和患者安全性方面具有天然优势。
|
技术路径 |
核心指标 |
2025年最新突破 |
优势 |
挑战 |
|
SERS 导航 (复旦/中科院) |
内源pH + PSA |
AUC 0.89, 2min出结果 |
无需造影剂, 自动分级, 高准确度 |
基底制造一致性要求高 |
|
MasSpec Pen (Baylor/UT) |
脂质/代谢组 |
阿片类筛查, 巴西多中心临床 |
分子覆盖面极广, 96%准确率 |
依赖质谱仪, 成本高昂 |
|
iKnife (Imperial College) |
烟雾脂质指纹 |
集成 da Vinci 5 平台 |
真正的手术中实时反馈 |
依赖组织烧灼, 易造成边缘损伤 |
|
NIR-II FGS (PSMA) |
跨膜蛋白表达 |
第一例人体试验成功 |
实时视觉显影, 深度穿透 |
需外源注射, 易受非特异性扩散干扰 |
|
NeuroSAFE (IFS) |
组织形态学 |
2025 EAU RCT 阳性结果 |
金标准, 指导神经保护 |
耗时长 (70min), 依赖病理医师 |
随着前列腺癌发病率在中国的攀升,以及机器人辅助根治性前列腺切除术(RARP)的普及,对术中实时病理工具的需求呈现出爆发式增长。市场报告预测,拉曼光谱市场到2030年将达到17.5亿美元,而AI在病理领域的渗透率将以25.56%的复合年增长率(CAGR)飙升。
2025年的一项成本效益研究指出,虽然冰冻切片(NeuroSAFE)是目前标准,但其导致的单次手术时长增加会显著推高医疗支出。相比之下,SERS导航系统这类快速、自动化的工具在每年执行超过160例前列腺切除术的高流量医院中,展现出了更优的经济效益。它不仅减少了二次手术的概率,更通过精准的神经保存,降低了术后长期康复的社会成本。
复旦大学与中科院团队目前正致力于设备的便携化与集成化。未来,该系统有望通过微流控芯片的耗材化和拉曼扫描仪的微型化,实现即插即用。此外,通过更换SERS基底上的报告分子,这一平台可以迅速迁移至胶质瘤、乳腺癌或肝癌的手术导航中。
前列腺癌根治术的历史可以追溯到1900年,从最初的开放手术到2000年的微创机器人革命,每一步跨越都旨在解决手术的安全性与彻底性之争。今天,我们正站在第三次革命的门口——“智能分子导航”。
这种将无标记传感器、微流控采样与AI图像识别算法深层融合的系统,彻底改变了外科医生看待肿瘤边缘的方式。它不再只是肉眼的观察或滞后的病理报告,而是变成了实时跳动的生化曲线。当内源性的代谢信号pH与功能信号PSA在AI的矩阵中交汇,手术刀便拥有了超越人类经验的分子视野。正如《麻省理工科技评论》所揭示的那样:最好的技术往往是无声的,它隐身于复杂的算法和微观的纳米结构之后,却在生死攸关的毫厘之间,重塑了精准医疗的定义。
[1] Jin, Z., Chen, S., Dong, X. et al. Label-free navigation system for grading prostate tumour malignancy in situ via tissue pH and prostate-specific antigen activity. Nat. Biomed. Eng (2025).https://doi.org/10.1038/s41551-025-01561-y END 撰文 | 赵亚军 排版 | 张艳青 审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
Nature Communications | 清华大学与剑桥大学等团队联合研发:大模型结合柔性传感,助力中风构音障碍患者重获自然发声
点击关注医工学人
本篇文章来源于微信公众号: 医工学人