星标“医工学人”,第一时间获取医工交叉领域新闻动态~

长期以来,医生像透过一根吸管观察人体内部的“生命之河”(血液循环)。2025年10月28日,发表在《Nature Communications》的一项结合多透镜阵列与超声定位显微技术的新方法,由来自法国巴黎物理医学研究所团队完成,首次能以毫米级视野、微米级分辨率、三维动态地“看见”并量化整个器官——从心脏、肾脏到肝脏——的完整微血管网络与血流动力学。这项技术成本仅为传统方案的1/5,却有望成为连接基础研究与临床诊断的桥梁,为微循环疾病的早期发现与AI驱动的精准医疗打开全新局面。

要理解人体的健康与疾病,观察其内部的微循环(毛细血管级别的血流)至关重要。这如同观察一个城市的交通,只看主干道(大血管)远远不够,真正决定城市活力的,是延伸到每个街区的毛细血管网络。然而,要“看清”并“追踪”整个器官的微循环,一直是医学影像领域的巨大挑战。
现有技术方案存在三大根本性瓶颈:
视野与分辨率的“鱼与熊掌”:临床金标准CT血管造影能看清大血管的解剖结构,但辐射强、无法动态评估血流,且对微血管分辨率不足。4D血流MRI虽能评估血流动力学,但空间分辨率有限(毫米级),且成本高昂、普及性差。
超声的“天花板”:超声波成像成本低、便携,但其分辨率受限于物理衍射极限,通常只能看到几百微米以上的结构,无法窥见微血管。传统的超声定位显微镜技术能通过追踪造影微泡实现超分辨率成像,但此前多限于小动物(如小鼠)的2D或小范围3D成像,因其探头复杂,若想覆盖人类器官,需要数千个通道,硬件成本和技术复杂度呈指数级上升。
数据的鸿沟:为了获得器官尺度的微循环动态信息,每秒钟需要处理高达3000亿体素的数据,这是一个令现有系统窒息的数据量级。
简言之,我们需要一种既能看得广(覆盖整个器官)、又能看得清(微米级分辨率)、还要看得动(三维动态血流)、并且用得起的影像技术。这正是法国研究团队试图攻克的终极目标。
这项研究的核心,是一个看似简单、实则巧妙的硬件革新:多透镜超声阵列。它摒弃了传统密集阵列为提高分辨率而不断增加微小阵元数量的“军备竞赛”思路,转而采用一种“大阵元 + 透镜”的逆向工程思维。
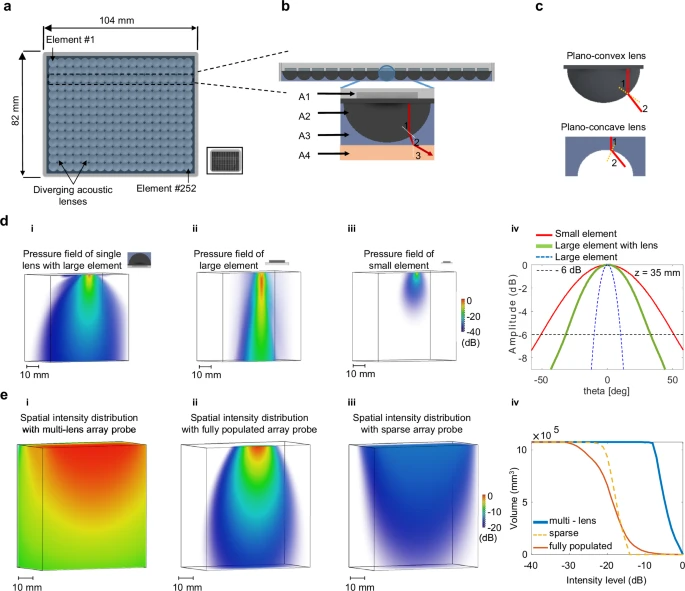
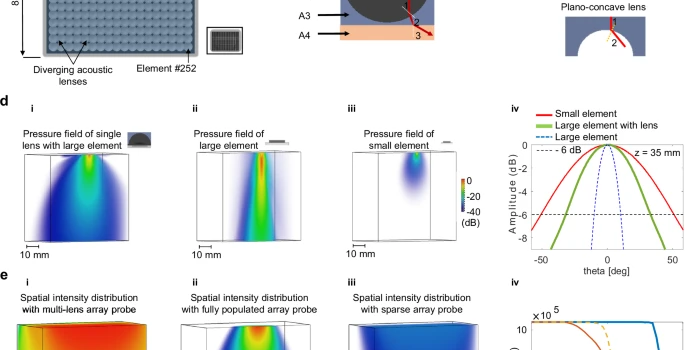
图1:多透镜阵列探头的定义、模拟研究及与传统方法的比较。
1)设计哲学
团队设计了一个由252个大尺寸压电元件(每个尺寸为3个声波波长)组成的大孔径(104 × 82 mm²)阵列。相比需要15042个小元件的传统方案,元件数量减少了98%。
2)核心“魔法”:复合发散透镜
大元件的痛点:单个大元件发射的声波指向性太强,像一束手电筒光,视野窄。
透镜的作用:在每个大元件前,集成了一个由平凸透镜和平凹透镜组成的复合发散透镜。根据斯涅尔定律,透镜改变了声波在不同介质(透镜材料与生物组织)中的传播速度,从而强制将“手电筒光”扩散为“泛光灯”,在不牺牲大元件高灵敏度和高能量输出的前提下,极大地拓宽了声束的覆盖角度(低指向性)。
3)结合“软件大脑”:3D超声定位显微镜
向血管内注射造影微泡,用上述阵列进行超高速(312.5 Hz体帧率)三维成像,精准定位并追踪成千上万个微泡的运动轨迹。通过长时间积累和复杂的算法处理,最终重建出远超衍射极限分辨率的三维微血管结构和血流速度场。
|
特性维度 |
传统密集矩阵探头 (技术瓶颈) |
新型多透镜阵列 (本研究突破) |
|
阵元数量 |
成千上万(例如覆盖相同孔径需15042个) |
仅252个 |
|
单阵元尺寸 |
小(约半波长,追求分辨率) |
大(3倍波长,追求灵敏度与能量) |
|
声束特性 |
高指向性(视野受限) |
低指向性 + 高能量(大视野高穿透) |
|
硬件复杂度 |
极高,通道数多,成本昂贵(约100万美元) |
极简,通道数少,成本低廉(<20万美元) |
|
成像视野 (FOV) |
小,通常局限于局部区域 |
超大,达 120 × 100 × 82 mm³,覆盖整个器官 |
|
空间分辨率 |
受限于衍射极限(数百微米) |
超越衍射极限,可达75-200 μm |
|
应用场景 |
局部、浅表或小动物成像 |
大型动物/人类全器官(心、肝、肾)成像 |
这项技术的巧妙之处在于,它用光学领域的透镜思维解决了声学领域的硬件难题,通过物理层面的创新设计,将硬件复杂度与成本降至极致,为高性能三维超分辨率超声成像的大规模临床应用铺平了道路。
研究团队通过模拟 → 体外 → 离体 → 活体的完整链条,严谨地验证了这套系统的能力。
1)模拟与体外验证
透镜效果验证:模拟显示,带有复合透镜的大元件,其角向指向性(-6 dB)达到33.17°,是同等大小无透镜元件的3倍多,证实了其扩宽视野的能力。
分辨率与流速测量:在体外流管模型中,系统成功重建了微泡密度与流速的三维图。通过分析泊肃叶流速剖面,证明了其空间分辨率高达75微米(λ/20),并精确量化了不同设定流速(R² = 0.98)。
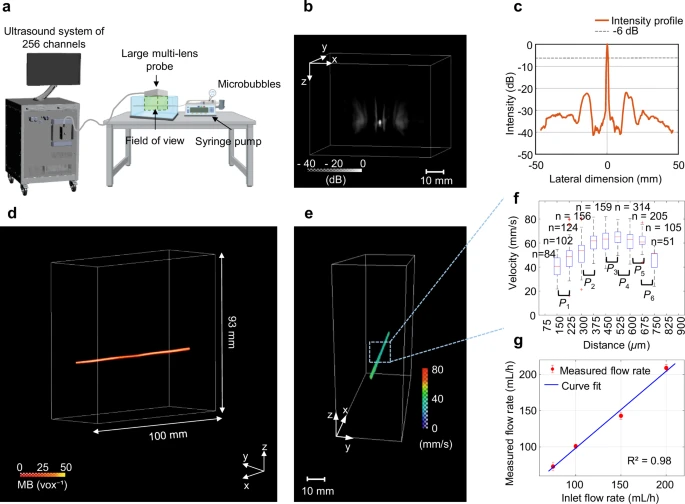
图2:多镜头阵列的体外验证。
2)离体全器官成像(猪心)
在灌流离体猪心中,系统以史无前例的 120 × 100 × 82 mm³ 的成像体积,首次完整绘制了整个冠状动脉树的三维地图(图3)。不仅看清了血管结构,还测得了血流速度剖面,为心血管研究提供了前所未有的细节。
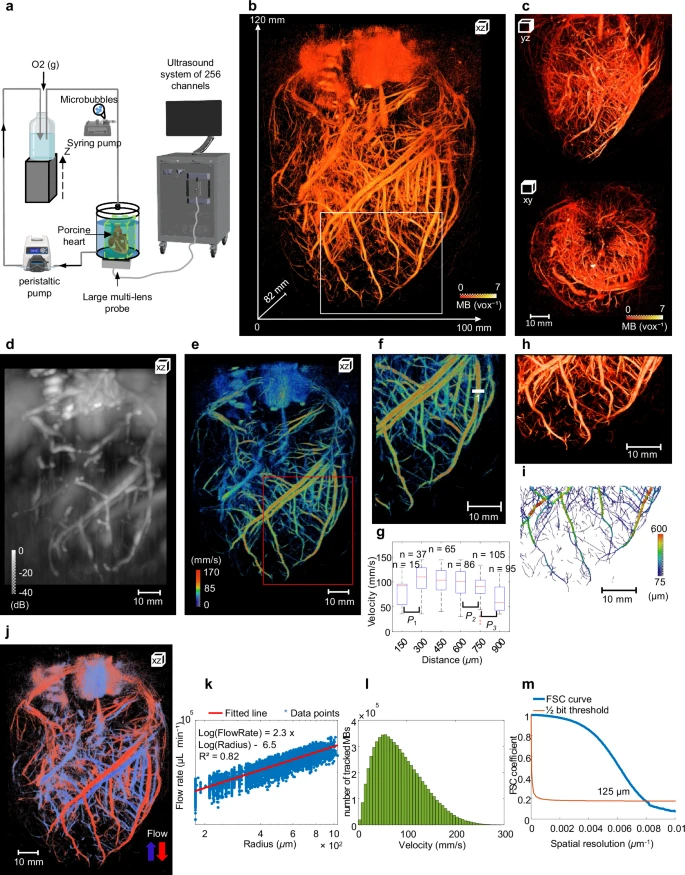
图3:一只离体猪心的三维冠状动脉分布图。
3)活体成像(猪肾与猪肝)
肾脏:在活体猪中,成功对肾脏进行了 60 × 80 × 40 mm³ 体积的成像,获得了147微米的空间分辨率。系统不仅区分了动脉(红色,向上流)和静脉(蓝色,向下流),还验证了血管半径与流量的关系符合默里定律(幂律指数2.13,R²=0.70),这是血管系统“设计最优性”的体现。
肝脏:尽管面临呼吸、心跳等多重运动干扰,系统仍成功对 65 × 100 × 82 mm³ 的肝区进行成像,分辨率为200微米,并成功区分了门静脉(无搏动,均匀流速)、肝动脉(搏动性)和肝静脉(搏动性)的血流特征。
运动校正:针对活体生理运动,开发了基于三维能量多普勒的块间刚性运动校正算法,显著提升了血管结构的对齐度和图像质量。
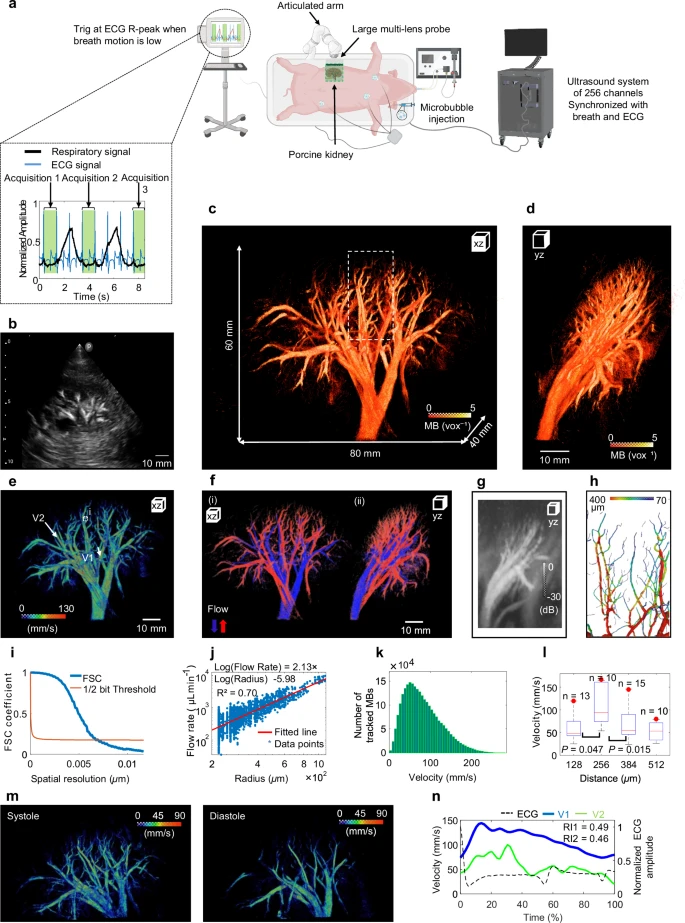
图4:体内猪肾脏。
这些实验系统性、阶梯式地证明了:多透镜阵列+3D ULM技术,确实有能力在大型动物身上,以接近临床可接受的条件下,实现全器官尺度的高分辨率、功能性微循环成像。
这项技术一旦走向成熟,其影响将是革命性的。
-
重塑生物医学研究范式:它将使在大型动物模型(如猪)上进行与人类生理更接近的全器官微循环研究成为常规。从心血管疾病、慢性肾病到肝纤维化,研究人员将能在三维空间中量化病理改变,极大加速新药研发和对疾病机制的理解。
-
开辟全新临床诊断路径:
-
早期诊断:为慢性肾病、小血管病、早期肝纤维化等目前缺乏有效无创定量诊断工具的疾病,提供前所未有的检测手段。
-
器官移植评估:可用于评估供体心脏、肾脏的微血管质量,辅助移植决策。
-
治疗监测:实时、定量地评估针对微循环的疗法(如抗血管生成药物)是否起效。
-
赋能AI与数字孪生:该技术产生的海量、高保真的全器官血管与血流四维数据集,正是训练高级AI算法、构建个人“血管数字孪生”模型所亟需的“燃料”。未来,医生或许能在虚拟模型中模拟药物对你个人血管网络的影响,实现真正的个性化医疗。
-
商业化前景:其低于20万美元的系统成本,远低于高场强MRI或高端CT,且基于成熟的超声平台,使其具备了大规模部署于研究型医院甚至顶级临床中心的潜力。它并非要取代CT或MRI,而是在微循环功能成像这一细分且关键的空缺领域,建立了一个高性价比的解决方案。
尽管前景广阔,我们必须清醒地看到这项技术走向广泛应用前必须翻越的几座大山:
-
分辨率仍有提升空间:当前75-200微米的分辨率足以观察小动脉、小静脉,但仍无法清晰分辨直径小于10微米的最细的毛细血管。未来需开发更高频率(2-3 MHz)的透镜阵列,在穿透深度和分辨率间寻找新平衡。
-
活体成像的挑战:肝脏成像结果目前细节仍较粗略,反映了在复杂生理运动和解剖结构(如肋骨遮挡)下成像的难度。需要进一步优化微泡注射协议、采集时长和针对性的运动校正算法。
-
探头舒适性与适应性:大尺寸探头在施加压力以确保声学耦合时可能造成患者不适。需要设计声学透射垫,并针对不同器官(如经颅脑成像)开发特定形状的探头。
-
临床转化路径:目前的研究仍处于大型动物实验阶段。迈向人类临床试验,需要解决微泡造影剂在人体中的安全性与标准化注射方案、针对人体不同部位(如通过颅骨进行脑成像)的探头优化等一系列问题。
-
算法与数据处理:虽然栅瓣在ULM处理中被有效过滤,但在传统的B模式或多普勒成像中仍可能造成伪影。需要发展更先进的波束形成或后处理算法。同时,海量数据的实时处理与可视化也是工程化的一大挑战。
结语: 这项研究代表了一种典型的突破性创新——不是通过更复杂、更昂贵的“堆料”,而是通过跨学科的物理洞察和巧妙的工程设计,将不可能变为可能。它为我们窥视生命最细微处的节律打开了一扇新窗。然而,从实验室的“惊艳演示”到临床的“可靠工具”,中间依然是一条需要科学家、工程师和临床医生共同跋涉的漫漫长路。我们期待的,是这扇窗最终变成一扇门。
[1]Haidour, N., Favre, H., Mateo, P. et al. Multi-lens ultrasound arrays enable large scale three-dimensional micro-vascularization characterization over whole organs. Nat Commun 16, 9317 (2025). END 编辑 | 郝娅婷 排版 | 张艳青 审核 | 医工学人理事会
https://doi.org/10.1038/s41467-025-64911-z
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
Nature Medicine | 仅凭一晚睡眠,预测130种疾病!斯坦福大学“睡眠AI”突破,是否颠覆了疾病预防体系?
Nature Machine Intelligence | 清华大学团队开发基于统一扩散Transformer框架的多模态心血管信号生成模型
点击关注医工学人
本篇文章来源于微信公众号: 医工学人