星标“医工学人”,第一时间获取医工交叉领域新闻动态~

2025年10月22日,由来自南方科技大学、香港城市大学和香港科技大学的研究团队开发了一款集传感与操控于一体的多功能纳米探针,并将其整合进全自动机器人平台。该平台首次实现了在不使用任何荧光标记的情况下,从活细胞中精准定位、抓取并提取线粒体,并能将提取的活性线粒体移植到其他活细胞内。这项技术以极高的时空分辨率和极低的细胞损伤率,突破了传统细胞内操作的瓶颈,为细胞器层面的研究、疾病机制探索乃至未来的“细胞器移植疗法”提供了革命性的工具。
过去数十年,科学家们一直梦想着对细胞内部进行精细的“手术”,如同在宏观世界操作机械一样,对特定的细胞器进行提取、移植或修复。然而,这个梦想面临着三大“不可能三角”般的困局: 1 . “看见”的代价:为了在显微镜下定位微小的细胞器(如线粒体),绝大多数先进技术依赖于荧光标记。然而,激发光本身会造成光损伤和光毒性,改变细胞的生理状态,甚至杀死细胞。这就像为了看清黑暗中的目标而使用强光手电,但强光却会灼伤目标本身。 2 . “定位”与“操作”的错位:即使看见了目标,如何让机械探针精确地移动到那个位置?在亚微米尺度下,布朗运动和细胞质流会轻易地将目标推离。传统的“传感-执行”分离式系统,由于坐标系难以精确对齐和时间延迟,导致操作成功率极低。好比在风浪中,用望远镜看到了远处的小船(传感器),再指挥另一艘船(执行器)去捕捉,过程充满了不确定性。 3 . 操作的“入侵性”:细胞极其脆弱。探针的插入位置、速度、深度等参数,会深刻影响细胞的迁移、生长、分化乃至生死。手动或半自动的操作往往带来不可预测的细胞死亡和极差的实验可重复性,使得研究结果难以解读和验证。 这些挑战,使得真正的、可重复的、低损伤的“单细胞手术”和“细胞器移植”长期停留在概念阶段。
来自上海科技大学等单位的研究团队,通过设计一款前所未有的双功能纳米探针,并构建全自动机器人系统,巧妙地解决了上述难题。其核心创新在于 “感知即执行”的一体化设计。 图1:纳米探针的结构、制造和功能。 技术原理简述: 该纳米探针尖端集成了两个独立寻址的铂纳米电极,赋予其双重身份: 身份一:超高灵敏“化学雷达”。铂电极对线粒体代谢产生的活性氧/氮物种(ROS/RNS)具有高选择性的电催化活性。当探针进入细胞,电极检测到局部的ROS/RNS浓度,并转化为微弱的电流信号(皮安级),从而实时绘制细胞内的“化学地图”,无光、无标记地定位线粒体。 身份二:纳米级“介电镊子”。当检测到足够强的ROS/RNS信号(阈值 >8 pA),系统瞬间切换模式。在两个电极间施加高频交流电场,产生强大的介电泳力,将纳米探针尖端约1.8微米范围内的线粒体牢牢“吸住”,完成抓取与提取。 图2. 自动机器人检测与操作线粒体。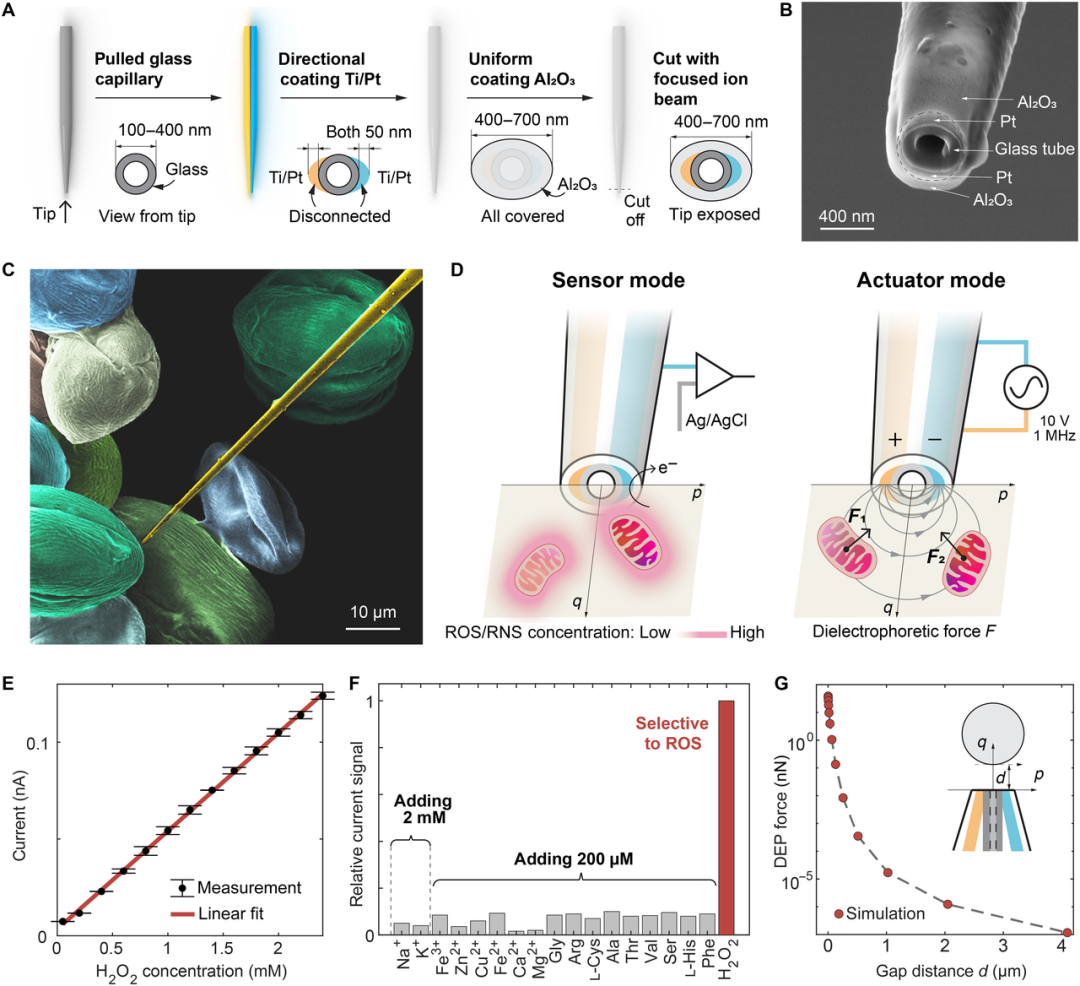
新旧技术对比: 特性维度 传统荧光引导式微操作 本研究的“无标签”机器人活检 引导方式 荧光标记成像(有创,光毒性) 电化学传感(无光,无标记) 时空分辨率 受限于光子数与曝光时间,存在权衡 传感速率1 kHz,执行速率1 MHz,亚微米空间分辨率 传感与执行 分离式,需复杂坐标对齐,延迟高 一体化于同一探针尖端,模式切换瞬时完成 细胞入侵性 较高,光损伤与机械损伤叠加 极低,细胞存活率高达96%(多次穿刺后仍达80%) 下游兼容性 荧光标记可能干扰生化、基因分析 无标记提取,样本可直接用于qPCR、测序等分析
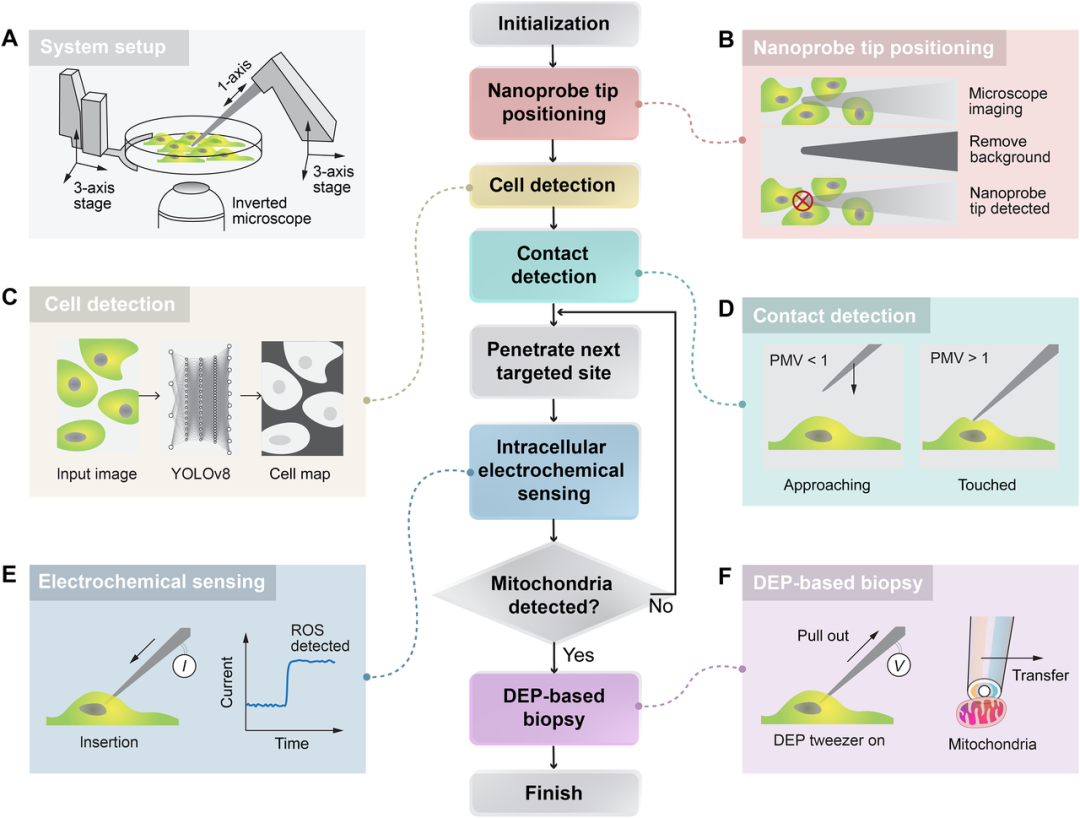
这套系统的“智能”不仅在于探针本身,更在于全自动化的流程控制:从基于深度学习的细胞识别与轮廓勾勒,到利用运动历史图像算法进行的膜接触探测,再到基于电化学反馈的穿刺与提取决策——整个过程由机器人精准、快速地执行,并完整记录所有操作数据,为分析和优化提供了可能。
研究通过一系列严谨的实验,验证了该平台的强大能力: 图3:自动化大规模单细胞ROS/RNS探测和生存率分析,结合活细胞无标记线粒体活检。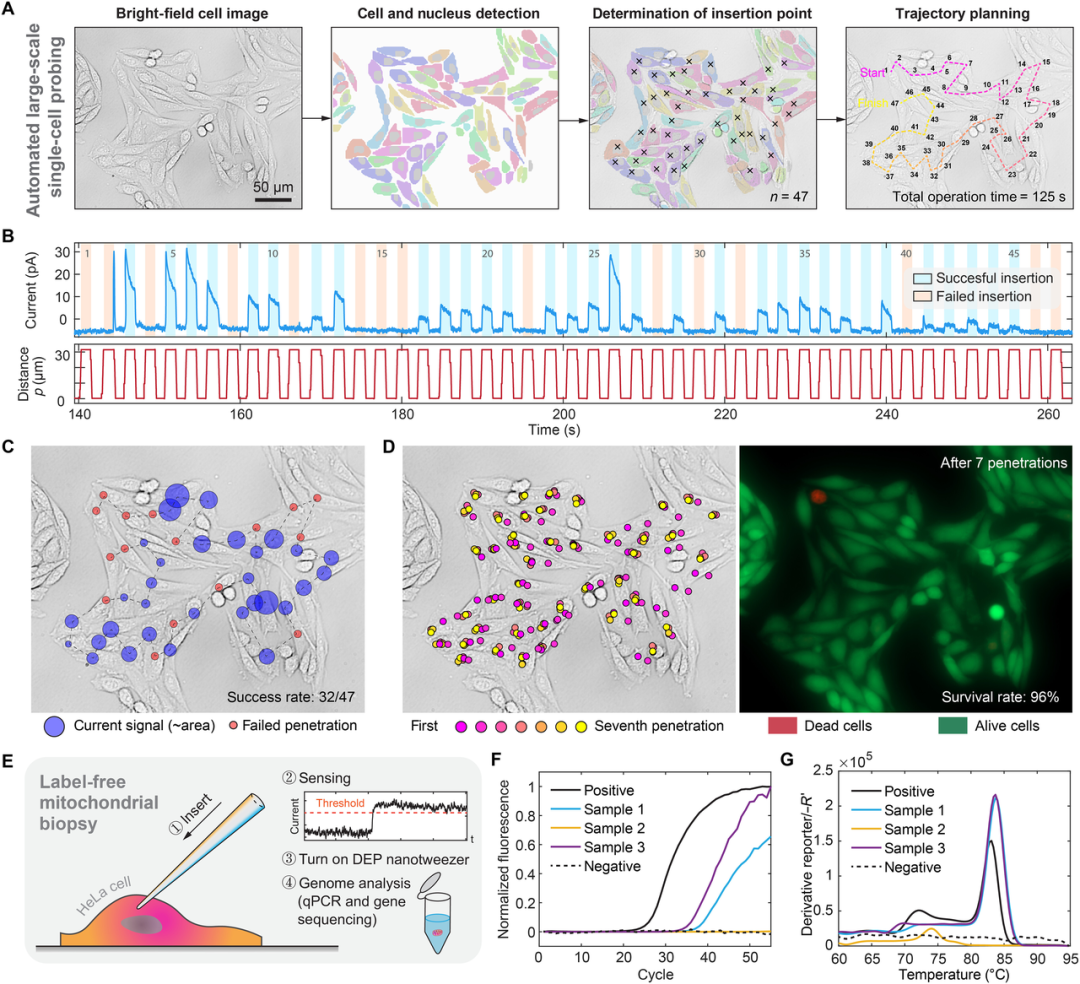
基础性能验证:探针对过氧化氢(一种ROS)的检测呈线性响应,选择性高,且性能稳定。模拟与实验均证实,其产生的介电泳力足以在纳米级范围内捕获目标。 无标签“化学定位”:在活细胞内,电化学信号与线粒体特异性荧光信号显示出显著的正相关性(皮尔逊系数0.65)。更重要的是,在细胞核区域,两种信号均很低,符合生物学常识,证明了ROS/RNS信号作为线粒体定位指示器的可靠性。 规模化、自动化操作演示:在一个包含47个细胞的密集区域内,系统在125秒内完成了对所有细胞的自动化穿刺与传感探测,成功率约68%。失败主要发生在未完全贴壁的圆形细胞上。全程数据被完整记录,这在细胞研究中是罕见的,极大增强了实验的可追溯性和可重复性。 核心突破:线粒体活检与验证: 提取:系统成功从活细胞中提取出线粒体,提取成功率受电压和持续时间影响(例如,在7V电压下等待60秒,成功率较高)。 验证:对提取物进行qPCR分析,显示标准的线粒体DNA扩增曲线;桑格测序证实序列与线粒体DNA匹配;膜电位检测显示提取的线粒体仍保持正常极化状态。这“三重验证”无可辩驳地证明了提取物的身份与活性。 迈向疗法:线粒体移植:研究展示了更具前瞻性的一步——将提取自红色荧光标记供体细胞的线粒体,移植到绿色荧光标记的受体细胞中。在9次独立试验中,观察到了多种结果:部分移植线粒体被排出;部分保持独立;而最激动人心的是,部分移植线粒体成功与受体细胞的线粒体网络发生了融合,甚至观察到了疑似由共转移mRNA介导的红色荧光增强现象。这直接证明了移植线粒体的生物活性和整合潜力。
这项技术的突破,其影响将远超实验室,可能深刻改变多个领域: 基础科研的新“显微镜”:它提供了一种无干扰、高时空分辨率研究细胞器动态、相互作用和异质性的全新工具。科学家可以像地质学家钻取岩芯一样,从单个活细胞的特定位置“活检”细胞器,进行多组学分析,以前所未有的精度解析细胞功能与疾病机制。 细胞治疗与再生医学的潜在路径:线粒体功能障碍与众多疾病(如代谢性疾病、神经退行性疾病、衰老相关疾病)密切相关。这项技术为实现 “细胞器置换疗法” 提供了概念验证和实用工具。未来,或许可以通过向患者细胞中移植健康的线粒体,来纠正或补偿功能缺陷,为治疗目前难以攻克的线粒体病开辟新思路。 合成生物学与细胞工程:它使得“组装”定制化人工细胞成为更具可行性的想象。从不同细胞中提取功能各异的细胞器,重新组装成具有新特性的“嵌合细胞”,或用于增强干细胞疗法中细胞的代谢活力。 药物研发的新平台:该平台可用于在单细胞水平高通量地测试药物对特定细胞器功能的影响,或作为精准递送系统,将药物直接送入细胞内的靶向细胞器。 商业化展望:目前该技术仍处于实验室原型阶段。走向临床应用,至少还需攻克:通量提升(目前仍是单次操作)、提取纯化流程优化以减少样本损失、与单细胞多组学分析平台的深度集成,以及针对不同细胞类型(尤其是更难操作的原代细胞、悬浮细胞)的协议优化。此外,移植后的长期功能性、免疫原性等问题也需在更复杂的模型中进行评估。
尽管前景广阔,我们必须冷静看待其当前的局限性: 融合效率尚不理想:在移植实验中,线粒体成功融合的比例仍有提升空间。这可能受到受体细胞自噬清除、内外源线粒体融合屏障等因素影响。未来可能需要结合药物(如促进融合的M1分子)或基因手段来改善融合效率。 探针尺寸的“双刃剑”:更小的探针侵入性更低,但电化学信号更弱,介电泳力也更小。需要在灵敏度、作用力和对细胞的干扰之间取得最佳平衡。目前的探针尺寸(~100 nm)针对线粒体(~0.3-1 μm)是合适的,但对于更小的细胞器可能面临挑战。 样本量的限制:单次提取的线粒体数量有限,目前仅能满足qPCR等分析。要对接更全面的单细胞多组学,需要开发超低输入量的样本制备技术,或实现连续、多次提取与累积。 系统的复杂性与成本:该平台整合了精密微加工、机器人控制、电化学检测、深度学习等多学科尖端技术,其复杂性和成本是目前广泛推广的障碍。 这项研究与其说是一项立即可以上市的产品,不如说是一个强大的原则性验证和平台性工具。它清晰地展示了一条绕过传统技术瓶颈的道路,为在生命最基本的单元内进行精准工程操作提供了全新的范式。正如显微镜的发明打开了细胞生物学的大门一样,此类“细胞内手术机器人”的成熟,或许将为我们打开一扇窥视并干预细胞内部运作奥秘的新大门。
Yanmei Ma et al. ,Label-free robotic mitochondrial biopsy.Sci. Adv.11,eadx4289(2025).DOI:10.1126/sciadv.adx4289
END 撰文 | 郝娅婷 编辑 | 吴苡齐 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊, 参与线上线下交流活动
推荐阅读
Nature Medicine | 仅凭一晚睡眠,预测130种疾病!斯坦福大学“睡眠AI”突破,是否颠覆了疾病预防体系?
Nature Machine Intelligence | 清华大学团队开发基于统一扩散Transformer框架的多模态心血管信号生成模型
点击关注医工学人

本篇文章来源于微信公众号: 医工学人