星标“医工学人”,第一时间获取医工交叉领域新闻动态~

长久以来,癌症化疗如同一场伤敌一千、自损八百的残酷内战。2025年10月29日,《Nature》报道一篇题为“How nanobots are accelerating cancer-targeting therapies”(纳米机器人如何加速癌症靶向治疗)的文章,一场源于纳米尺度的静默革命正试图终结这一切。研究者不再满足于制造更高效的“毒药”,而是致力于打造智能的“特种运输队”——纳米机器人。它们能利用磁场在血管中精准导航,甚至能感知肿瘤微环境的独特“信号”并自主激活“武器”。尽管尚未进入人体临床试验,但这些肉眼不可见的机器已在动物实验中展现出颠覆传统治疗范式的潜力:不是“淹没”全身,而是“渗透”敌后,进行一场外科手术式精确打击。

癌症治疗的“魔法子弹”梦想已延续百年,但现实却始终骨感。传统化疗药物在血液循环中“随波逐流”,依靠有限的增强渗透与滞留效应被动积累在肿瘤组织。这导致仅有约0.7%的给药剂量能最终作用于肿瘤,效率极低。绝大多数药物在全身“流浪”,攻击快速分裂的正常细胞,引发严重的脱发、骨髓抑制和恶心等副作用。 即便近年来兴起的靶向药物和抗体偶联药物,也大多依赖于肿瘤细胞表面的特异性标志物。然而,实体瘤内部异质性高、靶点表达不均,且狡猾的癌细胞易产生耐药性。更重要的是,现有递送方式难以突破肿瘤致密的细胞外基质和高压的间质液,药物渗透深度严重不足,无法根除深处的肿瘤细胞,成为复发和转移的温床。 简言之,当前的困境是:药物缺乏抵达复杂、深层肿瘤病灶的“自动驾驶”能力,也缺乏只在病变部位起效的“智能开关”。我们需要的不是更强大的“炮弹”,而是更聪明、更精准的“制导系统”。
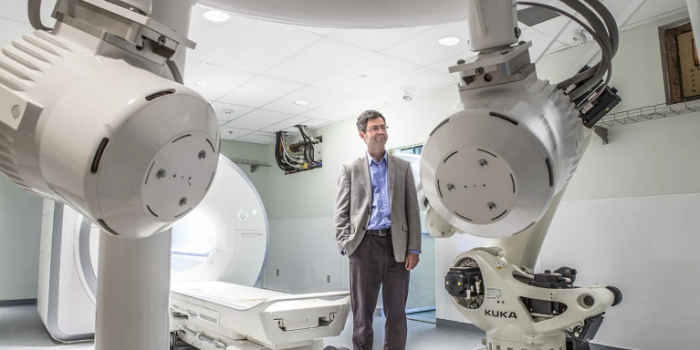
纳米机器人技术在癌症的识别与诊断领域持续推进,其效果已不逊于当前常规手段。来自马里兰州巴尔的摩约翰斯·霍普金斯大学的跨学科科学家戴维·格拉西亚斯(David Gracias)研发出一种微型夹持器,可用于对人体中难以抵达的部位实施活检。该金属夹持器仿人手结构设计,依靠一层起弹簧作用的薄蜡膜维持张开;一旦蜡质软化,夹持器便会强力闭合。目前,格拉西亚斯已在猪模型上完成了单腹膜癌与胃肠道癌的活检实验,并指出所得样本完全满足现有临床检测的诊断需求。 纳米机器人并非传统意义上的机械装置,而是由DNA、磁性纳米颗粒或聚合物等生物相容性材料构建的分子尺度“智能体”。其革命性在于,它们整合了 “导航”、“感知”与“执行” 三大核心功能,将被动给药变为主动治疗。 如《自然》文章所述,以加拿大蒙特利尔理工学院Sylvain Martel教授为代表的研究者,正在开发一种由核磁共振(MRI)设备磁场引导的纳米机器人集群。这相当于为纳米机器人装上了外部遥控的“方向盘”和“地图”。MRI不仅能实时成像,其均匀、可控的磁场还能引导负载药物的磁性纳米机器人群体,克服血流冲击,在如肝脏动脉网络般复杂的分支血管中穿行,最终抵达目标区域。团队甚至通过调整动物体位来利用重力辅助导航,展现了极高的控制策略灵活性。 更前沿的方向是让纳米机器人具备内在智能。瑞典卡罗林斯卡学院的研究是绝佳范例。他们利用“DNA折纸”技术,构建了一种在正常生理环境下保持闭合、无害的纳米结构。其内部隐藏着能诱导细胞凋亡的“致命武器”——特定肽链。 其创新开关在于:肿瘤组织因异常代谢通常呈弱酸性(pH约6.5-7.0)。一旦纳米机器人到达此处,酸性环境会触发其DNA结构展开,像“开花”一样暴露出细胞毒性配体,从而精准杀死癌细胞,同时在健康组织(pH 7.4)中保持惰性。这相当于让肿瘤自己交出“钥匙”,启动了锁定在机器人内部的“武器”。 未来的纳米机器人正朝着功能集成化发展。例如,中国国家纳米科学中心团队曾开发出装载凝血酶的DNA纳米机器人,它能特异性结合肿瘤血管,诱发血栓形成以“饿死”肿瘤。香港中文大学(深圳)的俞江帆教授团队则在探索“纳米机器人集群”,它们像蜂群一样协同工作,执行如肺部靶向给药、血管网络主动测绘等更复杂的任务。
蒙特利尔理工学院的Sylvain Martel利用磁共振成像扫描仪引导猪体内的药物纳米机器人。图片来源:Dumitru Loghin。 这些看似科幻的概念,已在动物实验中取得了令人振奋的实证数据,勾勒出未来临床应用的雏形。 这些实验共同传递出一个信号:纳米机器人的核心价值已不仅是提高药物在肿瘤的“浓度”,而是通过精准的时空控制,最大化治疗的“效率与特异性”,同时将系统性损伤降至最低。 如果这项技术最终走向成熟,它所引发的将是癌症治疗范式的根本性转移。 治疗模式重塑:从“全身暴露、被动扩散”到“局部聚焦、主动渗透”。化疗可能从令人畏惧的“毒性疗法”转变为精准的“局部手术”。 药物开发新路径:制药公司可以开发效力更强但此前因毒性太大而无法全身使用的药物分子,交由纳米机器人精准递送。 诊疗一体化:纳米机器人可同时负载造影剂和治疗剂,实现“看到哪里,打到哪里”,实时监控治疗效果。 目前,大多数尖端纳米机器人研究仍处于临床前动物实验阶段,尚未进入人体临床试验。根据行业评估,该领域技术成熟度正处于从实验室向临床转化的关键阶段。未来3-5年,我们有望看到首批基于相对简单原理(如磁性导航或单一环境响应)的纳米治疗设备进入早期临床研究。 长远来看,纳米机器人代表的是一种可编程的精准医学平台。一旦平台技术成熟,通过更换其表面的靶向分子或内部载荷,理论上可以用于治疗多种疾病,如精准输送溶栓药物清除血栓、突破血脑屏障治疗阿尔茨海默病、或定点调节免疫细胞治疗自身免疫疾病。这正如中国科学院院士赵宇亮所展望的:未来,纳米机器人可能让许多大型侵入性外科手术成为历史。 尽管前景广阔,但我们必须保持清醒。通往临床应用的道路上布满荆棘: 结语:纳米机器人治疗癌症的故事,是一群科学家试图在人体最微小的战场上,重写战争规则的史诗。它从一个简单的想法出发——“如果药物能自己去该去的地方,只在需要的时候工作呢?” ——如今已演变为一场融合了纳米技术、分子生物学、医学影像学和机器人学的跨界盛宴。虽然前路漫漫,挑战重重,但它无疑为我们照亮了一条通往更精准、更人性化癌症治疗的未来之路。这场静默的革命,正在微观世界里澎湃涌动。
Heidt, A. How nanobots are accelerating cancer-targeting therapies. Nature 646, S39–S41 (2025). DOI: https://doi.org/10.1038/d41586-025-03480-z
END 撰文 | 郝娅婷 排版 | 周宇茜 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊, 参与线上线下交流活动
推荐阅读
Nature biotechnology | 斯坦福大学发表研究:颅内碎屑的超声清除可减少炎症并改善出血性中风模型的预后

点击关注医工学人
本篇文章来源于微信公众号: 医工学人