星标“医工学人”,第一时间获取医工交叉领域新闻动态~

眼科手术被誉为外科领域的“禁区”——操作空间仅硬币大小,精度要求却达到微米级,人手自然的颤抖都会成为致命误差。2026年1月14日,一项发表于《科学机器人》的研究带来了突破:由中国科学院自动化研究所、北京理工大学及北京协和医院联合开发的ARISE系统,首次实现了全自主的视网膜下与视网膜静脉注射。在离体和活体动物实验中,该机器人以100%的成功率完成了超过100次手术,定位精度较人手提升79.87%。这不仅是一次技术验证,更可能开启显微外科自动化的新纪元。
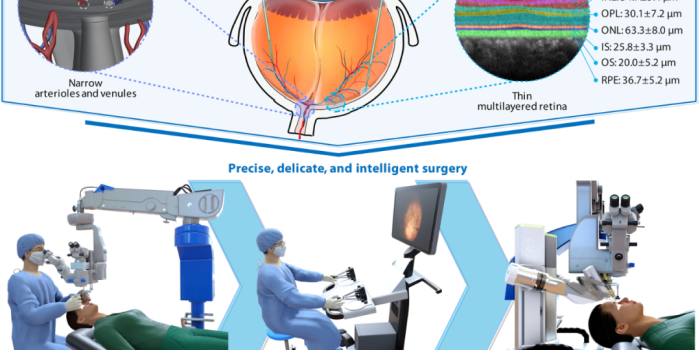
在眼球后极那片指甲盖大小的区域里,人类视觉的奥秘被封装在不足300微米厚的视网膜组织中。这里,视网膜色素上皮层仅25微米厚,视网膜静脉的管径通常小于150微米——比头发丝还细。当医生试图将基因治疗药物精准注入视网膜下间隙,或穿刺阻塞的静脉进行溶栓时,他们面临的是一个物理极限的拷问:人手固有的生理性颤抖(通常超过100微米),足以让最稳的外科医生越界。 图 1. 眼内结构及眼内手术技术的演变。眼内结构复杂,需要精确、精细且智能的手术方法。随着治疗手段的进步,手动及遥操作机器人手术已无法完全满足临床需求。自主机器人手术可提高手术一致性、改善患者安全、减少对人力的依赖并降低人为错误,从而支持更安全、更可靠的治疗。RNFL,视网膜神经纤维层;GCL,神经节细胞层;IPL,内丛状层;INL,内核层;OPL,外丛状层;ONL,外核层;IS,内节;OS,外节;RPE,视网膜色素上皮;DOF,自由度。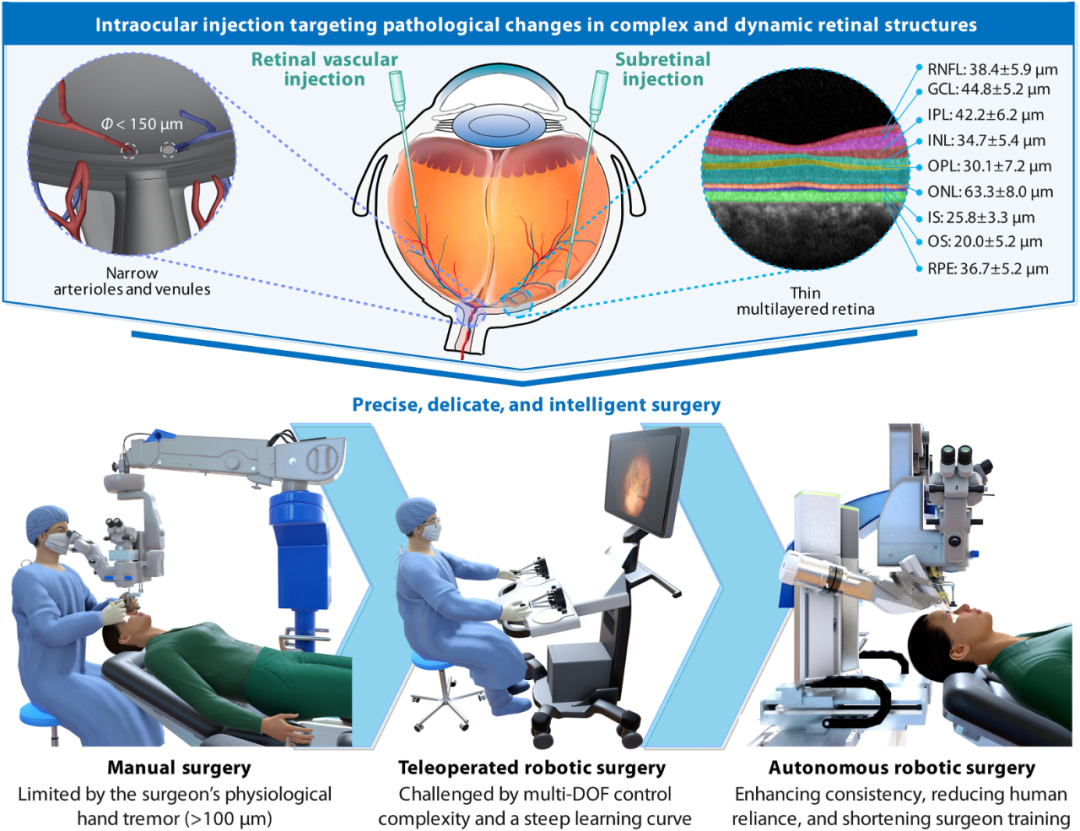
过去十年,眼科手术机器人(如PRECEYES、SHER等系统)的出现,通过震颤过滤和运动缩放技术,将医生从生理限制中部分解放出来。然而,现有方案仍停留在遥操作阶段——医生通过操纵杆或主从控制台指挥器械,术中的关键决策(“往哪扎”、“扎多深”)仍依赖人脑的实时判断。
这带来了三个无法回避的困境:
感知盲区:手术显微镜的视野有限,而OCT(光学相干断层扫描)虽能看清层次,却视野狭窄。医生如同在管中窥豹,难以在全局视野中精准定位器械与靶点的空间关系。
人因误差:不同医生的手术习惯、经验差异会导致手术结果的不一致性;即便是同一位医生,疲劳和应激状态下的操作也会产生波动。
学习曲线陡峭:掌握视网膜静脉穿刺等高级技巧需要数年训练,且难以规模化复制。
“自然颤抖、肌肉抽动和低频漂移会导致超过100微米的偏差,手术所需的精度已超越手动控制的生理极限。”——论文原文
正是这些痛点,让“自主手术”从概念走向刚需:如果手术的核心步骤能够像自动驾驶一样,由机器自主感知、规划和执行,是否可能突破人手的极限,实现真正标准化、无差别的精准医疗?
ARISE(Autonomous Robotic System for Intraocular Surgery)的核心突破,可以概括为三个关键词:“看全”、“想准”、“控稳”。它通过一套多模态感知与融合架构,解决了自主手术最核心的问题——在动态、狭小的眼内空间中,如何知道自己在哪里,要去哪里,以及怎么安全地过去。
| 维度 | 传统遥操作手术 | ARISE自主手术系统 | 技术跃迁 |
| 全局感知 | 依赖显微镜局部视野,需医生脑补空间关系 | 多视角空间融合,构建动态3D眼内地图 | 从“管中窥豹”到“上帝视角” |
| 器械定位 | 依靠视觉估算深度,或依赖单一OCT轴向信息 | 三级级联定位(RCM辅助定位 → 末端轮廓定位 → iOCT相对定位),多传感器加权融合 | 从“像素级估计”到“微米级解算” |
| 路径规划 | 医生手动操控,依赖经验避障 | 多约束目标优化,实时规划照明与穿刺路径 | 从“人肉避障”到“算法博弈” |
| 安全机制 | 依赖医生反应速度 | 力-位-像混合监控,毫秒级风险预警与主动回撤 | 从“被动纠错”到“主动防御” |
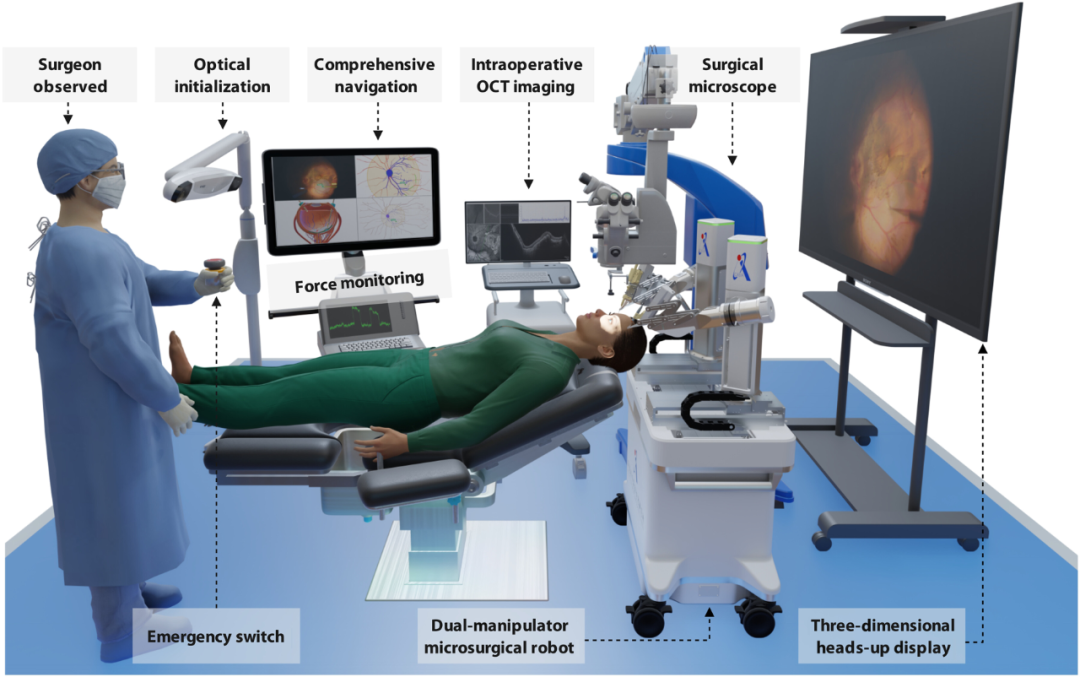
图 2. 用于眼内手术的自主机器人系统(ARISE)。一个高精度、灵巧的双臂显微手术机器人,在术中三维导航的引导下执行自主视网膜注射,整个手术过程在人力监控的力-位-影像混合安全控制下进行。
多视角空间融合:让机器“看懂”眼底
传统术中导航的痛点在于:显微镜视野宽但看不清层次(2D),OCT看得清层次但视野窄(仅4mm×4mm)。ARISE的解法是将两者动态对齐,并融合术前数据。
研究团队提出了一个交互式空间对齐模块:通过PRTransUNet分割算法提取眼底血管、视网膜层等微特征,利用局部-全局空间变换器,将术前OCT的体积数据、术前眼底彩照与术中显微镜图像、术中OCT B-scan进行实时配准。更关键的是,系统还引入了一个跨模态偏移预测模块,实时跟踪眼球旋转、器械遮挡导致的图像漂移,并以14Hz的频率更新局部动态地图(12mm×9mm×9mm),在全眼范围内实现了4.7μm(视野内)至20μm(视野外)的横向分辨率和6μm的轴向分辨率。
准则加权多传感器融合:微米级定位的“裁判系统”
在自主手术中,单一传感器总有弱点:光学追踪易被遮挡,机器人运动学会累积误差,OCT视野有限。ARISE的巧妙之处在于为这些传感器建立了一套动态评分系统。
系统从四个维度——可靠性(R,基于分割置信度)、有效性(E,基于历史误差分布)、实时性(T,基于采样频率)、一致性(C,基于马氏距离)——对多源数据进行加权。权重通过“最优最劣法”(Best-Worst Method)实时求解。这套机制确保了在不同手术阶段,系统总能“听信”最靠谱的那个传感器。
例如:当器械在显微镜视野外时,系统依赖RCM辅助的运动学定位(精度100μm);进入后极部后,切换为基于阴影轮廓的末端定位(精度<10μm);贴近视网膜时,再由iOCT A-scan进行微米级精调(精度5.3μm)。三级定位无缝衔接,实现了从巩膜切口到视网膜表面的全路径高精度追踪。
多约束目标优化:像“自动驾驶”一样规划路径
自主手术的路径规划远比自动驾驶复杂——不仅要有RCM运动约束(器械必须绕巩膜切口旋转,不能撕裂巩膜),还要保证照明光纤始终照亮靶点,同时避开视网膜上的敏感区域。
ARISE将这些问题建模为一个多目标优化问题:用椭球体拟合障碍边界,基于快速探索随机树(RRT)算法在约束空间中搜索最优路径。最终实现的是注射针与照明光纤的协同运动——无论针尖走到哪里,光都能跟上,确保术中视野始终明亮。
论文的实验设计堪称“阶梯式”验证:从硅胶眼模型(眼球phantom),到离体猪眼,再到活体动物(兔和猪),层层递进。关键数据如下: 图 3. 离体猪眼球上自主注射的结果。所有实验均在半静态眼内条件下进行,其特征是在局部组织形变、玻璃体扰动,但不存在呼吸或血流等生理性运动。(A) 实验装置。 (B) 视网膜下及视网膜静脉注射的结果。 (C) 自主工作流程各阶段所需时间。 (D) 定位误差、穿刺深度及注射前后 iOCT 图像对比。 图 4. 活体动物眼球上自主注射的结果。所有实验均在完全动态的眼内条件下进行,包括呼吸和血流等生理性运动。(A) 实验装置。(B) 视网膜下及视网膜静脉注射的结果。(C) 自主工作流程各阶段所需时间。(D) 定位误差、穿刺深度及注射前后 iOCT 图像对比。 成功率:全模式100% 离体猪眼:视网膜下注射(n=20)、视网膜中央静脉注射(CRV,n=20)、视网膜分支静脉注射(BRV,n=20)——成功率100% 活体动物眼:三类注射各16次——成功率100% 注:成功标准为单次穿刺到位,且无出血、视网膜撕裂等并发症。 定位精度:远超人手极限 与手动手术相比:定位误差降低79.87% 与遥操作机器人手术相比:定位误差降低54.61% 活体环境下平均定位误差:x轴16.6μm,y轴12.7μm,z轴9.3μm 最差情况:BRV注射时x轴最大误差53.17μm,仍显著低于人手平均误差(58.17μm)。 时间效率:可接受范围内的“慢即是快” 自主手术从目标定位到注射完成的平均时长:79.16秒 手动手术:22.48秒 遥操作:53.78秒 尽管自主手术耗时更长,但研究指出,术中玻璃体切割等步骤才是耗时大头(约184秒),自主注射增加的1分钟内耗时在临床可接受范围内。更重要的是,稳定性的提升——从运动轨迹图可清晰看出,自主手术的针尖运动曲线平滑,而手动和遥操作均存在明显抖动。 安全性验证 术中及术后即刻:无出血、视网膜撕裂、脱离等并发症 术后1周随访:无视力障碍、眼浑浊或异常行为,验证了干预的微创性。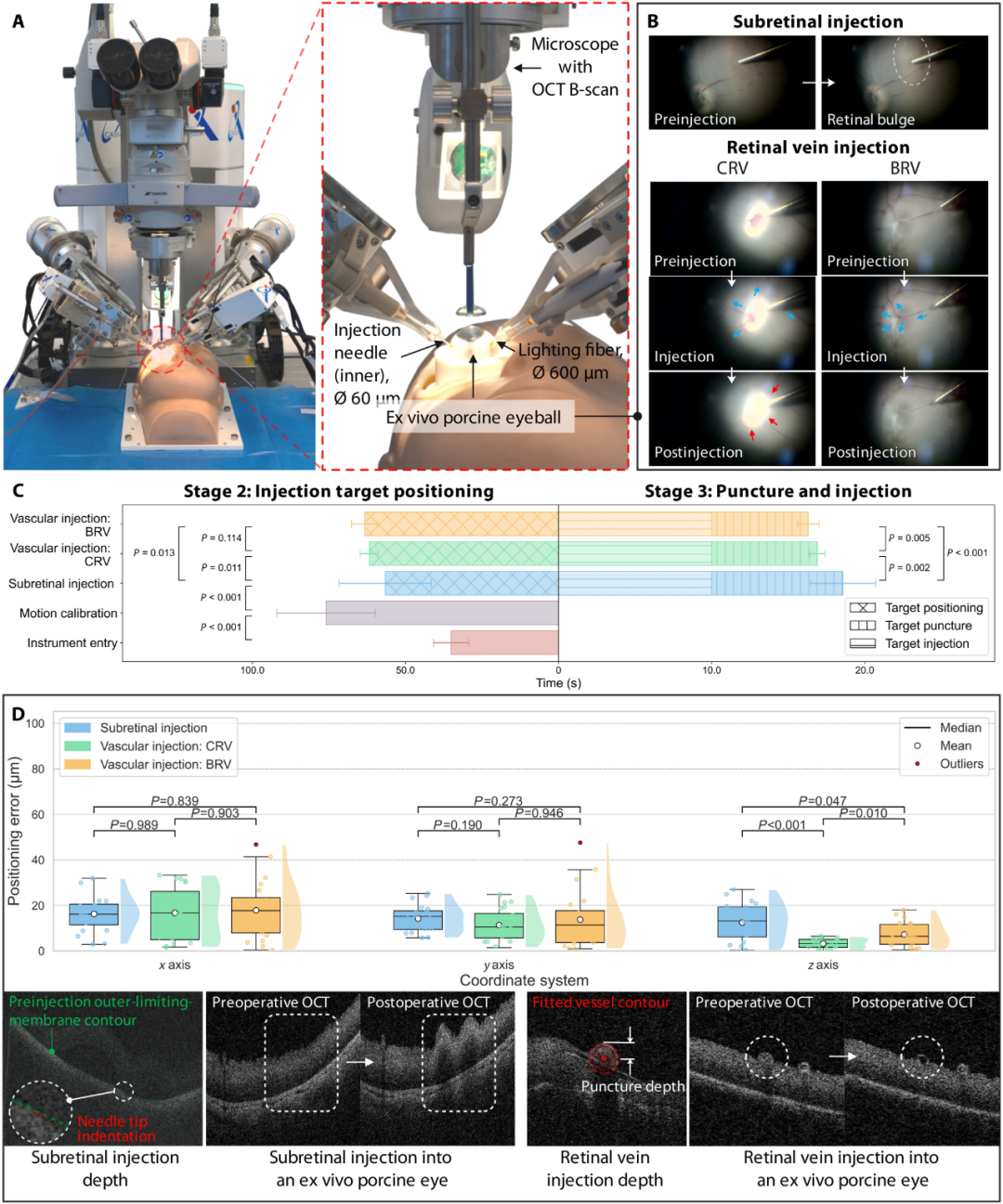
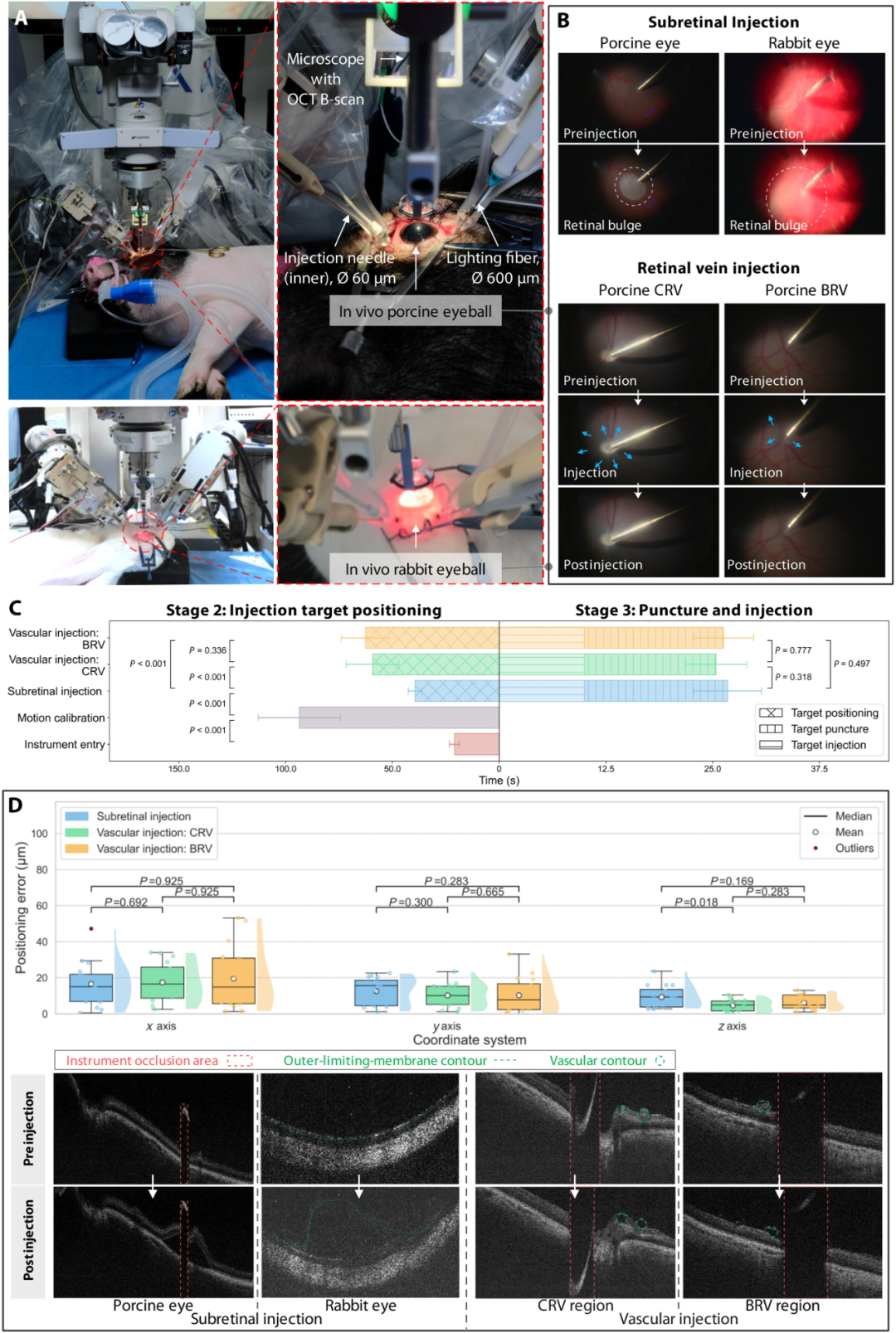
这项研究的价值不仅在于“成功做了手术”,而在于它证明了全自主显微外科在临床环境中的可行性。如果这项技术走向成熟,将带来三重变革: 1. 手术均质化:自主系统可以消除不同医生、不同手术日之间的操作差异,让偏远地区的患者也能享受到“顶级专家级别”的手术精度。 2. 治疗规模化:当前制约基因疗法眼科应用的一大瓶颈是给药难度——视网膜下注射需要极高技巧,能胜任的医生有限。自主机器人有望将这一操作标准化,从而支撑大规模临床试验和商业化落地。 3. 手术可及性:论文特别提到,自主手术可“在偏远或极端环境中实现”。这指向了远程医疗的终极形态——未来,一线城市的医生只需划定靶点,机器人即可在基层医院自主完成核心操作。 从商业视角看,眼科手术机器人赛道正处于爆发前夜。目前,仅PRECEYES和KU Leuven系统进入早期人体临床评价阶段,且均为遥操作模式。ARISE的自主能力,意味着技术代差——若能顺利通过临床审批,它将占据下一代手术机器人的制高点。
作为一份严谨的科技评论,我们必须指出,从论文到手术室,ARISE仍有四重关卡需要跨越: 1. 病理模型的缺失 目前所有实验均在健康动物眼球上进行,未模拟疾病状态(如糖尿病视网膜病变、黄斑水肿等)。病变组织的力学特性、解剖结构可能完全不同,自主算法能否泛化,仍是未知数。 2. 组织变形与生理运动 尽管实验在活体动物上进行,且存在呼吸、血流等生理运动,但论文承认,更复杂的组织变形(如穿刺时的弹性回弹、侧向位移)尚未被完全建模。对于更大尺寸的器械(如镊子、视网膜刀),变形控制将是更大挑战。 3. 药物反流与长期疗效 论文未量化药物注射后的反流情况,也未评估长期疗效。对于基因治疗而言,给药剂量和位置的精度的最终评判标准是治疗效果,而不仅仅是术中形态学改变。 4. 监管与伦理的真空地带 “自主决策”在医疗领域始终是敏感话题。当机器人拥有最终控制权时,责任主体如何界定?目前,ISO 13485等标准尚未覆盖完全自主手术系统。ARISE团队计划采取“模块化分步验证”策略,在现有遥操作系统中逐步植入自主功能,但这仍是监管机构的未知领域。 “尽管自主系统拓展了现有监管范式,但仍需在可解释性、可审计性和伦理问责方面投入大量努力,以确保临床和监管的接受度。”——论文原文 ARISE的出现,不是宣告外科医生的终结,而是敲响了显微外科新纪元的大门。当机器能稳稳握住那支比发丝还细的针,人类医生的角色将从“操作者”真正转向“决策者”和“监督者”——而这,或许才是医疗自动化的终极意义。
Gui-Bin Bian et al. ,Autonomous robotic intraocular surgery for targeted retinal injections.Sci. END 撰文 | 郝娅婷 排版 | 周宇茜 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊, 参与线上线下交流活动
推荐阅读
Robot.11,eadx7359(2026).DOI:10.1126/scirobotics.adx7359
点击关注医工学人 直播预告

本篇文章来源于微信公众号: 医工学人