星标“医工学人”,第一时间获取医工交叉领域新闻动态~

斜视影响着全球约4%的儿童,但传统诊断依赖繁琐的仪器和医生主观判断,儿童依从性差、误差大。2026年1月28日,清华大学与首都医科大学附属北京同仁医院团队在《科学进展》发表研究,研发了一款厚度仅60微米、可贴附于眼睑的柔性传感阵列“Eyelectronics”,通过测量眼球运动时的眼睑形变,结合AI算法,实现了96.6%的方向识别准确率和1.2°的角度测量精度。这项技术将生物力学传感与数字诊断深度融合,有望将斜视诊疗从“经验驱动”推向“数据驱动”的新范式。
如果你曾带孩子去看过斜视,可能会对这样的场景印象深刻:医生关掉诊室的灯,让孩子戴上红绿眼镜,盯着屏幕上移动的光点,然后问:“告诉我,绿光和红光重合了吗?”孩子困惑地摇头,医生皱着眉调整仪器,整个过程漫长而枯燥。
斜视,这个影响全球2%-4%儿童的常见眼病,其临床诊断至今仍停留在“主观问答”时代。目前的“金标准”Hess屏测试,需要患者在九个凝视方向上判断红绿光点是否重合——这要求患者具备良好的理解能力和配合度。对于年幼的儿童,这几乎是“不可能的任务”。
更致命的是现有技术的结构性缺陷:
|
技术手段 |
局限性 |
核心痛点 |
|
棱镜遮盖测试 |
仅能测量单一方向斜视角 |
无法评估多条眼外肌的综合影响 |
|
Hess屏/Lancaster屏测试 |
依赖患者主观反馈,设备笨重 |
儿童配合度差,结果重复性低 |
|
眼动追踪摄像头 |
需频繁校准,易受环境光干扰 |
摄像头与头部相对位移导致误差 |
|
眼电图(EOG) |
信号噪声大,电极易漂移 |
长期佩戴不舒适,稳定性差 |
“准确诊断需要医生的经验、患者的配合和笨重的仪器三者的完美协调,”论文通讯作者冯雪教授指出,“任何一个环节出问题,都可能导致高达20%-50%的斜视手术二次修正率。”在这样的背景下,临床亟需一种客观、量化、无感的一站式诊断方案。
清华大学团队给出的解决方案,乍听有些反直觉:我们不直接测眼球,我们测眼睑。
这一思路的生物学基础在于:眼睑与眼球之间存在紧密的机械耦合。当眼球转动时,上眼睑会发生相应的拉伸或压缩形变。如果能精确捕捉这种形变,就能反向解码眼球的运动轨迹。
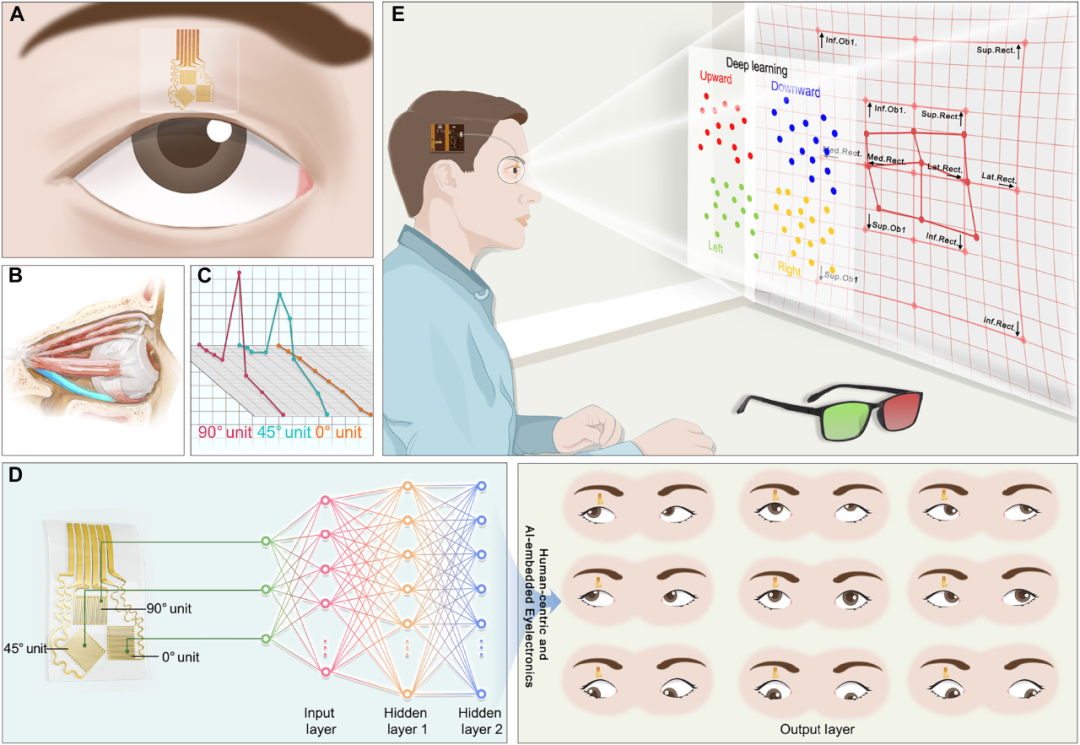
图 1. 通过集成人工智能的类皮肤可穿戴眼部电子器件实现一站式斜视数字诊断的示意图。
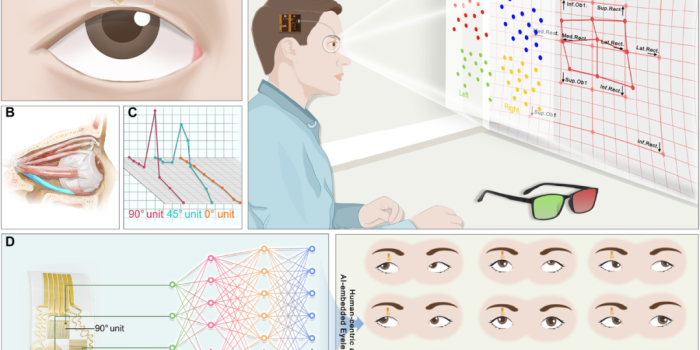
(A) 通过形态工程学设计,将 HMS 阵列共形贴附于上眼睑,用于测量眼球运动引起的眼睑应变。(B) 下直肌麻痹(以蓝色标记)导致眼球向上偏斜,引起眼睑变形。(C) 按 0°/45°/90° 角度排列的测量单元的典型信号示例。(D) 通过生理学知识驱动的端到端 AI 算法,可实现一站式斜视数字诊断。(E) 眼部电子器件包含眼戴式 HMS 阵列、头戴式柔性电路和一个支持蓝牙的设备。结合 Hess 屏测试,它可以实现一个无线、舒适、生物相容性好的—站式数字解决方案,用于同时进行斜视测量和眼外肌功能评估。
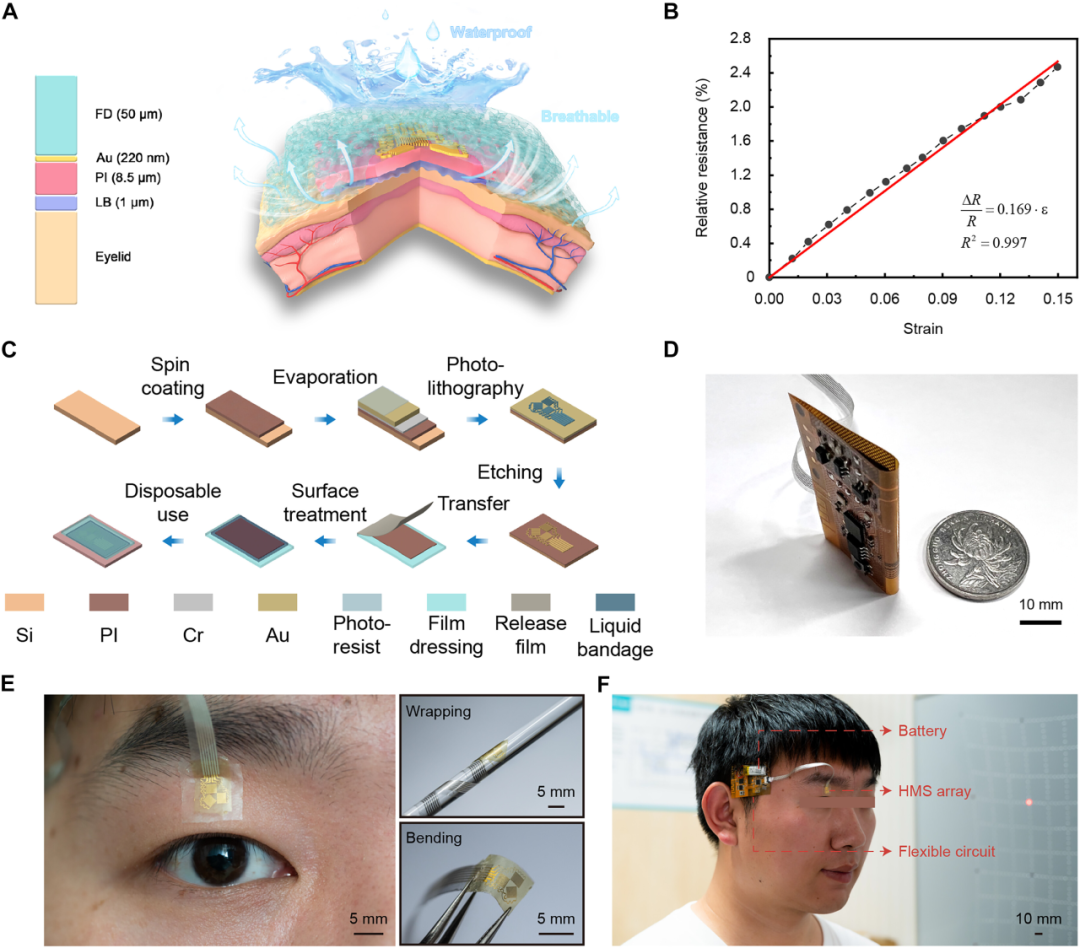
图 2. 眼部电子器件的设计。
(A) HMS 阵列的示意图,带有展示其结构的剖视图,自上而下依次由薄膜敷料 (FD)、应变传感部分和一层液体绷带 (LB) 组成。应变传感部分包含一个金属传感部分(Au 层)和一个 PI 层。这种结构使得该阵列能像表皮纹身贴片一样紧密贴附于眼睑,同时不会限制眼睑变形。通过敷料和液体绷带的混合固定方式,它可以轻松移除。这也确保了阵列的防水性和透气性。(B) 三个单元的相对电阻变化平均值与施加应变之间的线性关系表明,其灵敏度为 0.169,线性拟合优度为 0.997。(C) HMS 阵列的制造流程图,可实现批量生产和作为一次性医疗耗材使用。(D) 可折叠 180° 的柔性信号处理电路与一枚一元硬币对比,显示其紧凑的尺寸。比例尺,10 mm。(E) HMS 阵列的超薄柔性设计使其能共形贴附于眼睑。阵列的光学图像(左)、缠绕在外径 6 mm 的塑料管上(右上)以及处于弯曲状态(右下)。比例尺,5 mm。(F) 贴附在受试者上的类皮肤眼部电子器件。比例尺,10 mm。
研究团队开发的“Eyelectronics”核心是一个多层结构的多向应变传感阵列:
封装层:50μm厚的Opsite透明敷料,防水、透气、低致敏
传感层:220nm厚的金(Au)应变栅格,8.5μm聚酰亚胺(PI)缓冲层
粘附层:约1μm厚的液体绷带喷雾,实现与眼睑褶皱的无缝贴合
整个系统总厚度仅约60μm,可以像纹身贴纸一样贴附于上眼睑。最精妙的设计在于0°/45°/90°三个方向的应变单元——0°单元捕捉水平运动(左/右),90°单元捕捉垂直运动(上/下),45°单元提供冗余通道提升精度。
“这相当于在眼皮上贴了一个微型‘莫尔斯电码发射器’,眼球的每一次转动都会引发独特的电信号模式。”论文第一作者杨勇解释道。
但有一个根本问题:眼睑形变与眼球运动之间的关系并非线性,且受个体差异(如单/双眼皮、年龄、皮肤弹性)影响巨大。如何建立可靠的理论基础?
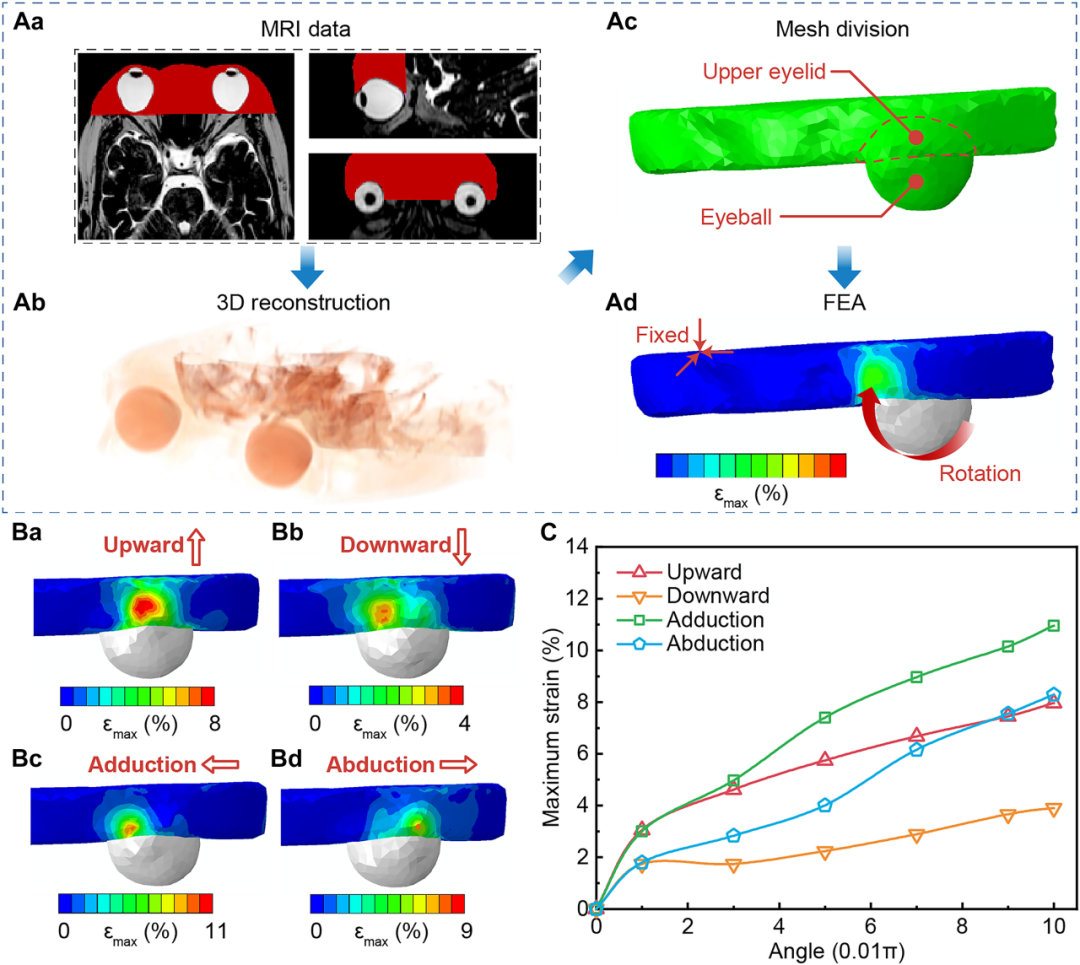
图 3. 眼球运动过程中上眼睑应变变化的有限元分析。
(A) 有限元分析方案。首先,获取人头部的 MRI 数据用于有限元模型重建。左侧、右上和右下分别是红色区域 (Aa) 所代表眼部区域的俯视图、左视图和正视图。其次,根据 MRI 数据对颅骨、眼球和上眼睑进行三维重建 (Ab)。第三,对感兴趣区域进行网格划分,并适当细化上眼睑的网格密度 (Ac)。最后,眼球运动引起眼睑上的应变变化 (Ad)。(B) 四个方向眼球运动时上眼睑的应变场:向上 (Ba)、向下 (Bb)、内收 (Bc) 和外展 (Bd)。(C) 有限元分析结果显示,眼球运动过程中眼睑应变的最大值随眼球运动角度的增加而增加,从理论上验证了通过测量眼睑应变进行眼动追踪原理的正确性。
团队采用了“建模-仿真-现实”(Model2Sim2Real)的三步策略:
-
MRI建模:基于真实患者的头部MRI图像,三维重建眼球、眼睑和颅骨结构
-
有限元分析:模拟眼球转动时眼睑的应变场分布,最大应变不超过11%
-
数字图像相关验证:在受试者眼睑喷涂无毒散斑图案,用高速相机验证实际应变
这一跨尺度的生物力学建模,不仅为传感器布局提供了理论依据(贴在眼睑下缘中部),也为后续AI算法提供了先验知识约束,避免算法陷入“唯数据论”的过拟合陷阱。
有了高质量的传感数据,下一步是解码。团队没有套用现成的深度学习模型,而是针对眼动信号特性设计了InceptionTime-Tiny算法:
输入:3个原始通道经“通道差分+时间差分”扩展为10通道
核心:两层级联的Inception模块,包含3/7/17三种尺度的卷积核
输出:分类头识别运动方向(96.6%准确率)+ 回归头预测运动角度(MAE < 1.2°)
轻量化:总参数量65,156,模型大小仅254kB,可部署于蓝牙设备端
与传统的KNN-DTW方法(78.4%准确率)相比,这一算法将八方向分类准确率提升至96.5%,且对眨眼、表情等面部动作的误识别率为零。
数据说话:三项关键验证
-
体外验证:与数字图像相关(DIC)方法对比,传感器信号波形与DIC/FEM仿真结果高度一致,验证了测量原理的可靠性。
-
算法性能:在5000次眼动数据上训练测试,四方向分类准确率96.6%,角度回归误差<1.2°,达到临床可用标准。
-
临床试验:7名受试者(6名斜视患者+1名健康对照)的Hess屏测试对比显示,与临床金标准的组内相关系数(ICC)达0.978,Bland-Altman分析显示水平方向偏差均值仅0.47°。
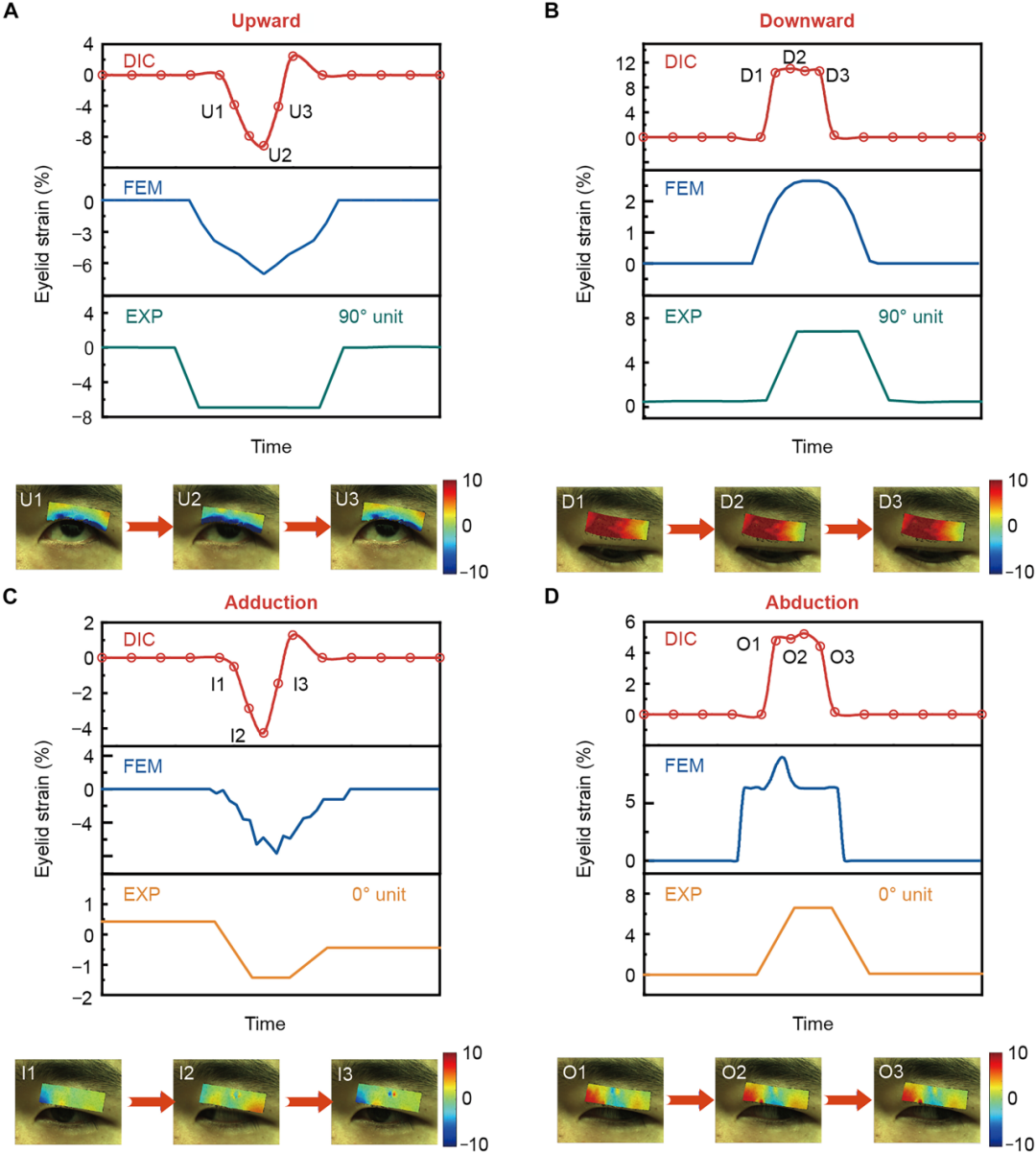
图4:通过 DIC 进行眼睑应变测量,并将其信号特征与通过 FEA 和 HMS 阵列测量的结果进行比较。
(A 和 B) 上侧图示为当眼球向上和向下看时,通过 DIC(红线)、FEM(蓝线)和 HMS 阵列的 90° 单元(绿线)获得的眼睑垂直应变变化。下侧图示为通过 DIC 测量的应变场变化图像。(C 和 D) 上侧图示为当眼球进行内收和外展运动时,通过 DIC(红线)、FEM(蓝线)和 HMS 阵列的 0° 单元(橙线)获得的眼睑水平应变变化。下侧图示为通过 DIC 测量的应变场变化图像。可以看出,三种信号的波形特征一致,证明了眼部电子器件的可行性。
真实场景:覆盖测试与Hess屏的数字化
研究展示了两个临床场景的落地可能:
覆盖-去覆盖测试:通过检测内斜视患者在遮盖健眼时患眼的“外展信号”,自动识别注视眼和斜视类型
Hess屏数字化:患者只需注视屏幕上的九个光点,系统即可生成完整的Hess图,无需手持绿光笔和主观重合判断
对于右眼内直肌麻痹的患者,系统生成的Hess图清晰显示:右眼注视点范围缩小、整体外偏——这正是麻痹性斜视的典型特征。
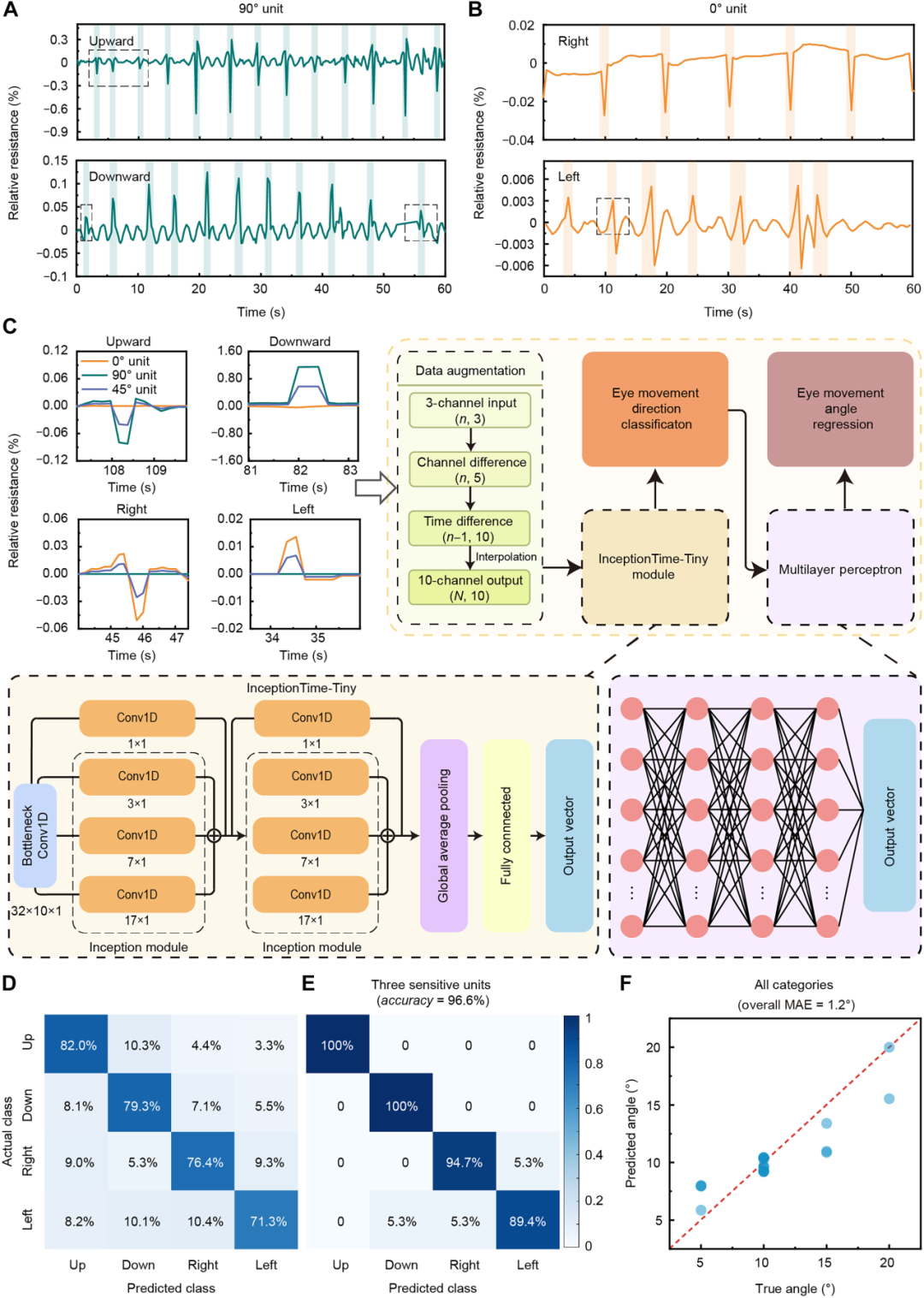
图5:通过集成 AI 的眼部电子器件实现精确眼动追踪。
(A) 向上和向下的垂直眼动及其对应的 90° 单元信号。(B) 向右和向左的水平眼动及其对应的 0° 单元信号。黑色虚线框标记的示例信号难以仅基于不同方向的测量单元和信号的极性来准确分类眼动方向。(C) InceptionTime-Tiny 算法流程图。来自 0°/45°/90° 单元的四方向眼动原始信号,在经过通道差分和时间差分处理后,输入到生理学驱动的算法中实现眼动方向分类,随后通过 MLP 网络实现角度回归。(D) 基于单个测量单元的正负信号进行眼动分类的准确率。(E) 基于 InceptionTime-Tiny 算法进行眼动分类的准确率。(F) 四个方向眼动回归的总体平均绝对误差小于 1.2°。
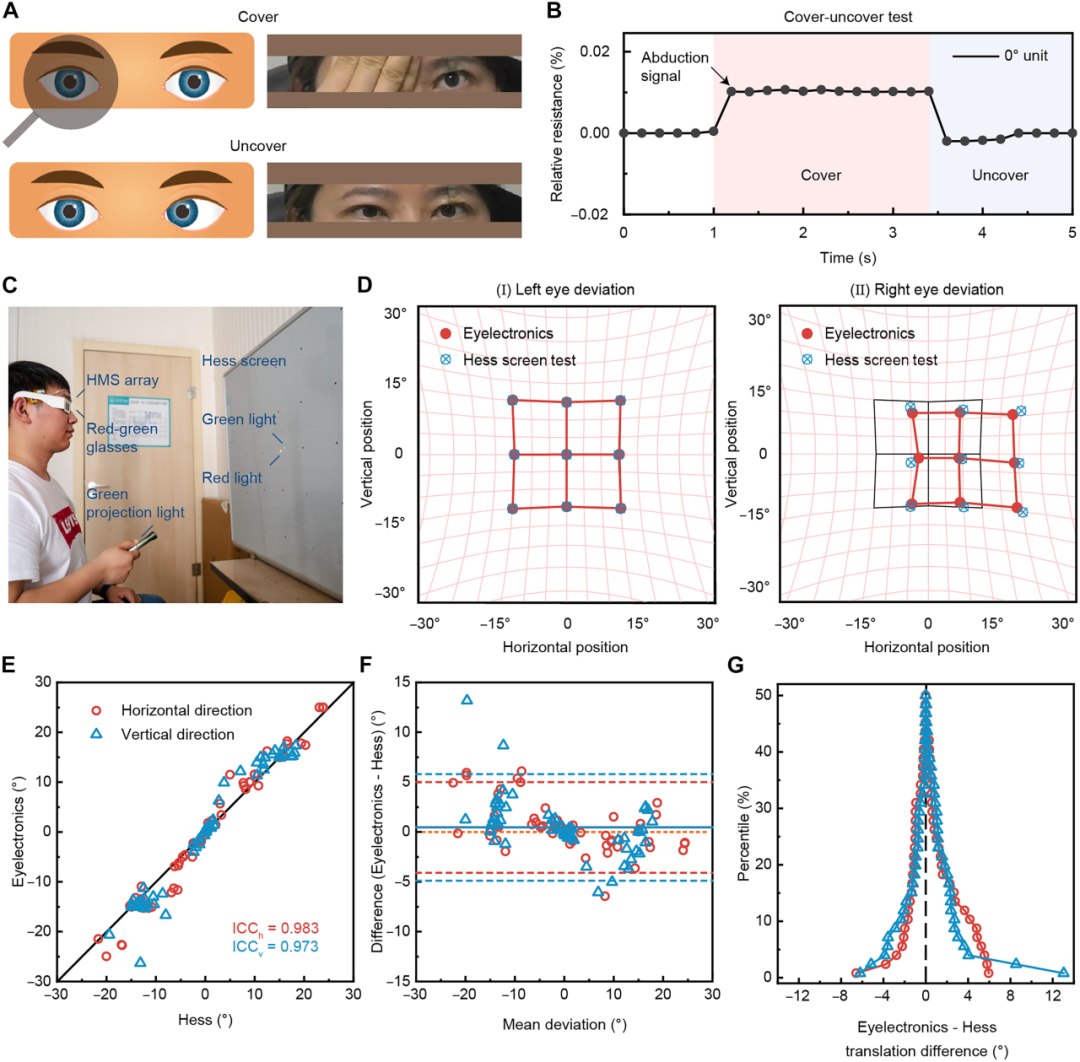
图5:使用集成 AI 的类皮肤可穿戴眼部电子器件进行一站式斜视数字诊断。
(A) 遮盖-去遮盖试验示意图及一名左眼内斜视患者的眼动照片。
(B) 使用眼部电子器件进行的遮盖-去遮盖试验结果。
(C) 使用眼部电子器件进行 Hess 屏试验的照片。
(D) 左眼(正常眼)和右眼(斜视眼)的标准 Hess 屏试验结果与使用眼部电子器件的试验结果对比。
(E) Hess 屏试验与眼部电子器件试验在全部九个主要凝视眼位上斜视度的相关性分析。全部九个水平及垂直斜视度的 ICC 分别为 0.983 和 0.973。
(F) 用于评估两种试验一致性的均值差值图。水平(0.47°,红色实线)和垂直(0.46°,蓝色实线)的平均差值均接近于零。垂直斜视度的 95% 一致性界限(蓝色虚线)宽于水平斜视度(红色虚线)。
(G) 用于说明两种试验结果间等级差异的折叠经验累积分布图。水平(红色)和垂直(蓝色)差异的中位数(峰值)均以零为中心,表明两种试验之间不存在系统性偏差。垂直峰的形态更窄,表明水平方向上的一致性略优于垂直方向。
临床意义:从“经验”到“数据”
传统的斜视诊断本质上是“黑箱”:医生看到的是患者行为反应(红绿光是否重合),推断的是眼外肌功能。而Eyelectronics第一次实现了眼外肌功能的直接量化测量。
“这对手术规划的变革是根本性的,”北京同仁医院焦永红教授表示,“我们可以根据每个眼位的实际偏差角度,精确设计肌肉缩短或后徙的量,而不是靠术中的‘手感’。”
商业化路径:一次性医疗耗材的想象空间
从工程角度看,这款传感器有几个值得关注的特质:
-
可量产:采用成熟的光刻工艺,可在硅片上批量制备
-
低成本:一次性使用设计,避免交叉感染
-
接口标准化:通过各向异性导电胶(ACF)与柔性电路板连接,实现“传感器抛弃、电路复用”
如果获批医疗器械注册证,这将是眼科检查领域第一个真正意义上的柔性可穿戴一次性耗材。
技术延伸:不止于斜视
论文最后提到,这一“Model2Sim2Real”框架可推广至其他可穿戴医疗设备的研发——通过物理电学建模+批量仿真+AI,大幅缩短医疗器械的迭代周期。此外,该系统未来可与眼外肌生物力学模型结合,实现药物疗效预测或手术效果仿真,向“数字孪生”迈进。
在展示技术潜力的同时,我们也需要正视当前版本的局限性:
样本量有限:临床试验仅纳入7名受试者,虽覆盖了常见斜视类型,但统计效力仍需更大规模多中心研究验证。
个体差异挑战:虽然AI算法通过few-shot学习(2-5个样本微调)可适应新用户,但年龄≥35岁和单眼皮人群的95%一致性区间略宽(最大达±5.8°),提示皮肤松弛度、眼睑褶皱深度对测量的影响仍需进一步建模。
缺乏纵向数据:目前研究聚焦于单次诊断的横断面验证,尚未追踪同一患者术前术后的长期变化——而这正是手术评估的核心场景。
设备集成度:当前系统仍需头戴式柔性电路板(5cm×4cm,2.48g),虽已做到轻量化,但距离“隐形电子纹身”的终极形态尚有距离。
正如论文在讨论部分坦诚指出的:“可穿戴设备通过临床试验获得医疗级监测能力,仍面临数据不足和样本量不足的困难。”
但这些困难并不削弱这项研究的根本意义:它第一次证明,眼睑可以成为窥视眼动功能的“窗口”,而柔性电子与AI的结合,足以将这一微小窗口转化为精准诊断的通道。对于全球数以百万计的斜视患儿而言,这可能意味着第一次,他们只需“看着屏幕”而不是“回答医生”,就能完成一次准确的眼部检查。
[1] Yong Yang et al. ,One-stop strabismus digital diagnosis via AI-integrated skin-like and wearable “Eyelectronics”.Sci. Adv.12,eaeb7242(2026).DOI:10.1126/sciadv.aeb7242
END
撰文 | 郝娅婷
排版 | 张艳青
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
点击关注医工学人
直播预告


本篇文章来源于微信公众号: 医工学人