星标“医工学人”,第一时间获取医工交叉领域新闻动态~

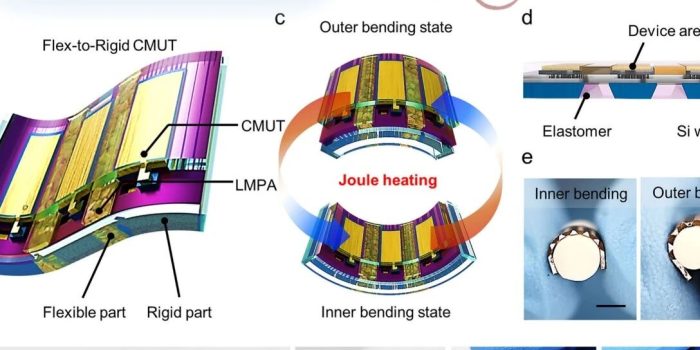
引言:柔性超声的“曲率危机”与可穿戴治疗的下一代平台 可穿戴超声贴片代表着医疗诊断和治疗的革命性方向,有望提供免提、长期和连续的解决方案。然而,现有的柔性超声换能器面临着一系列结构性矛盾,这些矛盾严重限制了它们在临床上的实际应用,尤其是在需要精确靶向治疗的领域。 传统柔性超声的固有矛盾与技术痛点 传统的柔性超声技术主要分为两大策略:一是使用软耦合贴片结合刚性压电(PZT)探头;二是开发基于压电陶瓷或聚合物的完全柔性阵列。这两种方法都存在难以调和的固有缺陷。基于软膜的电容式微机械超声换能器(CMUT)由于振动膜的杨氏模量较低,声学功率不足,难以实现深层穿透或高效治疗。 更关键的缺陷在于曲率控制的缺失。现有柔性贴片的设计空间和制造规模受限于人工流程。由于缺乏对曲率的精确控制,皮肤和身体的微小移动会轻易改变超声波束的方向。对于需要精确能量输送的治疗(如神经调控)或精确的医学诊断而言,这种声束方向的漂移是“致命缺陷”。此外,大多数柔性阵列依赖于复杂的手动制造,导致产出率低、成本高,难以实现晶圆级、低成本、大规模生产,从而构成了其从专业医院走向家庭护理的巨大壁垒。 核心突破:FTR CMUT——结构工程学的范式转移 为了克服这些限制,韩国科学技术院(KAIST)等机构的研究团队开发了一种基于柔性-刚性(Flex-to-Rigid, FTR)技术的超声换能器阵列。该技术的核心战略是通过混合晶圆级微制造,将具有高声学性能的刚性CMUT元件(刚性岛屿)嵌入到柔性弹性体桥接结构中。 FTR CMUT的创新焦点在于其引入了低熔点金属合金(Low-Melting-Point Metal Alloy, LMPA),实现了静态可调节的弯曲曲率。通过精确锁定所需的弯曲形状,阵列能够保持精确的超声束形成,从而实现对靶点的准确、静态聚焦。这种结构上的刚柔分离,从根本上解决了传统柔性器件在声学性能和机械柔性之间难以平衡的固有矛盾。该设备不仅保持了CMUT技术可大规模生产和高设计自由度的优势,还赋予了其机械灵活性和精确的几何控制,使其成为免提、长期、连续的抗炎治疗应用平台。
FTR CMUT的设计精髓在于对刚性和柔性区域进行物理解耦,确保声学功能和机械柔性的最大化。 1)FTR设计哲学:刚性岛屿与弹性桥接 FTR设计遵循“刚性岛屿和弹性桥接”的原则。超声的产生单元,即CMUT元件,被维持在其典型的刚性形式,以保证高声学功率。而元件之间的空隙则填充了弹性体(如PDMS),作为柔性互连桥。 实现高柔性的关键在于柔性区域的几何设计。研究团队通过对Si{100}晶圆进行各向异性湿法刻蚀,使硅基板暴露出晶面,形成了角度为54.7°的梯形凹槽。这一梯形结构赋予了阵列高度的柔韧性,允许其在内弯和外弯状态下进行大范围形变。实验证实,该结构可以在曲率半径小至2 mm的情况下弯曲,而不会损坏上方的刚性CMUT元件。 该制造技术还展现出极高的设计通用性。FTR结构可以被制造成各种形状,包括平面、立方体,甚至封闭的花朵形状。这表明FTR CMUT能够适应复杂的2D表面乃至各种3D目标,实现共形和静态可调的覆盖,为未来的靶向治疗提供了巨大的设计自由度。 2)晶圆级混合微制造工艺的实现 FTR CMUT的制造流程是晶圆级微制造与标准CMUT工艺的完美结合,解决了柔性超声量产的难题。 该工艺首先采用标准的CMUT制造流程,通过氧化物熔合键合在硅片上形成圆形真空腔体,并实现了整个晶圆的高键合良率。随后,通过晶圆减薄和背侧湿法刻蚀来定义柔性间隔。研究采用了兼容CMOS工艺的氢氧化四甲铵(TMAH)与羟胺(NH2OH)溶液进行背侧硅的各向异性刻蚀,以精确创建梯形柔性区域。 在柔性结构形成后,研究团队将LMPA(熔点47.2℃)通过微注射器涂覆在刻蚀的凹槽区域。为了确保操作安全并防止LMPA在弯曲过程中泄漏,随后将PDMS(弹性体)模塑在CMUT的背侧作为保护性钝化层。LMPA被放置在CMUT的背侧,与皮肤无直接接触,进一步保证了患者的安全性。这种结构工程与CMOS兼容制造的结合,从战略上确保了FTR CMUT技术具备大规模生产的潜力,使其成为可穿戴医疗设备商业化的有力竞争者。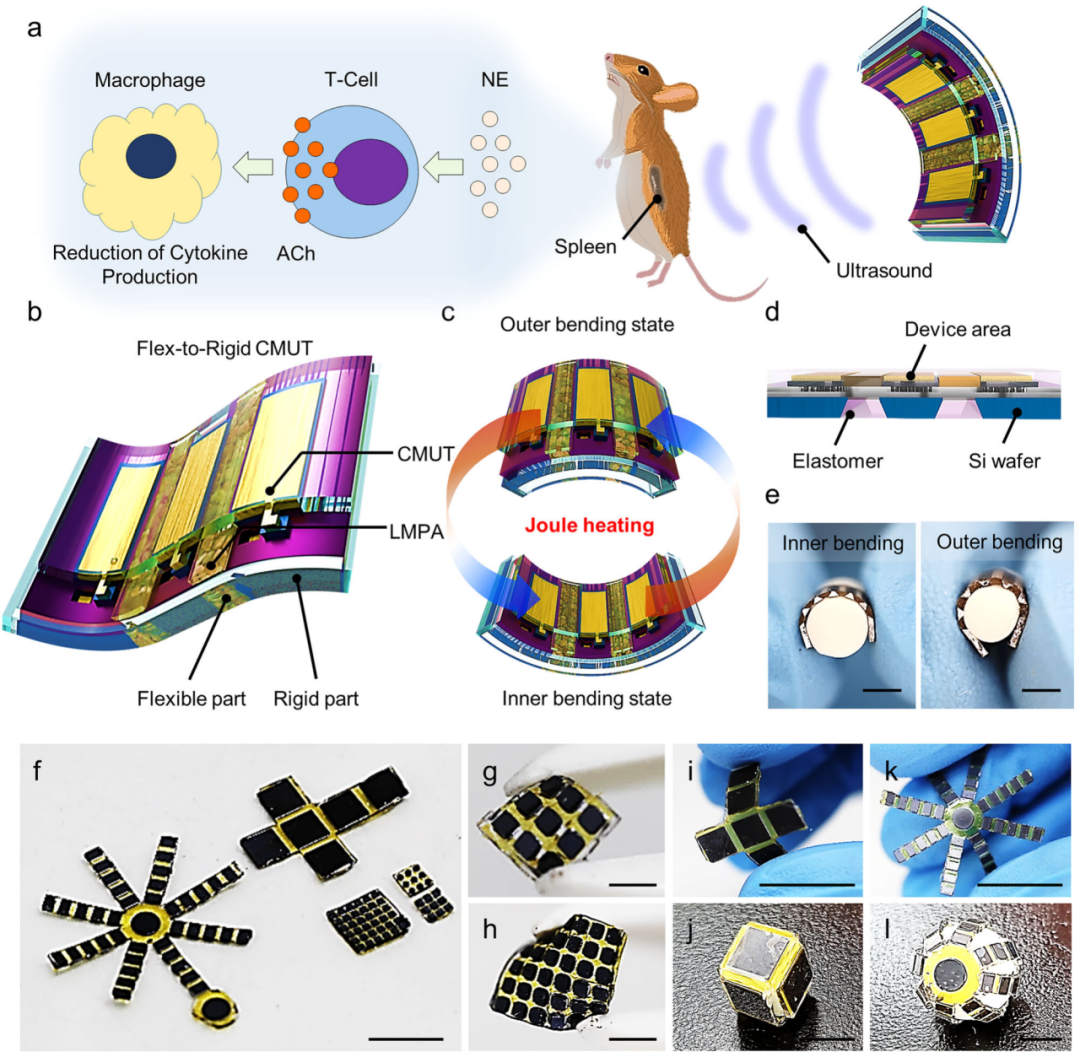
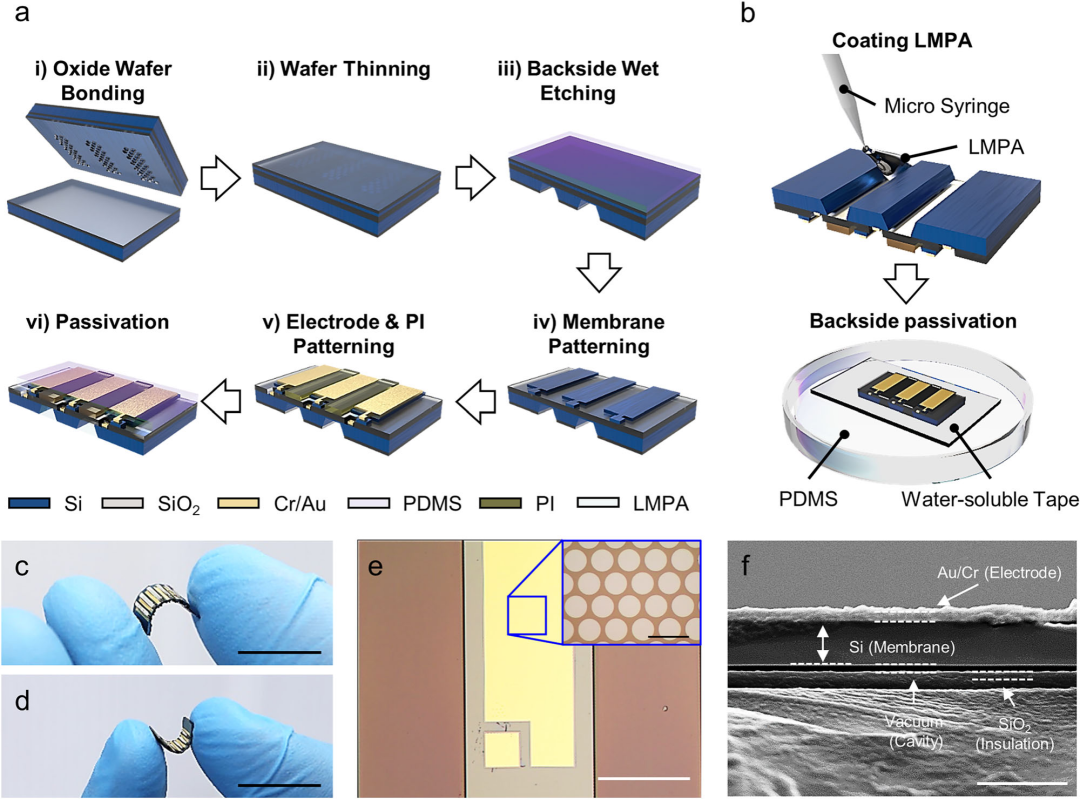
LMPA的引入是该研究的关键创新点,它提供了一种简洁、高效的物理执行机制,解决了柔性阵列在靶向治疗中精度难以维持的难题。 1)LMPA热力学调控与曲率锁定机制 FTR CMUT利用LMPA的固液相变实现曲率的动态调整和静态锁定。LMPA的熔点为47.2℃。通过对连接刚性岛屿的底部基板施加直流电压,产生焦耳热,使LMPA从固态转变为液态。在液态时,阵列可以被塑形为所需的弯曲角度(最大可达45度)。一旦电压被移除,LMPA冷却并固化,将阵列静态锁定在特定曲率上。 研究监测了焦耳热的瞬态响应,发现施加更高的电压可以缩短实现相变的时间。例如,施加3 V电压后,设备在平均约9秒内实现调制,并在约12秒后稳定。在热安全性方面,操作中结构温度被控制在安全范围内,低于美国职业安全与健康管理局(OSHA)规定的60℃安全上限。LMPA的这种可逆、可锁定的相变机制,确保了在长期治疗过程中,超声束的方向和焦点可以保持精确不变。 2)物理聚焦:声束轮廓的精确控制 超声波束对换能器元件的位置变化高度敏感。LMPA实现的可控弯曲曲率,带来了战略性的声学优势:它实现了无需复杂电子波束赋形的物理聚焦。 当FTR CMUT处于内弯(凹)状态时,随着曲率半径(ROC)的减小,超声波束自然汇聚于特定的焦点。这一物理聚焦效应显著提高了声学性能。模拟结果显示,在内弯状态下,与平坦状态相比,最大声压提高了1.6倍,轴向分辨率提高了五倍。相反,在外弯(凸)状态下,超声波束则会分散。这种高度敏感且可控的曲率变化,突显了在柔性超声换能器中实现曲率控制的重要性。对于可穿戴治疗系统而言,静态物理聚焦能够大幅简化驱动电子系统的复杂性,降低功耗,提升系统在靶向神经调控等应用中的能效和可靠性。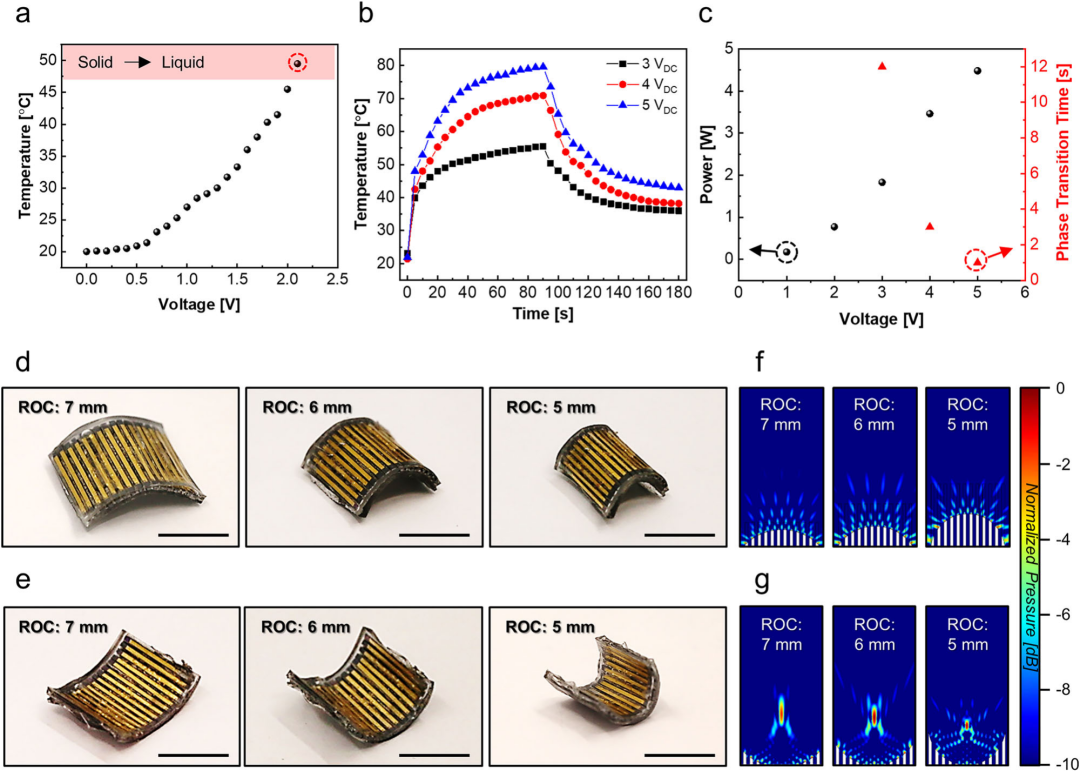
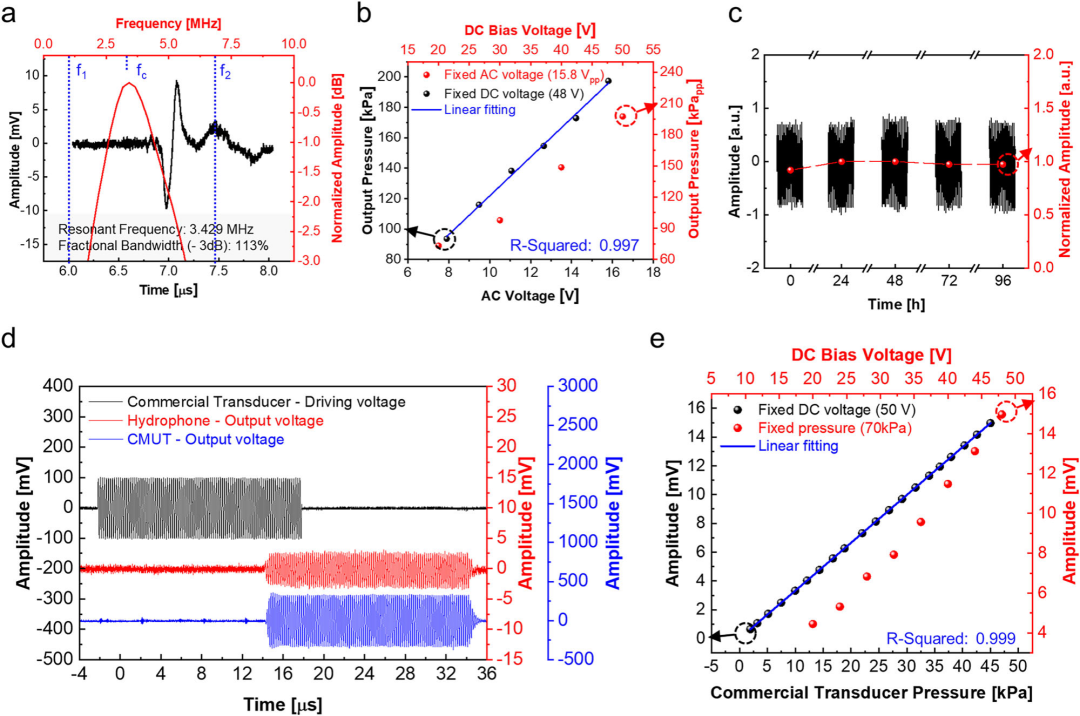
FTR CMUT在电学和声学测试中展现出与标准刚性CMUT相当的优异性能,并在高机械应力下保持了耐久性。 1)电学稳定性与机械耐久性 CMUT阵列的性能均匀性是其实现精确控制和商业化量产的基础。研究对在同一4英寸晶圆上制造的60个相同的CMUT元件进行了测试,结果显示中心频率和拉入电压的变异性分别低于3%和8%,这证明了该晶圆级制造工艺具有高度的可靠性和均匀性 。 在机械耐久性方面,FTR CMUT经受了严格的弯曲疲劳测试。设备在2.5 mm的曲率半径下,完成了100次内弯和外弯循环测试。疲劳测试结果显示,器件的中心频率在内弯和外弯疲劳测试后,仍保持在初始平坦状态频率的99%以内。这种高结构可靠性,是FTR CMUT作为长期可穿戴治疗设备能够投入实际应用的先决条件。 2)治疗级声学输出与宽带优势 FTR CMUT在油浸环境中的声学特性表现出色。在传输模式下,该设备具有超宽分数带宽。例如,在3.4 MHz中心频率下,其-3 dB分数带宽达到了113%。用于抗炎治疗的1.5 MHz器件也提供了86%的分数带宽。高带宽优势意味着单个CMUT可以在广泛的频率范围内工作,这对于研究超声的治疗机理和支持多功能应用(如诊疗一体化)具有重要价值。 在声压输出方面,该器件在固定直流电压48 V下,最大输出声压达到了197kPa(峰峰值)。研究指出,该声压水平处于或高于低强度聚焦超声(LIFU)的典型范围(10 kPa至550 kPa),表明其足以用于神经调控等低强度治疗应用。此外,接收模式下的灵敏度高达332.57 V/kPa(在50 V偏置下)。连续四天的浸入式操作测试显示声学性能没有退化,进一步印证了其在长期治疗应用中的可靠性。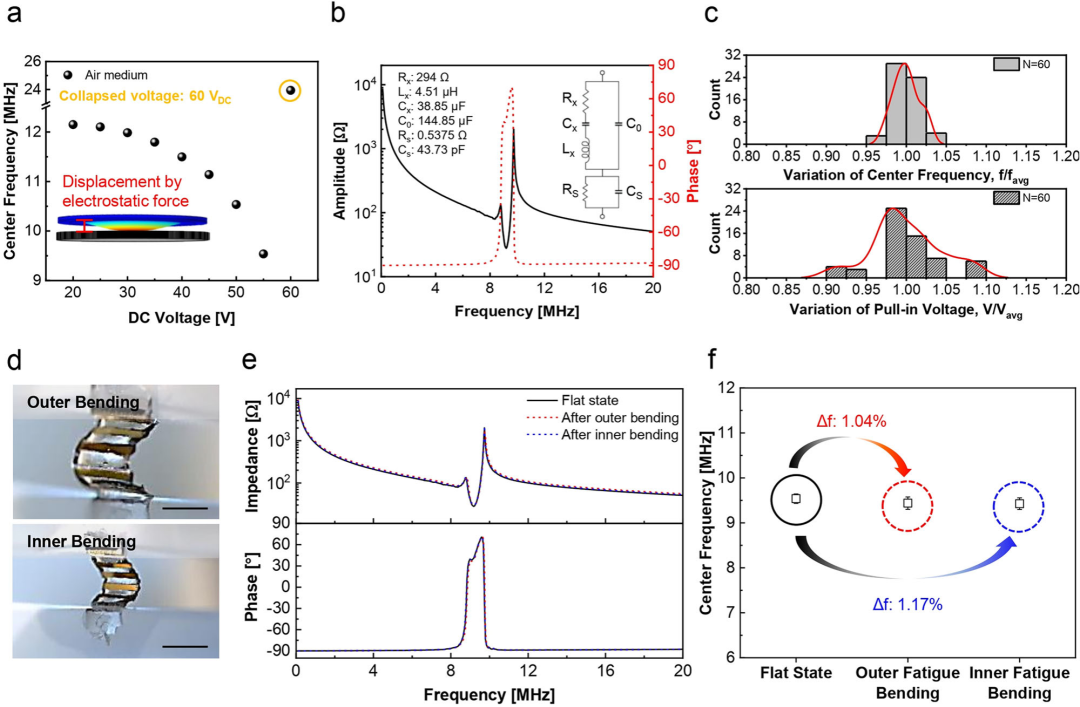
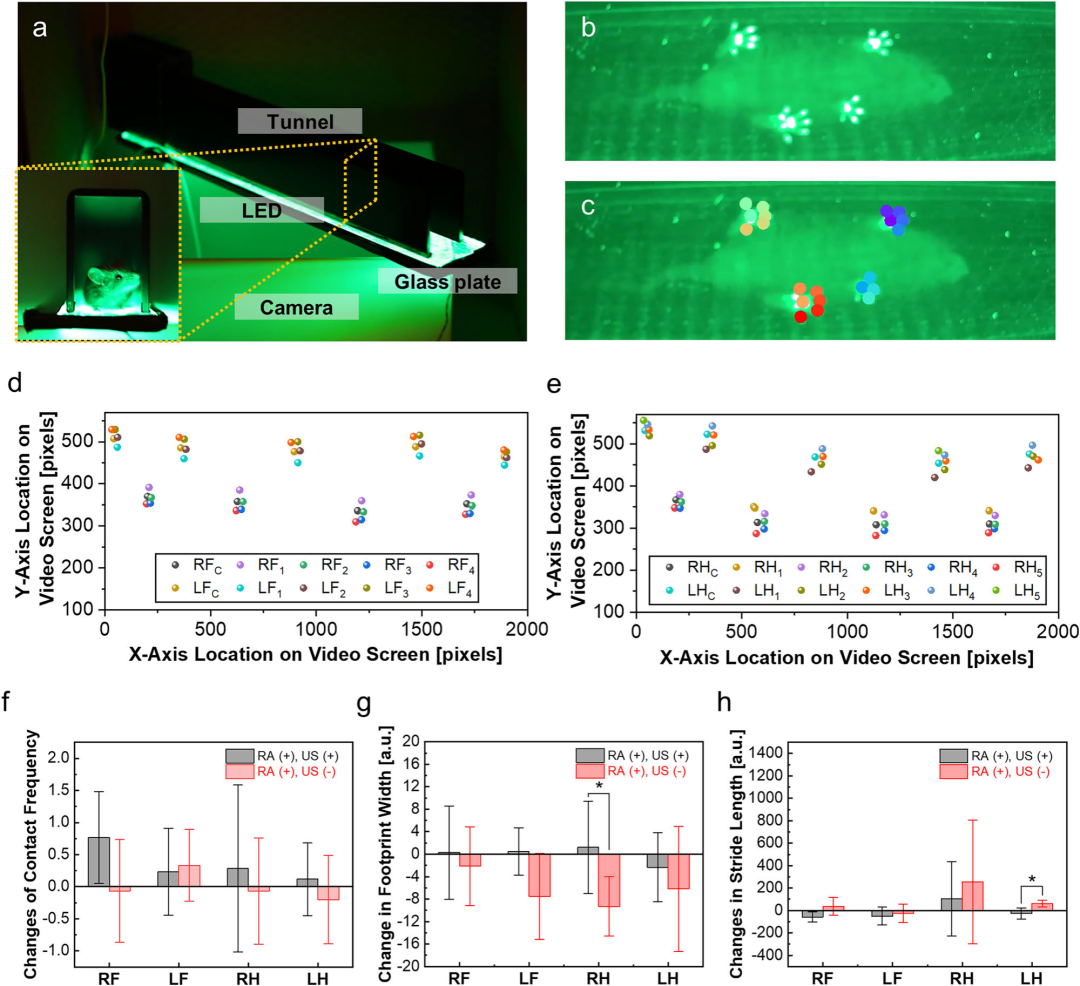
为了验证FTR CMUT在连续治疗中的潜力,研究人员在胶原诱导性关节炎(CIA)小鼠模型上进行了超声刺激脾脏的活体实验,以缓解类风湿关节炎(RA)症状。 1)治疗机制与实验设计 超声刺激脾脏是一种非侵入性的神经调控疗法。其机制在于激活胆碱能抗炎通路(CAIP)。通过迷走神经传导信号,该通路能够抑制巨噬细胞等免疫细胞分泌促炎细胞因子(如TNF)。 实验采用了1.5 MHz的FTR CMUT一维(1D)长条阵列,该阵列被放置在小鼠背侧皮肤上,以确保对脾脏进行充分的超声覆盖。治疗方案为每周3次,持续两周,每次刺激20分钟(脉冲重复频率0.167 Hz,占空比16.7%)。超声参数设定在1 MHz频率、峰值压力350 kPa。研究严格控制了安全指标:空间峰值脉冲平均强度为4.08 W/cm2,热指数(TI)为5.82,均在FDA的安全标准范围内。 2)炎症指标的量化结果 (图6b-g) 研究通过连续测量踝关节厚度和临床评分来评估疗效。结果显示,在接受超声刺激的治疗组(RA+, US+)中,小鼠的踝关节厚度在两周治疗后表现出显著减少(p=0.037)。与此形成鲜明对比的是,假手术组(RA+, US-)和模型组(RA+)的踝关节肿胀在实验期间持续恶化或增加。 此外,治疗组的类风湿关节炎临床评分也明显改善,而对照组的症状则持续恶化。在整个实验期间,所有组的小鼠体重均持续增长,这从侧面验证了超声治疗的安全性,未引起全身性的不良反应。 3)行为学功能恢复:DeepLabCut步态分析 为了更客观地评估治疗对功能恢复的影响,研究使用了基于机器学习的DeepLabCut(DLC)工具进行步态分析。该分析通过追踪小鼠足印的接触频率、宽度和步幅长度等行为学指标,量化了疼痛减轻带来的功能性改善。 结果显示,在刺激组中,足印的接触频率在治疗后显著增加。这表明小鼠的踝关节疼痛减轻,能够更频繁、更自然地使用受影响的肢体。同时,刺激组的步幅长度呈现下降趋势,这通常意味着步态功能正在恢复到更正常的水平。这些行为学数据提供了强有力的证据链,证明FTR CMUT的超声刺激不仅在形态学上减轻了炎症肿胀,更在功能上实现了小鼠的步态恢复,验证了该技术在神经调控治疗中的临床转化潜力。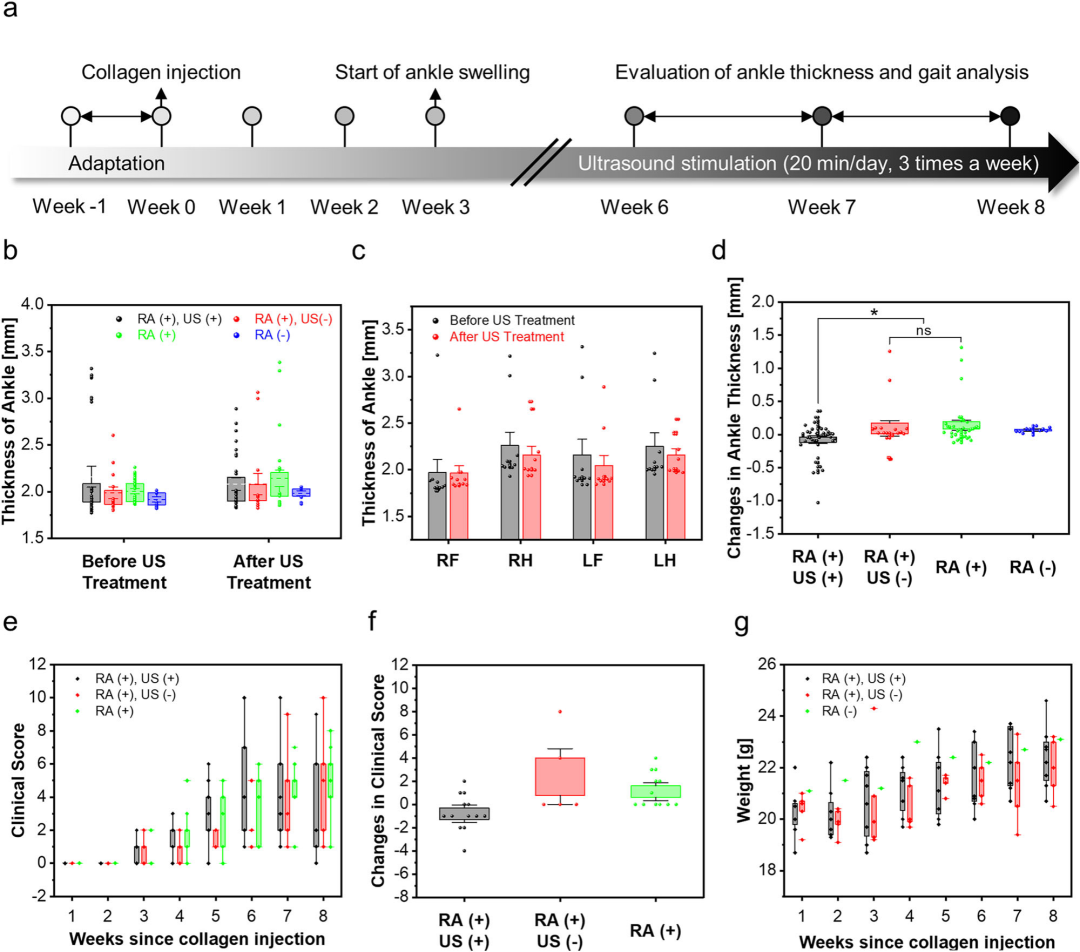
FTR CMUT的出现标志着柔性超声技术进入了可控、高效率的新阶段。然而,要实现大规模商业化和集成,仍需解决核心工程挑战,并结合新兴的AI技术。 1)柔性超声的市场定位与工程挑战 FTR CMUT通过结构解耦的巧妙设计,成功地将其声学性能提升至治疗级,超越了性能受限的完全柔性CMUT。同时,其静态可调曲率使其优于依赖外部耦合介质的传统刚性探头,满足了可穿戴设备对共形性和聚焦稳定性的高要求。 然而,CMUT技术固有的主要劣势是需要较高的操作电压。这与当前可穿戴设备追求的低功耗、小型化目标存在本质冲突,是其商业化集成到家用便携系统中的关键障碍。 尽管存在高压驱动的挑战,但CMUT技术与CMOS技术的高度兼容性是其长期战略价值的决定性因素 。这种兼容性允许在同一硅片上集成换能器和驱动电子,为实现系统级小型化和大规模量产提供了无可比拟的优势。随着半导体技术的进步,通过优化器件几何结构、使用先进的高k绝缘层或开发高效率的高压驱动电路,CMUT的电压需求有望逐步降低,最终消除这一商业化壁垒。 2)迈向终极集成:从1D到2D阵列与AI闭环的未来 该研究团队明确指出,未来的工作方向是将FTR制造和LMPA弯曲调控扩展到2D超声换能器阵列。2D阵列是实现下一代医疗应用的关键,它能够实现同步的高质量超声成像和治疗。这意味着医生或家用系统可以实时监测脾脏的解剖位置和炎症状态,并同时施加精确的超声刺激,实现真正的诊疗一体化。此外,通过优化设备几何和驱动电子,阵列的声学输出可以进一步提高,最终有望支持高强度聚焦超声(HIFU)等更高强度的应用。 AI驱动的闭环神经调控系统是柔性超声的终极演进方向。AI算法可以通过分析患者的生物标志物、功能超声成像(fUSI)信号或DLC步态分析等数据,实时评估治疗靶点状态。LMPA在这一系统中扮演了关键的物理执行器角色。AI可以根据实时反馈,指令LMPA快速、精确地调整曲率,实现低能耗、高保真的静态物理聚焦。随后,驱动电子只需精确控制超声脉冲。这种“AI决策 + 物理聚焦 + 电子控制”的闭环机制,将确保超声剂量始终精确聚焦在靶点,极大地提高了治疗的个性化和长期疗效,为类风湿关节炎等慢性炎症性疾病的家庭化、非侵入性管理开辟了新路径。
这项基于柔性-刚性(FTR)CMUT和低熔点金属合金(LMPA)的超声换能器阵列,代表了可穿戴医疗技术在工程结构和功能控制上的重大飞跃。该技术通过独特的结构设计,成功解决了传统柔性超声在性能和曲率控制上的核心矛盾,同时保留了CMUT技术晶圆级制造和大规模生产的战略优势。 在概念验证层面,该设备通过对CIA小鼠模型脾脏的非侵入性超声刺激,成功激活了抗炎通路,并在形态学(踝关节肿胀减少)和行为学(步态功能恢复)上提供了清晰的疗效证据。 从战略投资角度来看,FTR CMUT的静态可调曲率技术,实现了无需电子波束赋形的物理聚焦,为可穿戴设备提供了低功耗、高精度的靶向治疗基础。尽管目前仍面临高压驱动的工程化挑战,但其与CMOS技术的兼容性,决定了其在未来诊疗一体化和AI驱动的闭环神经调控系统中,将占据核心“神经接口”的地位。这项研究不仅为类风湿关节炎等慢性炎症性疾病的长期家庭管理提供了可行的新工具,更为下一代可穿戴医疗设备的结构设计和智能集成指明了方向。
文章链接:https://www.nature.com/articles/s41528-025-00484-7
END 撰文 | 赵亚军 编辑 | 吴苡齐 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊, 参与线上线下交流活动
推荐阅读
Nature Sensors | 加州大学徐升团队开发AI增强型柔性电子皮肤接口,让机器人在剧烈运动中也能读懂你的“手语”
Nature Medicine | 温州医大&北大等联合团队打造“全生命周期时钟”,AI+常规体检数据即可预测未来疾病风险

点击关注医工学人

本篇文章来源于微信公众号: 医工学人