星标“医工学人”,第一时间获取医工交叉领域新闻动态~

想象一下这样的场景:一个患有Ⅰ型糖尿病的孩子在深夜熟睡,血糖水平却在悄然无声地降至危险低点。传统的液体胰高血糖素注射剂因为稳定性差,无法用于自动化的植入式药泵 ;而家中的急救包则需要父母在慌乱中完成混合药粉、抽吸、注射等一系列复杂操作,每一秒的延迟都可能带来灾难性后果。
现在,麻省理工学院的研究团队在《自然-生物医学工程》上发表的一项研究,为我们展示了解决这一困境的方案:一个比硬币还小、重量不足2克的无线“救援芯片” ,可以安全存储稳定的粉末药物,并在紧急情况下主动“弹射”药物,突破人体为抵御异物而形成的疤痕组织,为血糖骤降、严重过敏等急性病症提供即时救援。它不仅解决了药物长期存储的稳定性难题,更以一种巧妙的机械方式,攻克了所有植入式设备都面临的终极障碍——纤维包囊。

全文约3178字,全部听完大约5分钟~
开发长期植入式自动给药系统,尤其是在紧急救援领域,科学家们始终面临两大核心难题:
1)药物稳定性
许多救命的生物制剂,如用于提升血糖的胰高血糖素和用于抗过敏的肾上腺素,在液体状态下极不稳定,保质期甚至不足一天 。这使得依赖液体药物的传统植入式药泵方案难以实现长周期、免维护的“闭环”管理。相比之下,它们的干粉(冻干)形态则可以无限期稳定保存。
2)纤维包囊
当任何异物被植入体内,人体的免疫系统会本能地在其周围形成一层致密的疤痕组织,即纤维包囊 。这层“隔离墙”会严重阻碍药物的扩散和吸收,对于需要争分夺秒的紧急情况而言,这种延迟是致命的。
如何将稳定的干粉药物,在需要时,精准、快速地穿透这层生理屏障,送达体内?这正是MIT团队试图破解的难题。
该团队设计的救援芯片(Emergency Rescue Chip)结构紧凑而高效。其核心在于一个由“形状记忆合金”(Shape-Memory Alloy, SMA)制成的微型密封盖。
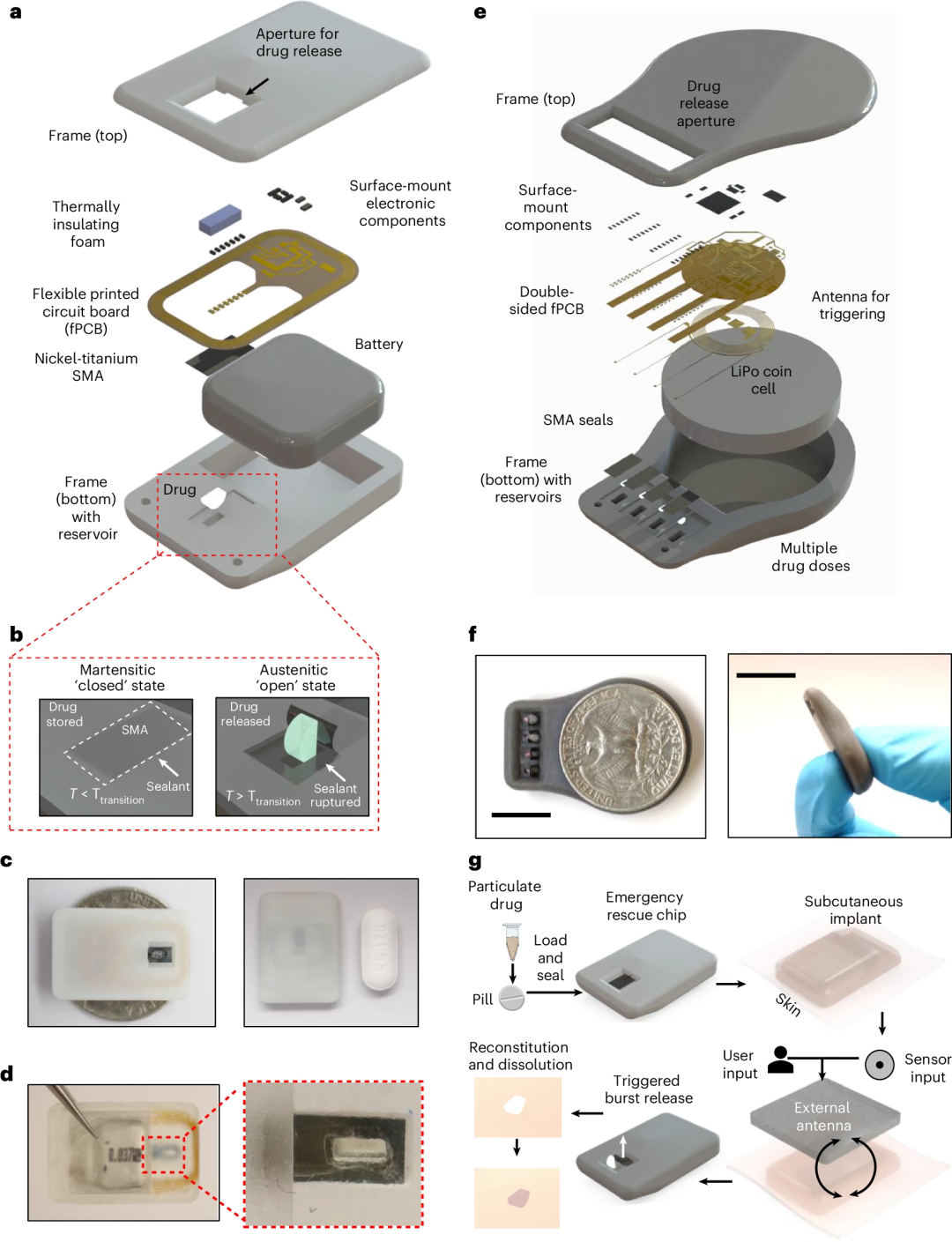
图1:单剂量与多剂量无线救援芯片的设计。 (a, c, d) 展示了单剂量设备的设计,包含电池、柔性电路板(fPCB)和存储药物的药仓。e, f) 为多剂量版本的设计,可容纳多个独立的药物胶囊。g) 描绘了其工作流程:装载药物、皮下植入、通过外部信号(如手机或传感器)无线触发,最终实现药物的爆发式释放与快速吸收。
这种镍钛合金拥有一种神奇的物理特性。研究人员预先将其“编程”成一种卷曲的“开启”形态,然后在低温下将其压平成一张薄片,用以密封存储着冻干药物粉末压成的药丸的药仓 。这个密封过程还采用了低渗透性的聚合物和疏水性蜡质进行边缘密封,确保了药物在体内的长期干燥和稳定。
当紧急情况发生时,一个外部无线信号(例如来自智能手机的NFC信号,频率为13.56 MHz)会激活设备内的微型加热元件 。在不到25秒的时间里,加热元件使SMA薄片温度升高到其35℃的相变温度以上。这瞬间的温度变化,如同唤醒了这片金属的“肌肉记忆”,使其在不到10秒内猛然恢复到预设的卷曲形态。这个剧烈的机械动作会撕裂密封层,以爆发式的力量将药物药丸主动“弹射”出去。
研究团队通过一系列严谨的实验,验证了该设计的有效性和巨大潜力。
1)突破屏障,效率提升三倍
在模拟人体组织的琼脂糖凝胶实验中,研究人员对比了药物的被动扩散和设备的主动释放。结果惊人:在10分钟内,被动扩散的药物前沿仅推进了约400微米;而通过救援芯片弹射出的药物,其扩散距离达到了1.2毫米,扩散效率提升了整整三倍 。高速摄像机捕捉到的画面显示,SMA的开启过程在凝胶中造成了局部的物理破裂,为药物开辟了快速通道。
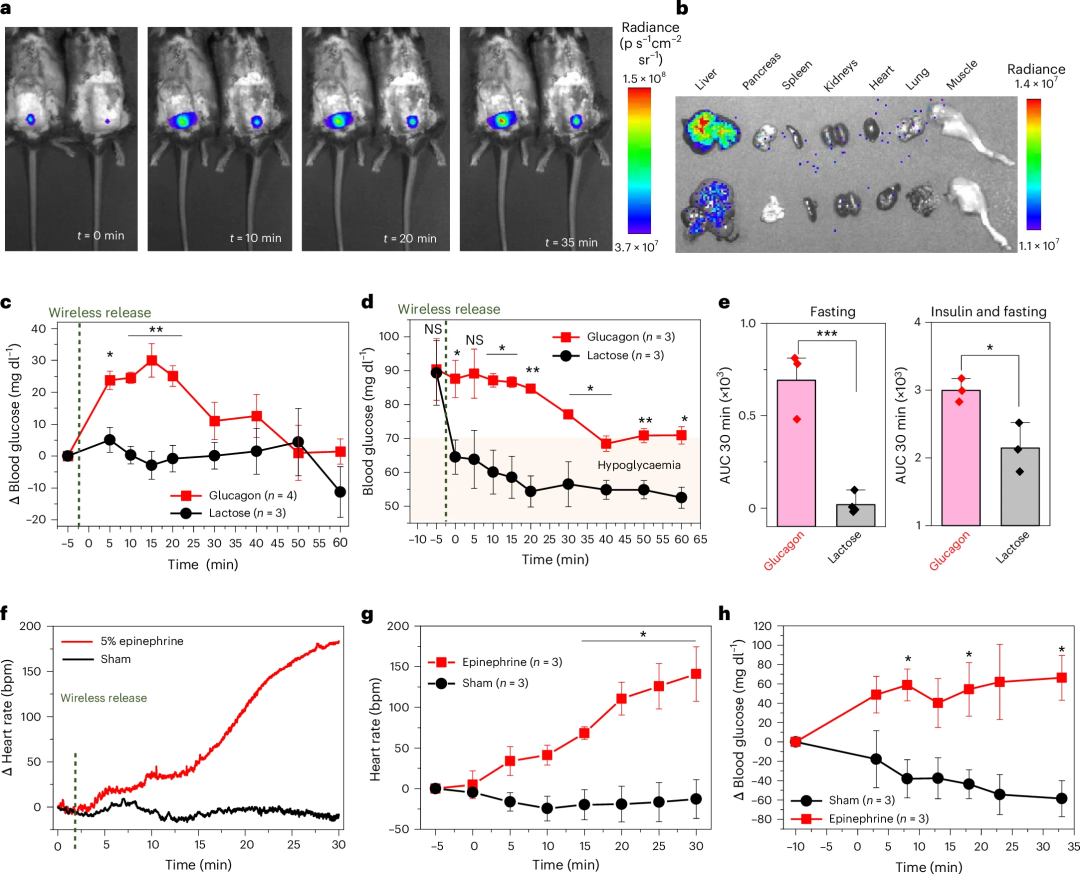
图5:在糖尿病小鼠模型中实现紧急低血糖救援。 (c) 在仅禁食诱导的轻度低血糖模型中,无线释放胰高血糖素(红色方块)后,小鼠血糖在15分钟内迅速升高,显著高于对照组(黑色圆圈)。
(d) 在通过注射胰岛素诱导的严重低血糖模型中,该设备同样成功将血糖维持在安全水平以上,实现了有效的低血糖救援。
2)闭环控制与活体救援
更进一步,团队将该设备与市售的连续血糖监测仪(CGM)集成,构建了一个全自动的闭环救援系统 。在模拟实验中,当系统连续两次检测到血糖浓度低于50 mg/dL的危险阈值时,便会自动触发无线信号,释放药物。
在糖尿病小鼠模型中的活体验证更是令人振奋。研究人员通过注射链脲佐菌素(STZ)诱导小鼠产生糖尿病,并植入了装有胰高血糖素药丸的救援芯片。当小鼠因禁食或注射胰岛素而出现低血糖时,研究人员通过无线方式触发了药物释放。结果显示,在释放后的10-15分钟内,小鼠的血糖水平出现了快速且显著的回升,成功避免了严重低血糖的发生 。相比之下,植入了仅含安慰剂(乳糖)设备的对照组小鼠则持续处于低血糖状态,并表现出行动迟缓、反应微弱的典型症状。
此外,该平台还成功用于释放肾上腺素,在5分钟内引起了小鼠心率和血糖的预期生理变化,证明了其作为通用型紧急药物递送平台的广泛适用性。
3)长期植入与“破壁”能力
最关键的验证来自长期植入实验。设备在小鼠和和免疫功能健全的大鼠体内植入长达4至7周后,其周围已形成了成熟的、厚度可达数百微米的纤维包囊 。在取出这些带有组织的设备后,研究人员在体外激活了释放机制。结果显示,SMA的弹射力量足以完全穿透这层致密的纤维组织,成功释放药物 。对未开封设备中药物的检查也证实,经过长达7周的体内植入,药丸依然完整、稳定,未受体液侵蚀。
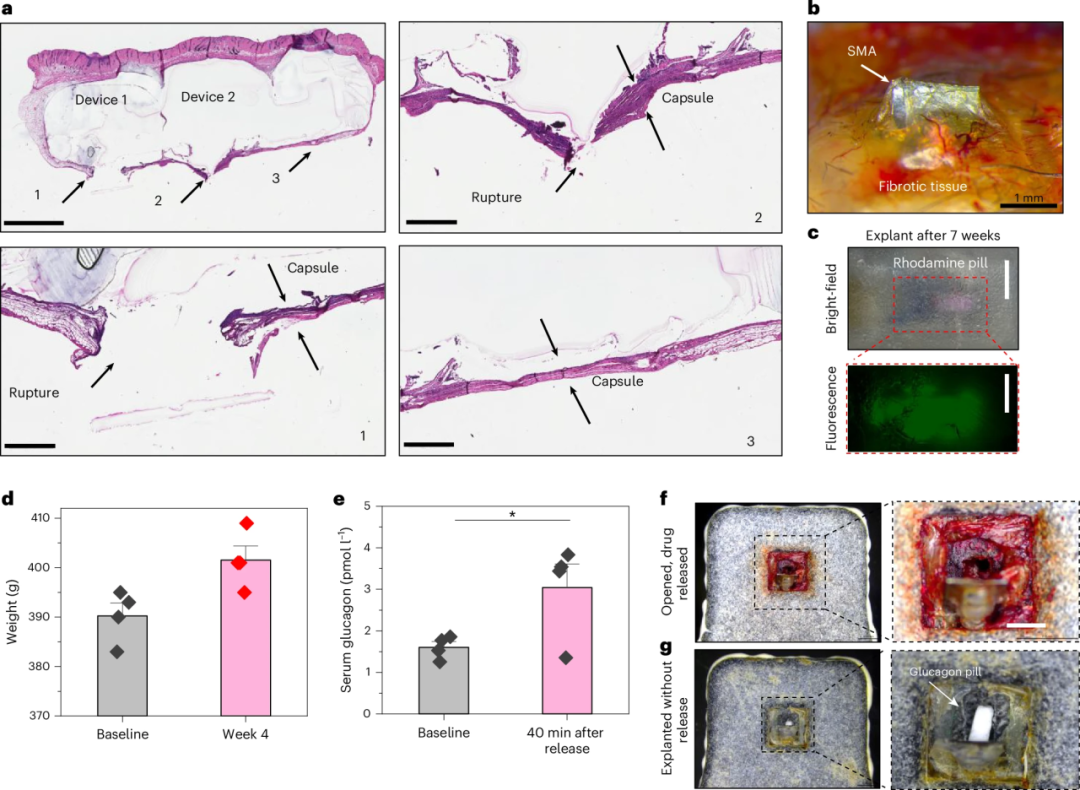
图6:长期植入后的药物稳定性与突破纤维包囊能力。 (a, b) 组织学切片和光学图像显示,经过7周的皮下植入后,设备被一层纤维包囊(Capsule)包裹。激活后,SMA密封盖能够完全撕裂(Rupture)这层组织,实现药物释放。
(g) 在另一组为期4周的植入实验中,未被激活的对照设备在取出后打开,可见内部的胰高血糖素药丸完好无损,证明了其出色的密封性和药物稳定性。
这项工作不仅仅是一次巧妙的工程设计,它为解决慢性病管理的“最后一公里”问题——即无法预料的紧急状况——提供了全新的思路。
1)评论与分析
范式转变:该技术实现了从“被动扩散”到“主动递送”的范式转变。传统的植入式给药系统,无论药物如何释放,最终都需依赖在组织液中的缓慢扩散。而这种“弹射”机制,本质上是一种微型的“皮下注射”,它通过机械力克服了生理屏障,这种理念对于所有需要快速起效的植入式疗法都具有启发意义。
闭环系统的关键拼图:在糖尿病管理领域,“人工胰腺”等闭环系统已取得巨大进展,但它们主要负责日常的胰岛素精细调控。而MIT的这项技术,则完美扮演了“安全气囊”的角色。它作为一个独立、长期待机、一触即发的救援系统,有望消除患者及其家人(尤其是儿童患者)对夜间低血糖的持续恐惧 ,从而极大地提升生活质量,并鼓励患者更积极地进行血糖管理。
平台化潜力:尽管研究聚焦于胰高血糖素和肾上腺素,但该技术的核心是储存和递送冻干粉末药物的能力。理论上,任何可以被制成稳定干粉的药物,都有可能被整合进这个平台。这为治疗阿片类药物过量(递送纳洛酮)、癫痫持续状态或其他需要紧急干预的医疗场景打开了想象空间。
2)未来展望
当然,这项技术从实验室走向临床应用仍有路要走。研究人员指出,下一步需要在更接近人体的大型动物模型中进行验证,以确定精确的给药剂量和药代动力学 。此外,反复“刺破”纤维包囊对局部组织的长期影响,以及多剂量设备在实际使用中的可靠性,也需要更深入的研究。
Krishnan, S.R., O’Keeffe, L., Rudra, A. et al. Emergency delivery of particulate drugs by active ejection using in vivo wireless devices. Nat. Biomed. Eng (2025). https://doi.org/10.1038/s41551-025-01436-2
END
撰文 | 刘帅
编辑 | 吴苡齐
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
点击关注医工学人

本篇文章来源于微信公众号: 医工学人