星标“医工学人”,第一时间获取医工交叉领域新闻动态~

一款微型植入设备,在强化康复训练中精确刺激迷走神经,为慢性颈椎脊髓损伤患者的手臂和手部功能恢复带来了显著希望。21日,发表于《自然》杂志的研究,采用“闭环”系统,昭示着在损伤发生多年后,有意义的康复仍有可能实现 [1]。

数十年来,对于慢性脊髓损伤 (SCI) 患者而言,获得显著恢复的前景一直黯淡,大多数康复手段在损伤发生后很长一段时间内收效甚微。但一项主要由德克萨斯大学达拉斯分校和贝勒斯科特与怀特研究所的研究人员进行的新研究,正在挑战这一固有观念 。他们的方法被称为闭环迷走神经刺激 (CLV),通过协同结合游戏化物理治疗与精确定时的迷走神经电脉冲刺激(VNS),从而调控这一身体主要的通讯高速公路 。一项包含19名受试者的双盲、假手术对照试验结果表明,该方法可以开启运动功能恢复的新层面 。 01 蓝图:靶向神经可塑性
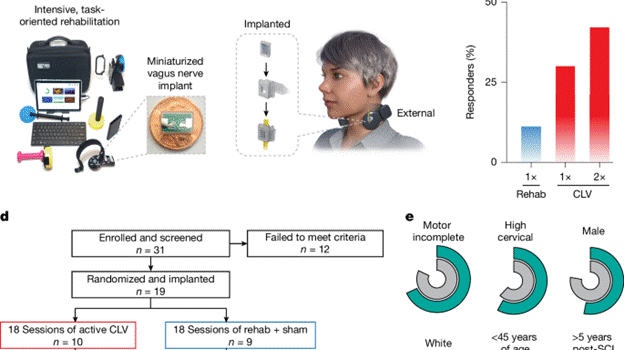
CLV背后的核心理念不仅仅是刺激神经,而是智能地进行刺激。该系统采用了一种微型化迷走神经刺激器,比现有设备小约50倍,通过简化的手术植入颈部迷走神经附近 。该植入物由参与者仅在治疗期间佩戴的外部单元进行无线供电和控制 。
图1 用于慢性脊髓损伤的闭环迷走神经刺激。 “闭环”是其关键所在:刺激并非持续进行,而是在传感器检测到参与者在游戏化练习中成功完成治疗性动作时,以短暂的半秒脉冲形式精确传递 。这种精确定时被认为利用了大脑的“突触易感性痕迹”——一个短暂的窗口期,在此期间,由运动激活的神经回路如果接收到由VNS触发的神经调质信号,则非常容易被强化 。已知VNS能驱动中枢神经系统中关键神经调质(如乙酰胆碱、去甲肾上腺素和血清素)的释放,从而促进突触可塑性 。
该研究精心招募了19名患有慢性(损伤后至少一年)、不完全性颈椎SCI的个体 。植入设备后,参与者被随机分配接受18次积极CLV或假刺激联合强化康复治疗,随后所有人再接受额外18次积极CLV治疗 。这种设计既能与假手术对照组进行比较,也能检验剂量效应 。令人鼓舞的是,参与者在损伤类型、种族和年龄方面的人口统计学特征与全国平均水平基本一致,这增强了研究结果的潜在普适性 。
02 瞄准功能障碍:为何聚焦手腕功能? 研究人员将重点放在上肢恢复,特别是手和手腕功能,原因在于这些功能障碍在颈椎SCI后常见且严重影响生活质量。他们的基线评估证实,通过GRASSP(分级和重新定义的上肢力量、感觉和抓握评估)评分衡量的临床损伤程度,与捏力 (R2=0.77) 和腕部扭矩 (R2=0.68) 等客观指标之间存在强相关性 。事实上,这两项力量指标的线性组合可以解释该人群中87%的上肢残疾变异 。
图2 脊髓损伤后手部和腕部功能障碍是功能恢复的目标。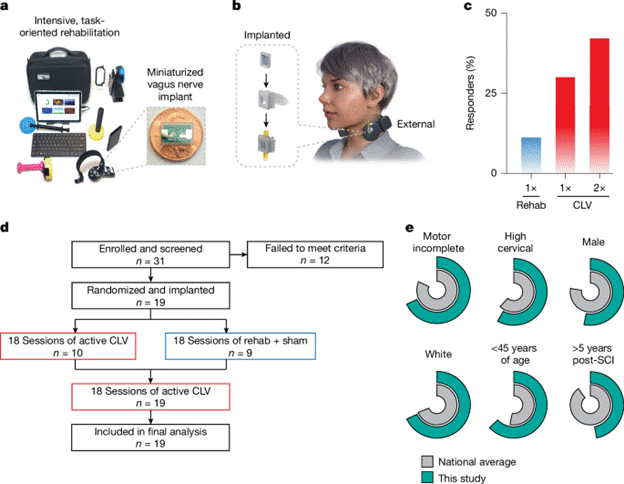
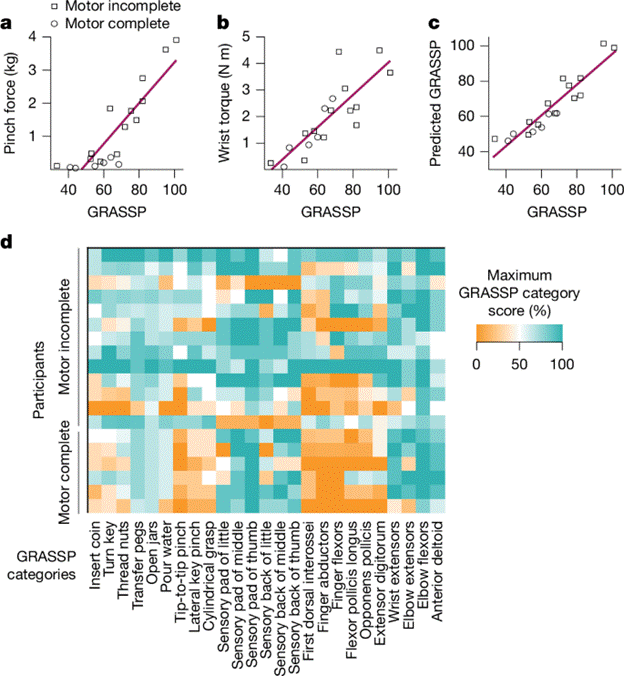
然而,这些损伤的具体性质因人而异,存在显著的异质性(图2d) 。这种异质性强调了个体化治疗方法的必要性,而非一刀切的方案 。
03 治疗方案:强化、个体化与自适应的康复之路 CLV治疗绝非千篇一律。每位参与者都进行了一套个性化的、包含六到九种游戏化练习的方案,利用一系列传感器(加速度计、应变片等)来追踪运动和力量 。这些练习针对特定的功能限制,范围从物体操纵、手指运动到打字和握力等 。
图3 强化、个体化的闭环迷走神经刺激治疗。 治疗师通过修改应用于传感器输入的“辅助因子”(或增益)来持续调整任务难度,使得游戏既具有可玩性又充满挑战 。正如预期的那样,该辅助因子与参与者的基线GRASSP分数呈负相关,证实了治疗是根据个体能力水平量身定制的(图3c)。游戏级别也逐步提高,要求更高的速度和精确度 。尽管损伤程度差异很大,参与者在游戏过程中的错误率保持稳定,表明他们始终在其能力极限受到挑战 。
迷走神经刺激由一种能够根据表现自适应调整的算法触发,确保了在不同损伤水平和整个治疗过程中VNS的稳定递送(每90分钟治疗约341次刺激) 。一个自动算法最终控制了大部分刺激,通过更精确地瞄准超常运动,其表现优于治疗师手动触发的刺激(扩展数据 图5)。
04
成果显现:力量、速度与活动范围的显著提升 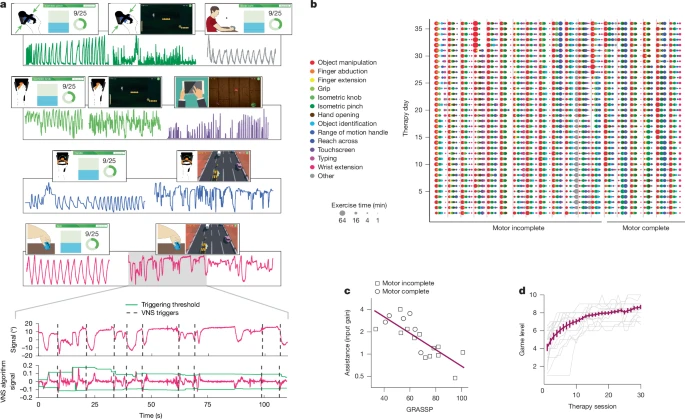
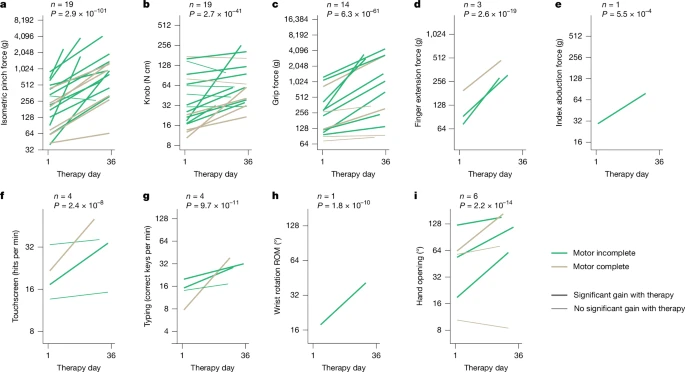
经过36次CLV治疗的效果是显著的。以手部功能的关键指标——等长捏力为例,19名参与者中有18名表现出统计学上的显著增加,平均改善了 936±247 克——相较于基线水平,增幅高达393%(图4a) 。类似地,19名个体中有13名的腕部扭矩(旋钮力量)显著增加,平均改善了152%(图4b) 。
图4 闭环迷走神经刺激改善手部和手腕的力量、速度和运动范围。 这些改善并非孤立存在。在由不同参与者子集(由于个体化方案)进行的各种练习中,均观察到握力、手指伸展力、食指外展力、触摸屏打字速度、键盘打字速度、腕关节旋转活动度和手张开角度的显著改善(图4c-i) 。平均而言,各种练习中产生的力量、速度和活动范围大约增加了一倍 。
05 临床影响:从力量增益到功能改善
至关重要的是,这些原始运动输出的增加转化为了具有临床意义的改善。作为研究主要临床终点的GRASSP评分,在CLV治疗后显示出统计学上显著的平均改善 4.1±1.5 分(图5a) 。这一改善显著超过了通常认为具有临床重要性的最低水平,并对慢性SCI患者功能不再可能进一步改善的观点提出了质疑 。19名参与者中有8名在GRASSP评分上取得了“有意义的”6分或以上的增加 。
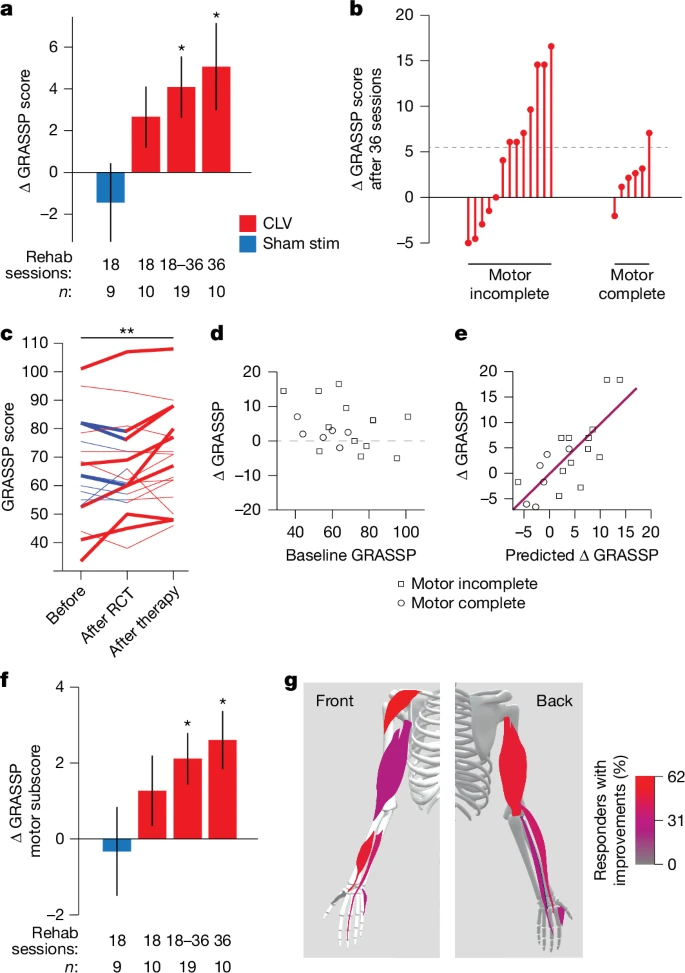
图5 闭环迷走神经刺激改善了上肢功能的临床指标。
该研究还为哪些人群可能受益最大提供了线索。运动功能不完全性损伤(AIS C级或D级)的个体通常比较运动功能完全性损伤(AIS B级,损伤平面以下无运动功能保留)的个体表现出更大的恢复程度(图5b)。
有趣的是,单独的基线损伤严重程度、年龄或受伤后时间并不能预测治疗反应(图5d) 。然而,一个包含AIS分级、基线力量以及特定感觉评分的多因素线性回归模型,能够以合理的准确性 (R2=0.6) 预测GRASSP评分的变化(图5e) 。
这些益处也扩展到了日常生活活动中,Jebsen-Taylor手功能测试分数以及脊髓独立性评估量表 (SCIM-III) 中与手臂和手相关的项目均有显著改善 。甚至未训练的手臂在GRASSP评分上也显示出适度但统计学上显著的改善,这是一个意想不到的发现,值得进一步研究(扩展数据 图4a)。
在双盲、假手术对照阶段(前18次治疗),接受积极CLV的参与者在GRASSP评分上的改善大于假刺激组,效应量为中等(Cohen’s d = 0.58),尽管在这种相对较小的样本量中,这种差异未达到统计学显著性——这是早期可行性研究中的常见挑战。
该疗法改善了手臂和手部的多种肌群,其中三角肌、拇长屈肌(一种拇指肌肉)、肘伸肌和腕伸肌是最常得到改善的肌群(图5g)。拇对掌肌(另一种拇指肌肉)是唯一未显示改善的肌肉,这提示了未来练习方案改进的潜在方向。
06
安全性与展望
包括新型微型化植入物在内的CLV疗法被证明是安全且耐受性良好的 。在19例植入手术、760次患者访视和近370万次VNS脉冲刺激过程中,未发生与设备相关的严重不良事件 。所有报告的不良事件,如临时的切口部位疼痛或颈带引起的皮肤刺激,均被归类为轻度 。值得注意的是,声音改变这一传统大型VNS系统常见的副作用,其发生率似乎有所降低,这可能归因于设备尺寸更小和侵入性更小的手术过程 。重要的是,CLV并未对心血管功能产生负面影响,也未诱发自主神经反射异常这一在SCI中需要严重关注的问题 。
这项研究为CLV的潜力提供了令人信服的首次人体证据。作者承认研究存在局限性,例如缺乏神经调质参与或可塑性的直接生物标志物,这些标志物未来可能有助于个性化刺激参数 。需要更大规模的试验来确认这些发现,进一步探索恢复的预测因素,并评估长期益处 。
07
相关研究与产品
CLV在SCI领域的成功与VNS在其他神经系统疾病中日益增多的研究相一致。MicroTransponder公司(现为Vivani Medical的一部分)的VNS系统 (Vivistim® Paired VNS™ System) 已获得FDA批准 [2],用于改善慢性缺血性卒中幸存者在配合康复治疗时的上肢运动功能。这一在卒中治疗领域的监管成功,其效应量与当前的SCI研究相当,为VNS在SCI领域的应用铺平了道路。本研究中使用的设备由XNerve Medical Inc.开发,凸显了VNS硬件领域的持续创新。
硬膜外电刺激 (EES):ONWARD Medical公司正在开发EES系统,向脊髓本身提供靶向刺激。他们的ARC-EX®疗法用于上肢功能恢复,ARC-IM®用于血压调节和躯干稳定性,均在临床试验中显示出有希望的结果,一些个体在刺激激活时恢复了运动和自主神经功能 [3]。正如Grégoire Courtine实验室等的研究所示,这种方法通常侧重于在刺激激活时实现损伤平面以下的自主运动。
脑-脊髓接口 (BSI):研究人员在脑机接口 (BCI) 方面也取得了进展,BCI能够从大脑活动中解码运动意图,并将其转化为对脊髓或肌肉的刺激。今年3月3日,由复旦大学类脑智能科学与技术研究院加福民团队全球首创的“三合一”脑脊接口技术在复旦大学附属华山医院成功实施了全球首批第4例、通过脑脊接口让瘫痪者重新行走的临床概念验证手术。虽然这一技术在全球几乎没有任何经验可以采纳,但是实验结果令人印象深刻 [4]。
经皮脊髓刺激 (tSCS):非侵入性方法如tSCS也正在被探索,与植入式设备相比,其准入门槛更低,尽管其精确度或功率可能稍逊一筹。V. Reggie Edgerton等人的研究在这一领域奠定了基础 [5]。
神经生物制剂与细胞疗法:作为神经调控的补充,对生物制剂(如神经生长因子)或细胞移植(如神经干细胞)的研究仍在继续,旨在促进再生或为恢复创造更有利的环境。
CLV方法的独特之处在于,它旨在通过精确定时的神经调控与患者在康复训练中的积极参与相结合,诱导现存的、 spared 神经回路发生持久的可塑性改变。它更侧重于增强神经系统自然的恢复能力,而非简单地绕过损伤。
这项利用微型化和自动化VNS系统的研究的成功,有力地证明了组合疗法——智能地将神经刺激与强化、个性化的康复训练相结合——是开启慢性脊髓损伤患者更大程度恢复的关键。随着这些技术的成熟和融合,曾经被认为是静态的SCI预后,或许将被改写。
▼参考资料
[1] Kilgard, M.P., Epperson, J.D., Adehunoluwa, E.A. et al. Closed-loop vagus nerve stimulation aids recovery from spinal cord injury. Nature (2025). https://doi.org/10.1038/s41586-025-09028-5
[2] https://www.microtransponder.com/
[3] https://www.36kr.com/p/2930737633565572
[4]https://news.fudan.edu.cn/2025/0304/c4a144336/page.htm
[5] https://www.liebertpub.com/doi/10.1089/neu.2017.5082
END 编辑 | 罗虎 排版 | 罗虎 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊,参与线上线下交流活动
点击关注医工学人 最新直播

本篇文章来源于微信公众号: 医工学人