星标“医工学人”,第一时间获取医工交叉领域新闻动态~

帕金森病患者在行走时,大脑究竟发生了什么?传统脑机接口研究受限于实验室环境,无法回答这一问题。如今,加州大学旧金山分校团队首次在完全植入式设备上,实现了对患者居家自然行走状态的实时、高精度解码。2026年2月13日,这项发表于《科学进展》的研究不仅揭示了真实世界中的步态神经编码机制,更证明了利用现有植入设备进行“按需”闭环神经调控的临床可行性,为运动障碍疾病的精准治疗开辟了新路径。
对于数百万帕金森病患者而言,最困难的症状往往不是静止时的震颤,而是行走时的艰难——冻结步态、平衡障碍、起步困难。这些症状严重影响着他们的生活质量,却是现有治疗手段最难攻克的堡垒。
理论上,脑深部电刺激可以通过调节异常神经活动来改善这些症状。但一个根本性的困境在于:现行的DBS设备是“开环”的——它们以固定参数持续刺激,无论患者是在睡觉、静坐还是行走。然而,大脑本身是动态的。研究早已证实,皮质-基底节网络的振荡活动会随着运动状态和药物状态发生剧烈变化。用治疗静止期症状的参数去应对行走期,无异于刻舟求剑。
为什么不能实现“按需刺激”?答案在于解码的缺失。要实现在患者开始行走时自动切换到“行走模式”,首先需要设备能准确判断“患者正在行走”这一状态。
过去,这依赖于复杂的机器学习算法和实验室环境:患者被电线束缚,在跑步机上执行标准任务,算法在外部电脑上运行。这种模式存在三大致命缺陷:
非自然:实验室里的行走无法复现真实世界中转向、避障、因情绪而变的复杂步态。
不可持续:受限于设备,无法进行数天乃至数周的连续监测。
无法转化:复杂的算法无法植入到功耗和算力受限的微型植入设备中。
如何将神经解码从实验室解放出来,让它走进患者真实的家,成为实现自适应DBS必须跨越的鸿沟。
这项研究的核心突破,在于搭建了一条完整的、从数据采集到片上解码的真实世界神经解码流水线。它巧妙地结合了现有技术与创新的方法论,让“读懂自然行走”成为可能。
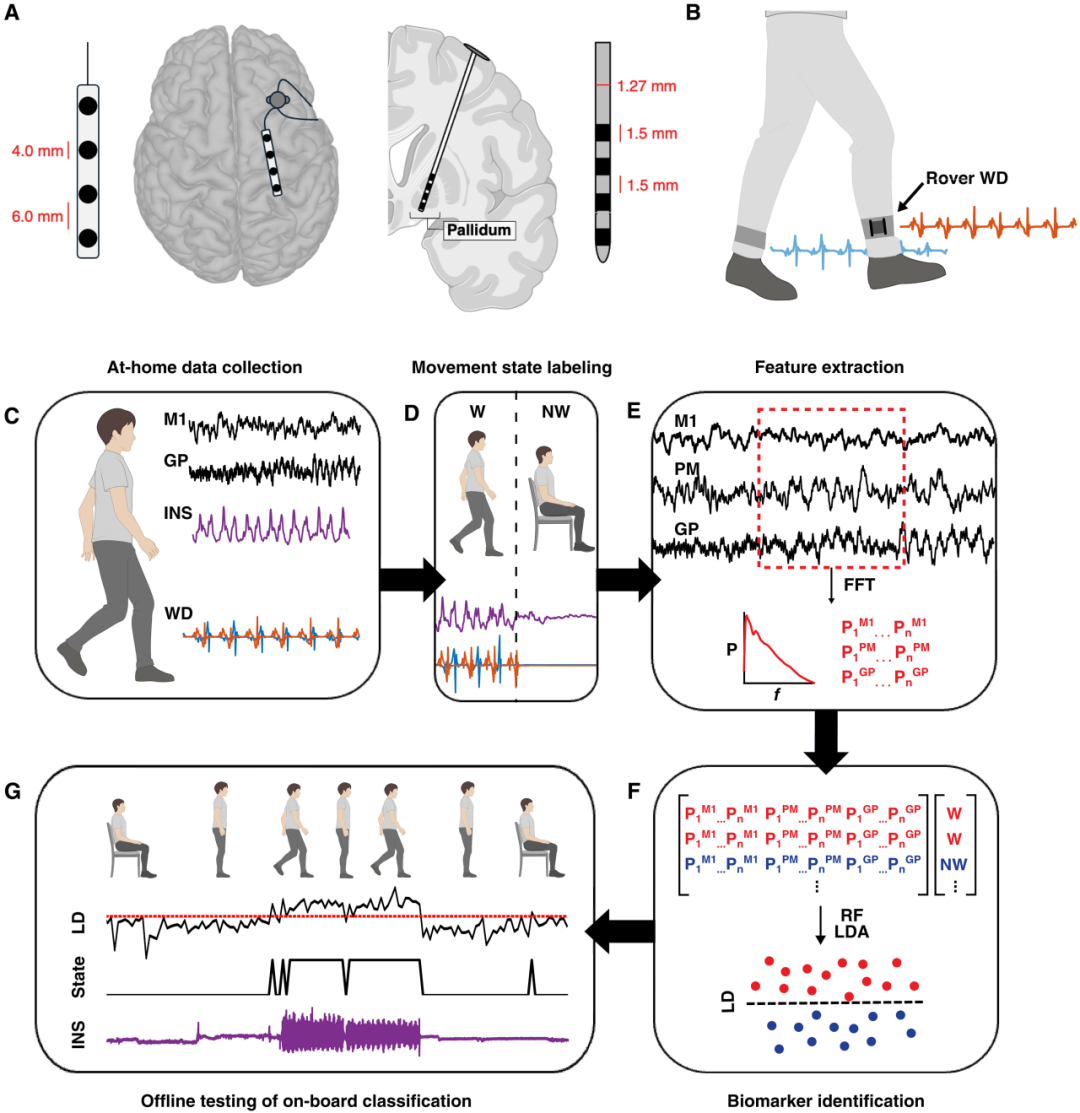
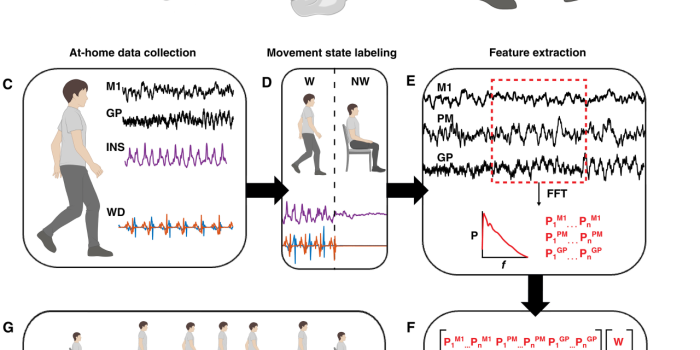
图 1. 帕金森病居家运动状态的皮质-苍白球神经生物标志物识别流程。
(A) Summit RC+S 双向神经刺激器的皮质电极(覆盖于 M₁ 和 PM 上方,左图)和植入苍白球(GP)的皮质下深度电极(右图)示意图。
(B) 双侧佩戴于脚踝的 Rover 加速度计可穿戴设备(WD)示意图。展示了来自左脚和右脚的样本加速度信号。
(C) 从患者家中流式传输来自 M₁、PM 和 GP 的神经数据以及来自可穿戴设备和 INS 的加速度数据。
(D) 加速度信号经过对齐,划分为 10 秒长的时段,并使用可穿戴设备数据标记为持续行走(W)或非行走(NW)时段。
(E) 从每个时段中,计算 1 至 50 Hz 范围内所有可能频段的平均功率。
(F) 这些功率值特征被用于训练和测试线性判别分析(LDA)模型。
(G) 最后,使用从居家数据中得出的、受系统约束的生物标志物,进行模拟的片上运动状态分类测试。
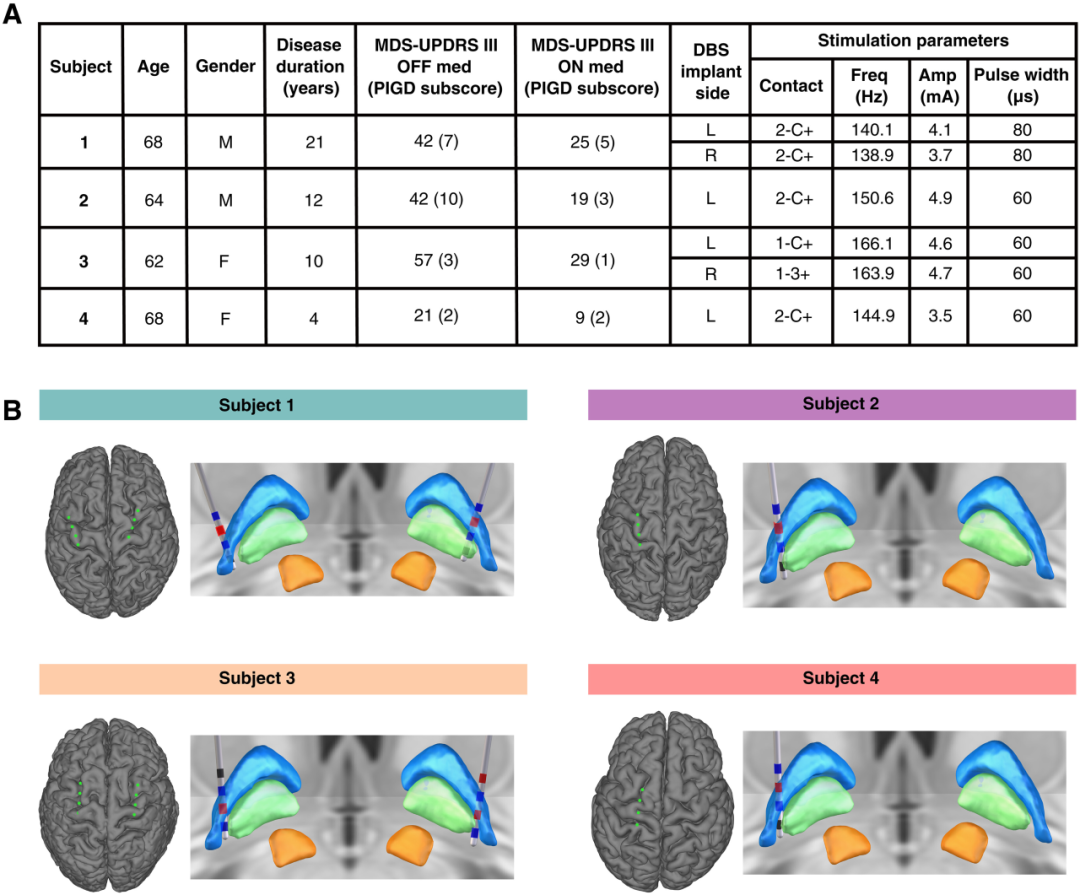
图 2. 受试者人口统计数据与电极定位。
(A) 展示了参与本研究的四位受试者的人口统计学和临床特征。
(B) 展示了针对特定受试者的、靶向 M₁ 和 PM 的皮层脑电图(ECoG)触点以及靶向 GP 的深度电极的重建图像。刺激触点用红色表示,记录触点用蓝色表示。C,病例;F,女性;L,左侧;M,男性;R,右侧。
“同步记录”的居家实验室:研究团队让4位植入Summit RC+S(一种具备感知功能的实验性DBS设备)的帕金森病患者,在居家生活中同时佩戴踝部运动传感器。通过在超过80小时的无监督活动中,将大脑(运动皮层M1/PM、苍白球GP)的场电位信号与身体(双脚)的运动学数据精确同步,他们首次捕捉到了真实行走时的大脑活动快照。
寻找“个性化指纹”:传统分析只看几个固定频段(如13-30Hz的β频段),但研究发现,每个人的“行走脑电指纹”都不同。团队采用随机森林模型,以1Hz为滑动窗口,在1-50Hz范围内扫描,识别出对区分“行走”与“非行走”最重要的个性化窄频带。例如,有些人的关键特征在苍白球的δ/θ频段(与运动启动相关),而另一些人的关键特征则在运动皮层的β频段(与感觉运动抑制相关)。
“芯片上的解码器”:最大的工程挑战在于,Summit RC+S芯片内置的线性判别分类器只能接受最多4个输入特征(且每个通道不超过2个)。这与动辄数十个特征的复杂模型相去甚远。团队将从居家数据中筛选出的最关键的1-4个窄带特征,输入到芯片的模拟环境中进行测试。结果表明,仅用3-4个特征,就能在芯片上实现AUC值最高达0.81的实时行走状态分类。
核心论断:这项技术的精髓不在于发明了新的大脑传感器,而在于创造了一套方法论,教会了现有的“智能”植入设备如何在真实世界中倾听患者,并用它们自己能理解的“简单语言”(4个特征)做出精准判断。
研究团队通过层层递进的实验设计,验证了这套方法的有效性和鲁棒性。
传感器验证:首先,他们验证了踝戴式运动传感器在患者群体中识别步态的准确性。结果显示,其平均准确率超过95.8%,甚至高达99.0%,为后续的神经数据分析提供了可靠的“地面实况”标签。
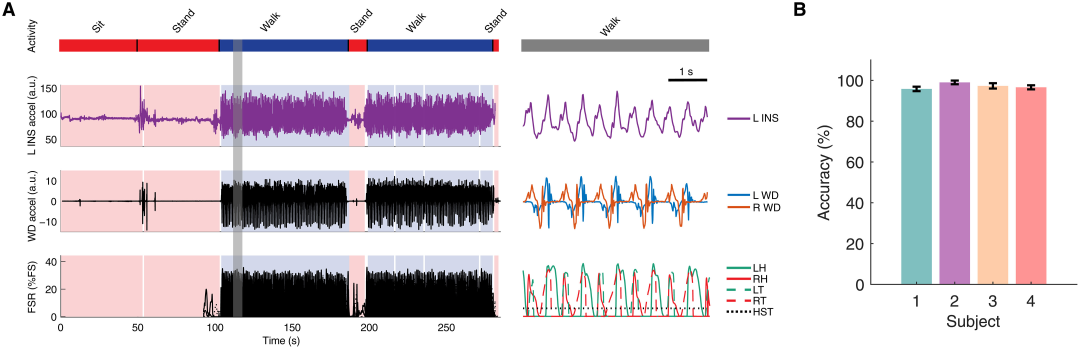
图 3. 可穿戴设备(WD)标记行走与非行走时段准确性的验证。(A) 在一次时长 300 秒、包含地面行走并穿插站立或静坐休息时段的实验过程中,展示了来自左侧 INS 和双侧可穿戴设备(WD)的加速度信号,这些信号与受试者足部力敏电阻器(FSR)的力信号对齐显示。顶部的颜色条指示了整个过程中受试者的行为(蓝色,行走;红色,非行走)。灰色方框标出的一个 5 秒连续行走时段已在右侧子面板中放大显示。(B) 展示了针对特定受试者的、基于可穿戴设备(WD)的运动状态标记的平均准确率(图 S2B)。误差线代表标准差。a.u.,任意单位;FS,力信号;HST,足跟触地阈值;LH,左脚跟;LT,左足趾;RH,右脚跟;RT,右足趾。
神经特征发现:通过分析同步的神经与运动数据,他们发现了一些有趣的共性规律:在所有受试者中,行走期间的运动皮层(M1)α和β频段功率均显著降低。这验证了运动时感觉运动皮层处于“去同步化”或活跃状态的经典理论。但在更深层的苍白球(GP)中,模式则因人而异:有的患者GP的β功率在行走时降低,有的反而升高。这揭示了基底节在步态控制中的复杂性和个体差异性。
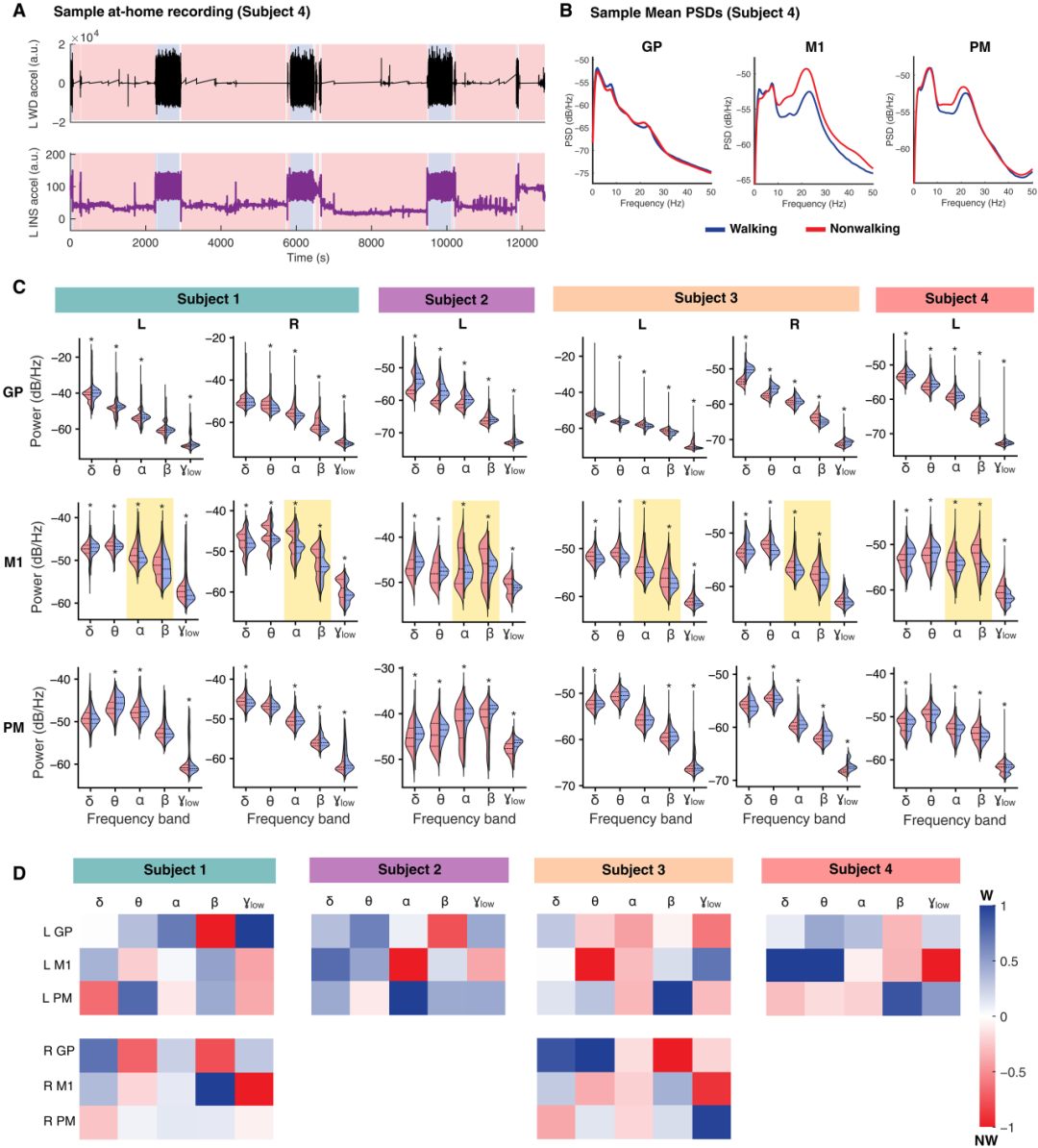
图 4. 居家行走与非行走时段的频谱分析。
(A) 展示了来自受试者 4 的样本居家记录,其中左侧可穿戴设备(WD,上图)和植入式神经刺激器(INS,下图)的加速度信号已对齐。基于可穿戴设备标记确定的行走时段(蓝色)和非行走时段(红色)已用阴影标出。
(B) 展示了受试者 4 的苍白球(GP)、M₁ 和运动前区(PM)所有分析的行走(蓝色)与非行走(红色)10 秒时段的样本平均功率谱密度(PSD),频率范围为 0 至 50 Hz。
(C) 小提琴图比较了所有 10 秒非行走(红色)与行走(蓝色)时段内每个经典频带的平均功率。使用了双侧 Wilcoxon 秩和检验,并采用 Benjamini-Hochberg 法对多重比较进行校正。在所有半球中,M₁ 的 α 和 β 频带功率在行走时段显著降低,已用黄色框突出显示。*P<0.05(表 S3)。
(D) 展示了所有半球的运动状态逻辑回归分类器的归一化平均特征系数(表 S4)。δ,1 至 4 Hz;θ,4 至 8 Hz;α,8 至 13 Hz;β,13 至 30 Hz;γ_low,30 至 50 Hz。
片上解码性能:最关键的一步——模拟芯片解码。当使用仅含3-4个特征的个性化生物标志物时:
-
在居家数据上测试:所有半球均实现了高于偶然水平的解码性能,最佳AUC达0.81。
-
在独立的实验室数据上验证:用居家数据训练出的模型,在实验室的验证性行走任务中同样表现良好,最佳AUC达0.87,证明了这些从真实世界学到的“生物标志物”具有良好的泛化能力。
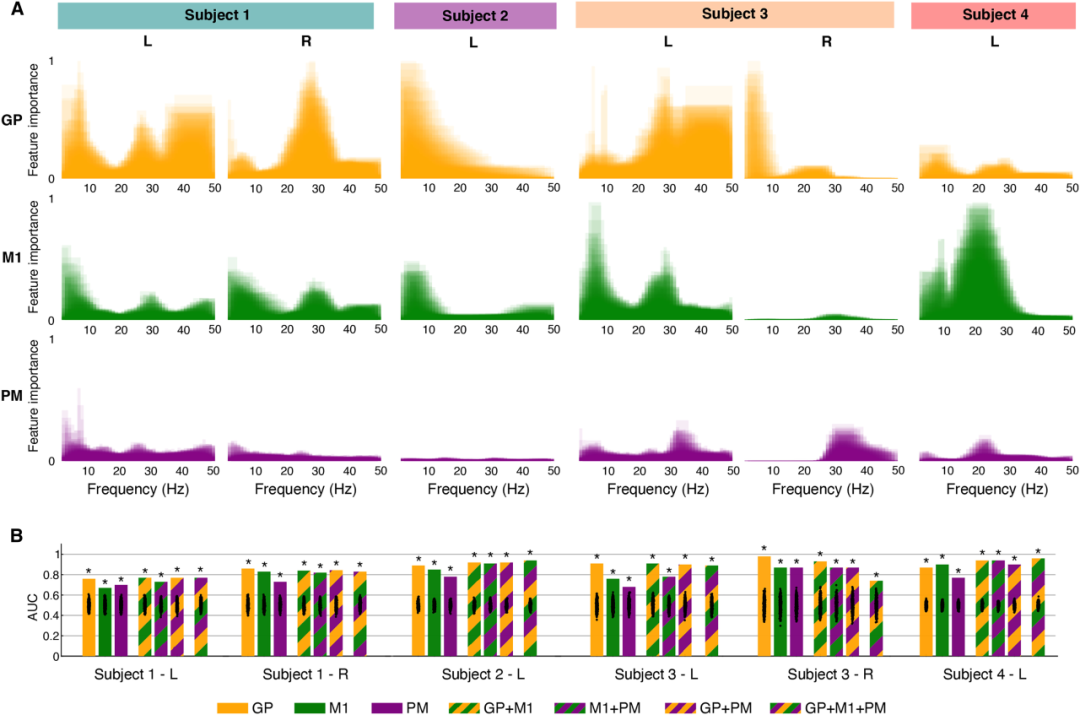
图 5. 受试者特异性运动生物标志物的识别。(A)展示了基于 1000 次随机森林(RF)迭代的基尼不纯度平均下降(MDI)所得到的、所有皮质-苍白球频带的归一化特征重要性。(B)展示了每个半球及每种模型类型(单区域、多区域和全区域)的线性判别分析(LDA)运动状态分类器性能。黑点表示经过置换得到的偶然水平性能(n=1000),这些用于计算单侧经验P值。
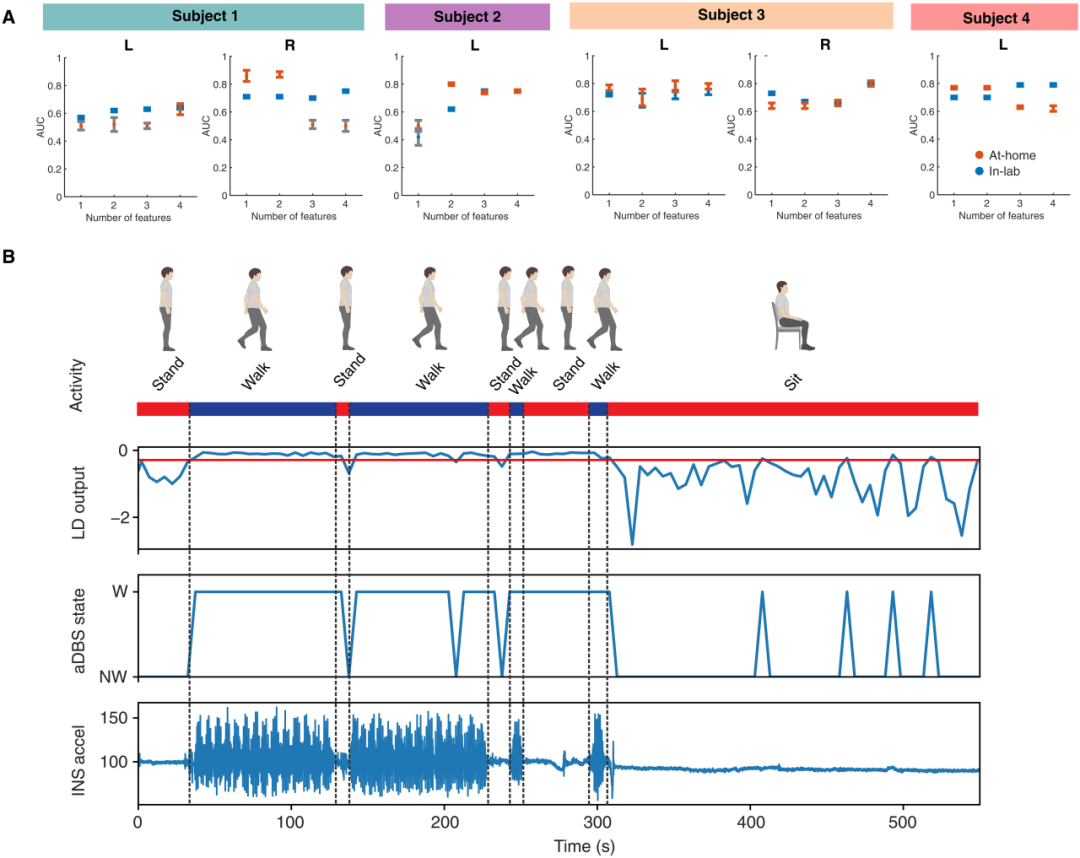
图 6. 片上运动状态分类的测试。
(A) 展示了模拟片上线性判别分析(LDA)分类器在两种数据集上的测试性能:在居家数据上测试的模型(蓝色)以及在实验室内观察到的、穿插站立或静坐休息时段的地面行走试验中进行验证测试的模型(橙色)。经验单侧 PP 值是通过将模型性能与经过置换的偶然水平分布(n=1000)进行比较计算得出的(表 S7)。统计上不显著的模型(P≥0.05)以灰色柱状图显示。
(B) 展示了针对受试者 1、使用从居家数据导出的生物标志物进行的连续片上分类(采用 5 秒时段)的样本可视化。展示了一次观察到的试验,顶部的颜色条指示了真实的运动状态。模拟的线性判别(LD)输出如图,红线指示阈值,其后依次为相应的自适应脑深部电刺激(aDBS)状态和真实的植入式神经刺激器(INS)加速度信号。
这些数据有力地证明:即便是在不受控的、充满干扰的居家环境中,使用设备自身的简陋芯片,也足以稳定地解码出患者的行走状态。
这项研究的价值远不止于“解码行走”。它为整个神经调控领域指明了方向。
-
对帕金森病治疗:从“持续刺激”到“按需刺激”:这是迈向自适应DBS最关键的一步。未来的DBS设备可以内置两套参数:一套用于静止期(控制震颤、僵硬),一套用于行走期(优化步态、预防冻结)。当芯片上的解码器检测到患者开始行走,便能自动切换参数,实现真正的“个性化动态治疗”。
-
对脑机接口行业:开启“现实世界神经科学”:这项研究证明,通过结合植入设备和可穿戴传感器,在真实世界中长期、稳定地研究人类大脑功能是可行的。这为研究其他复杂行为(如语言、社交、情绪波动)的神经基础打开了大门,有望催生新一代的生态效度更高的BCI解码框架。
-
对商业化的启示:研究使用的Summit RC+S是美敦力公司的实验设备。这项工作直接证明了现有硬件通过算法升级就能实现更智能的治疗,这将极大激励医疗器械公司加速推进下一代自适应设备的研发和审批。同时,它也强调了多模态数据融合(神经+可穿戴)在神经疾病管理中的巨大商业潜力。
尽管成果令人振奋,但作为一篇严谨的科技报道,我们仍需指出其通往临床普及之路上的障碍。
-
样本与普适性:研究仅包含4位患者。虽然这是侵入性研究领域的常规规模,但个体间巨大的差异性(图5A清晰地展示了这一点)意味着,我们发现的“规律”可能只是冰山一角。更复杂的步态问题,如冻结步态,其解码难度将呈指数级上升。
-
对齐的瓶颈:目前神经信号和运动信号的对齐仍需大量人工校准。要实现规模化应用,必须开发出设备间的自动蓝牙同步功能,否则数据处理将成为难以逾越的瓶颈。
-
商业化的距离:虽然证明了片上解码的可行性,但当前商用设备的计算能力和可编程特征集仍非常有限。研究团队使用的特征计算方式是“离线模拟”,与设备内部的实际运算可能存在差异。真正转化为可编程的商用产品,还需硬件迭代和严格的临床验证。
-
伦理与责任:当设备开始根据患者状态自动调整刺激时,谁来为潜在的“误判”负责?如果一个错误的“非行走”判断导致患者在家中行走时失去了应有的步态支持,风险将由谁承担?这不仅是技术问题,更是监管和伦理问题。
总而言之,这项研究为脑疾病治疗打开了一扇充满希望的窗。它证明了“智慧大脑”的第一步,是让植入设备学会倾听大脑在真实世界中的细语。尽管前路漫漫,但我们已经找到了正确的方向。
Rithvik Ramesh et al. ,At-home movement state classification using totally implantable cortical-basal ganglia neural interface.Sci. Adv.12,eadz4733(2026).DOI:10.1126/sciadv.adz4733
END
撰文 | 郝娅婷
排版 | 王可豪
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
Nature biomedical engineering |从图像到视频,从报告到对话:牛津大学团队首个胎儿超声视觉语言模型如何重构超声培训范式
npj flexible electronics | 柔性纤维电极:韩国团队实现抗弯抗洗、可同时监测多部位的无源织物传感
点击关注医工学人
直播预告


本篇文章来源于微信公众号: 医工学人