星标“医工学人”,第一时间获取医工交叉领域新闻动态~

在现代外科学中,尽管手术室内的精密设备已能实现对生命体征的极致掌控,但患者在离开手术台后的前几周——即围手术期恢复的关键窗口——却往往处于一种监测上的“断层”状态。目前的临床痛点在于,术后并发症如器官缺血、移植物排斥或胃肠道功能障碍往往隐匿于深层组织中。现有的监测手段存在显著的“时滞性”与“非特异性”:基于血压、心率的宏观体征评估难以察觉局部器官的早期生化波动;而周期性的血液化验则如同“事后诸葛亮”,当血清指标异常时,局部组织往往已遭受不可逆的损伤。
为攻克这一难题,达特茅斯学院(Dartmouth College)Wei Ouyang 教授团队近期在《自然-生物医学工程》(Nature Biomedical Engineering)上发表了一项里程碑式研究,题为“A programmable bioresorbable electrochemical microneedle sensor array for perioperative monitoring of organ health”(一种用于围手术期器官健康监测的可编程生物可吸收电化学微针传感器阵列)。研究团队开发了一套集成了柔性电子、生物可降解材料与多模态传感技术的新型系统。这不仅是对现有植入式设备的修补,更是一次从材料架构到监测范式的彻底革新。通过赋予设备“空间映射、按需消亡、多维感知”的协同特性,该系统旨在为深层器官提供连续、实时且精准的生化图谱,彻底规避了二次手术取出的临床负担。

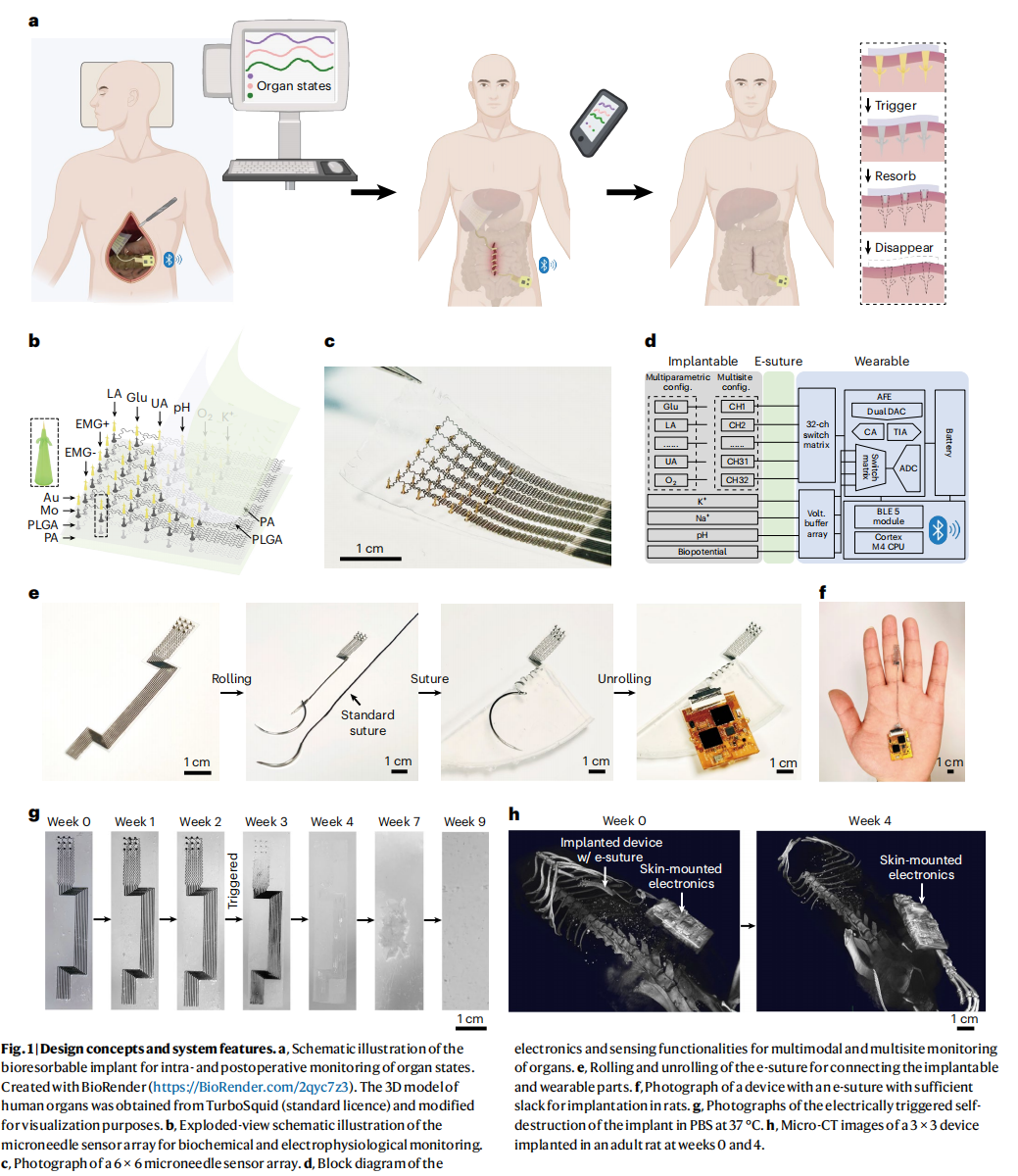
该系统的核心理念在于其“集成化与可编程性”,标志着深层器官监测从刚性、永久性植入物向柔性、瞬态电子系统的跨越。其创新点主要体现在以下四个维度:
三元集成架构(3D-B-A):
系统由可编程的微针阵列、柔性电子缝合线(e-suture)及体外无线电子模块组成。这种“内外联动”的设计将复杂的信号处理留在体外,而将极其微创的传感触点深入器官实质。
电子缝合线技术:
团队创新性地将多达 32 个并行的钼(Mo)导线集成在聚乳酸-羟基乙酸共聚物(PLGA)基底中。这种 e-suture 不仅提供了稳定的电学通道,还具备标准手术缝合线的机械性能,其特有的“松弛(slack)”设计能有效抵消呼吸和器官蠕动带来的拉拽力。
按需降解机制:
不同于传统设备依赖自然水解,该系统引入了电编程自毁机制。通过施加微小的过电位,金属保护层会迅速氧化消融,暴露出易水解的核心,使设备在完成天关键监测期后,于数周内完全消失在人体新陈代谢中。
无光刻 3D 打印制造:
突破了传统光刻工艺难以制造复杂三维形貌(如倒钩结构)的局限。团队利用高精度 3D 打印与“变形耦合”技术,实现了微针长度与传感器功能的个性化编程,显著降低了制造门槛与成本。

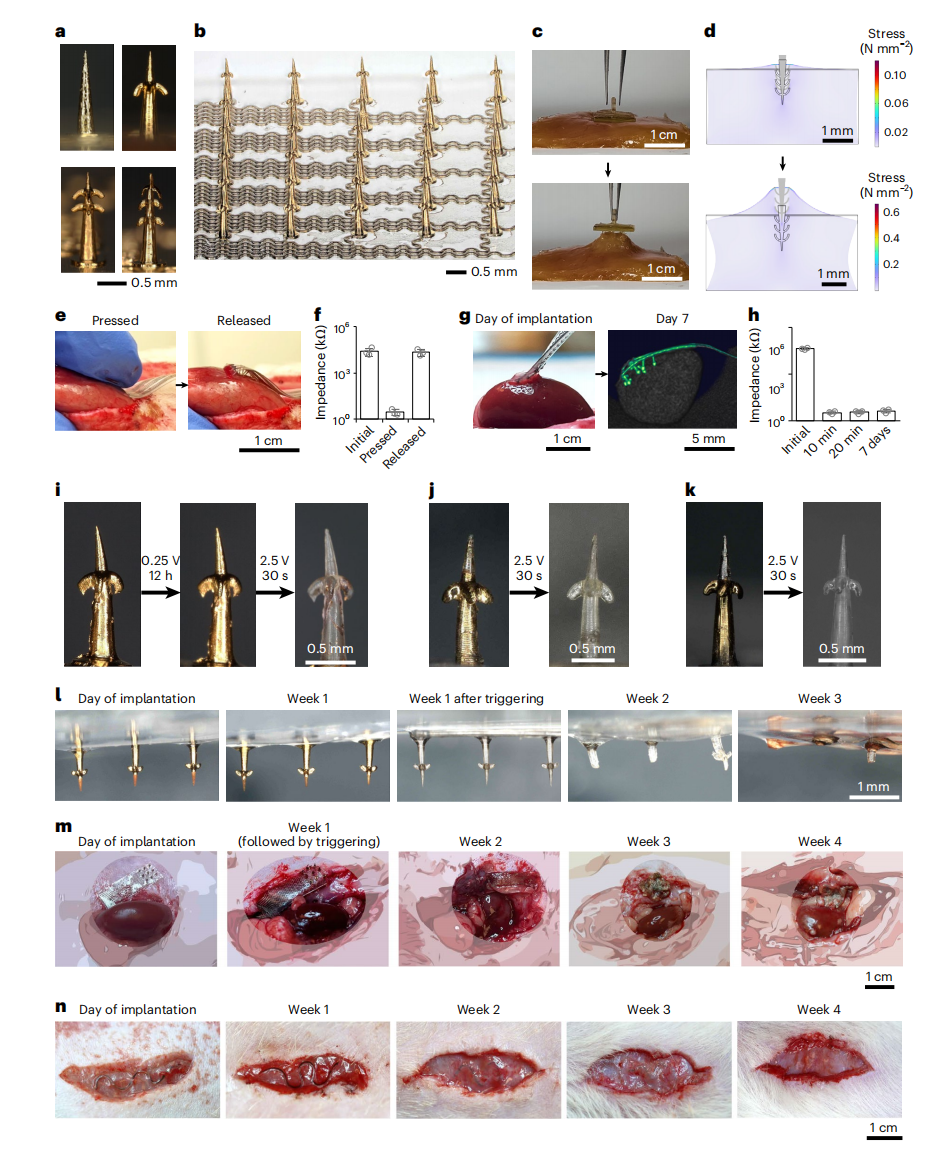
植入式设备在蠕动器官(如肾脏、肠道)上的附着力是长期监测的前提。研究团队受生物启发,设计了具有向后倒钩(backward-facing barbs)的微针。力学测试显示,相比于易脱落的平滑微针,单排倒钩的临界拔出力提升至 12.2-18.1 mN,三排倒钩更是高达 61.7 mN,使组织附着力增强了 14-71 倍。在活体实验中,微针阵列在剧烈振动环境下(加速度 40m/s2)依然能保持约 1 毫米的稳定切入深度。
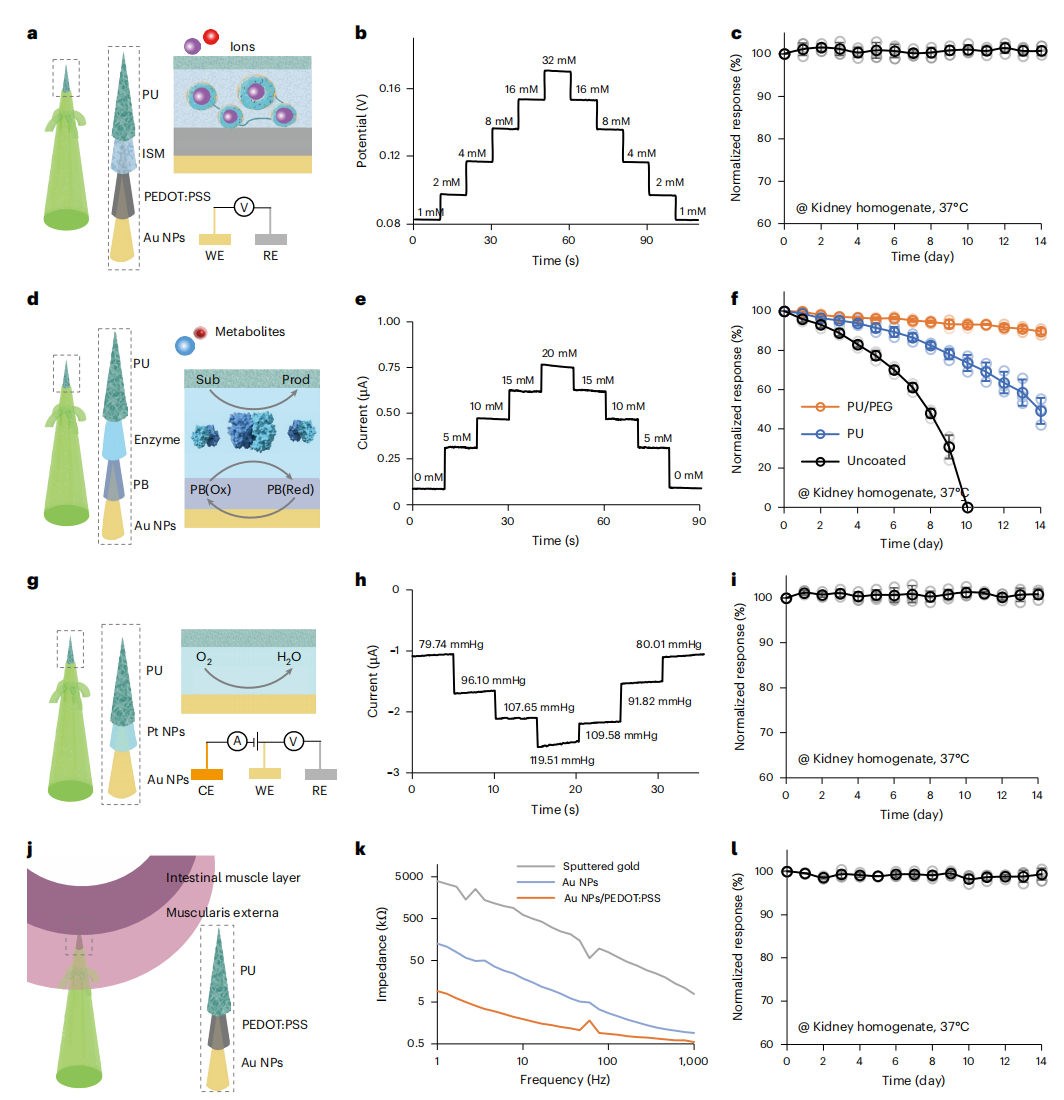
为了全面评估器官健康,系统集成了电位型和安培型两大类传感模态,涵盖了钾(K+)、钠(Na+)、pH、葡萄糖(GLU)、乳酸(LA)、尿酸(UA)及氧分压(PO2)。
性能优异:离子传感器展现出优异的 Nernst 响应K+(如 灵敏度达69.8mV/dec),代谢物传感器通过引入普鲁士蓝调节剂和金纳米颗粒(AuNPs),实现了高灵敏度与极佳的抗干扰能力。
长期稳定性:凭借创新的 PEG 修饰聚氨酯(PU)防污涂层,传感器在复杂的肾脏组织液中工作 14 天后,依然能保持约 90% 的响应,解决了生物传感器极易受生物膜干扰而失效的难题。
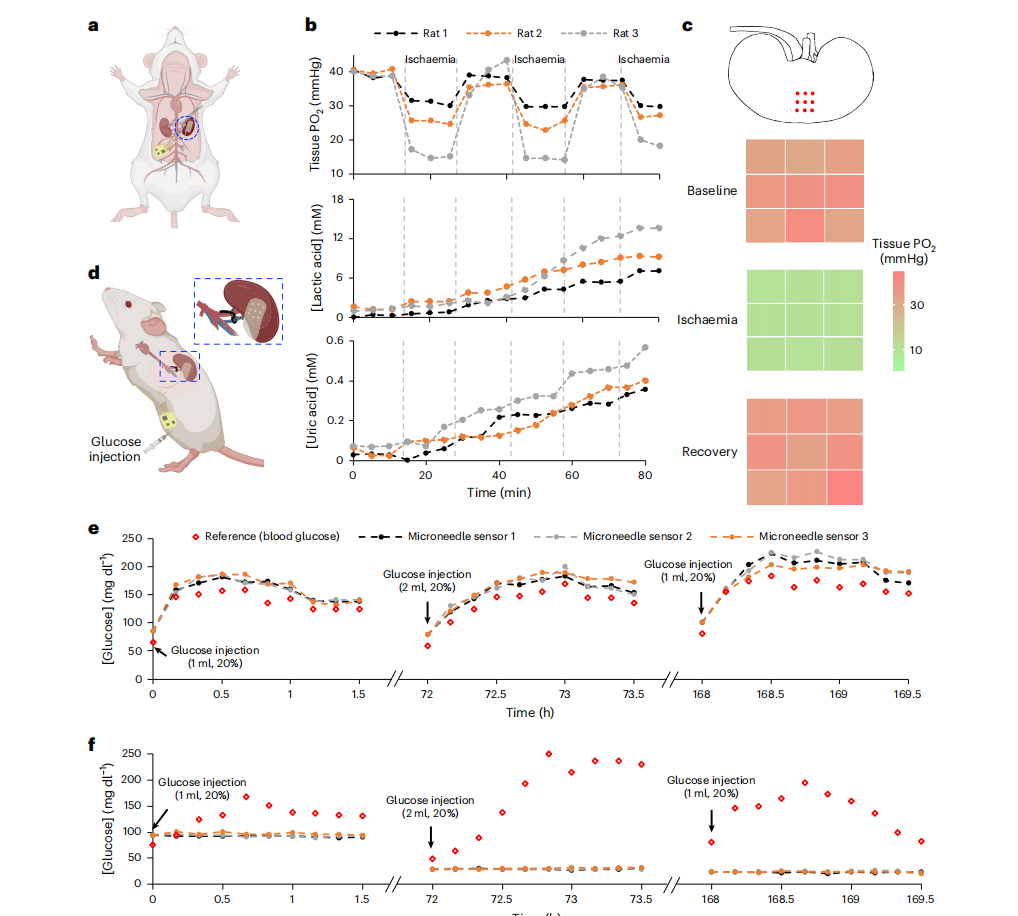
肾脏缺血监测:系统实时捕捉到了氧分压在血流中断后的断崖式下跌,并首次展示了肾皮质氧合浓度的空间异质性映射。
肠道功能评估: 微针阵列成功监测了肠道对营养物质(葡萄糖)的吸收动力学,并通过电生理传感器记录了肠道肌电图(EMG),为术后肠麻痹的恢复评估提供了量化依据。
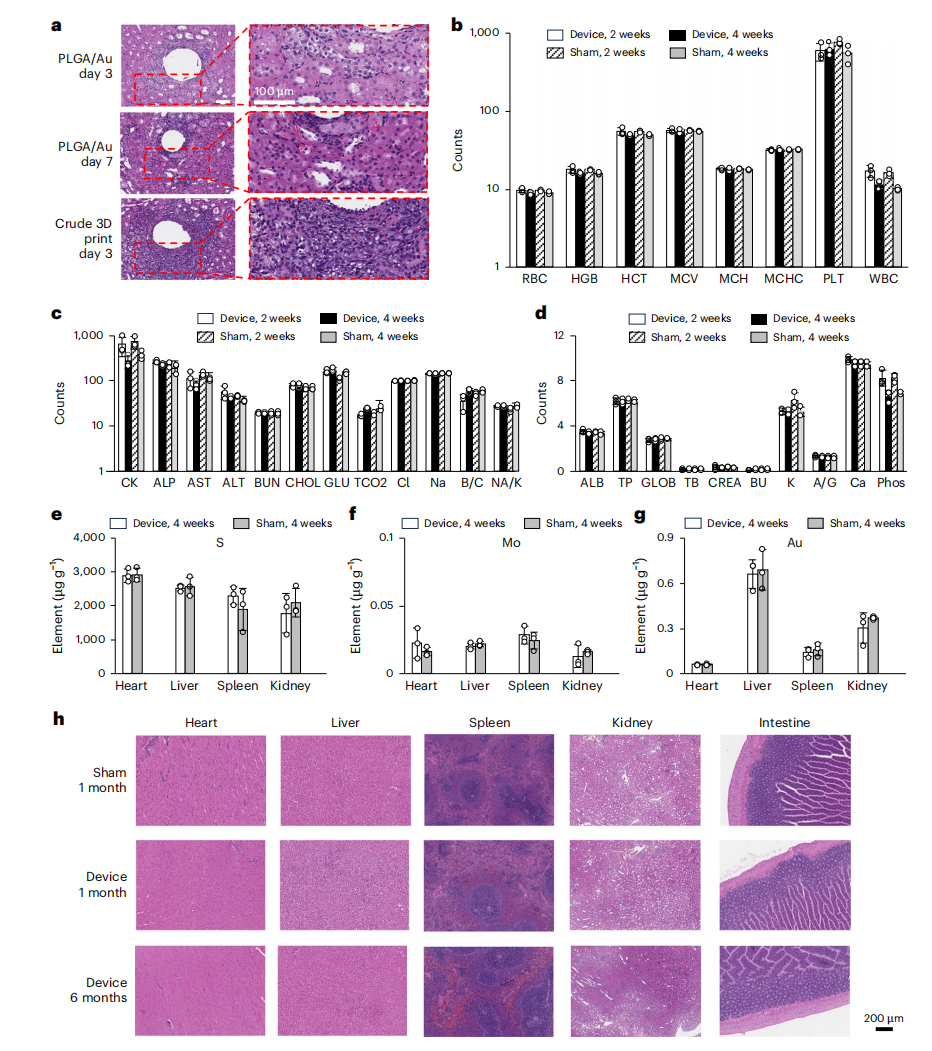
安全性是植入式设备进入临床的底线。研究团队进行了为期 6 个月的长周期跟踪,HE 染色和生化分析显示,降解产物(如金、钼等金属残留)仅处于纳克级水平,远低于毒性阈值,未引发系统性毒性或长期炎症反应。
在 2026 年的生物医学版图中,Wei Ouyang 教授的这项成果正处于瞬态电子学向产业化转型的最前沿。该系统直接对标了目前临床上昂贵且具有侵入性的连续监测方案,其“数字守护者”角色将对现有的围手术期管理模式发起有力挑战。
行业纵横: 相比于 John Rogers 团队(Northwestern)专注于超薄硅基物理传感器 或清华大学邢声教授(Xing Sheng)的光电神经接口 ,Ouyang 团队的研究在“深层器官、多模态生化、主动自毁”三个维度的结合上表现出了独特的临床实用价值。
商业化挑战与潜力: 尽管该技术在实验室表现卓越,但其商业化道路仍需跨越量产工艺的门槛。目前,诸如 Tensive(生物可降解支架) 和 4D Biomaterials(高精度可降解打印) 等公司正积极布局可降解植入材料领域。同时,MIT 实验室展示的智能缝合线技术也为该系统的 e-suture 组件提供了产业链配套的可能性。
未来愿景: Ouyang 教授指出,未来的方向是实现“全系统 100% 降解”并延长监测周期至数月。最终,这类器件将融入“物理 AI”范式:通过边缘计算自主分析生化趋势,并在检测到异常(如炎症因子升高)时,联动电子缝合线释放药物,实现从“实时监测”到“闭环治疗”的无缝衔接 。
达特茅斯学院的这项研究代表了生物电子学从“表面测量”向“器官内核探测”的一次质变。尽管面临生产转化挑战,但其赋予外科医生的“数字化视界”,极有可能在未来的器官移植、复杂腹腔手术等高风险领域,成为保障患者生命安全的基石。
https://www.nature.com/articles/s41551-025-01609-z
END
撰文 | 赵亚军
排版 | 王可豪
审核 | 医工学人理事会
扫码加入医工学人,进入综合及细分领域群聊,
参与线上线下交流活动

推荐阅读
Nature Biomedical Engineering | 苏黎世大学新研究:基于多模态数据集的3D计算机断层扫描通用基础模型
Microsystems & Nanoengineering | 告别扎针!新型“光学智能手表”结合等离激元纳米阵列,实现无创汗液血糖监测
点击关注医工学人

本篇文章来源于微信公众号: 医工学人










