星标“医工学人”,第一时间获取医工交叉领域新闻动态~

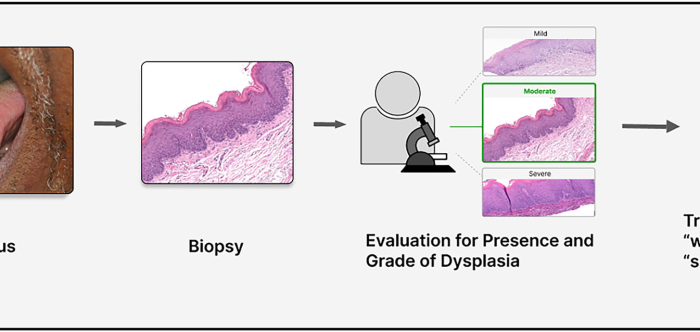
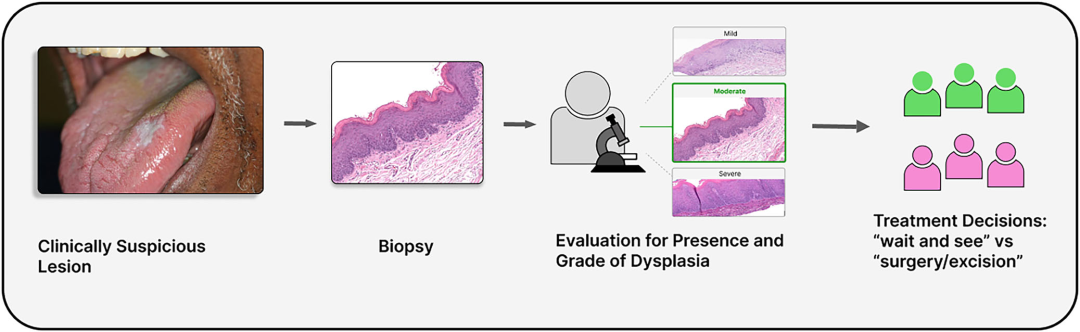
长期以来,临床决策依赖于WHO的三级异型增生(dysplasia)评分系统:轻度、中度、重度。这看似严谨的阶梯,实则充满了主观性的迷雾。一位病理学家眼中的“中度异型增生”,在另一位专家眼中可能就是“重度”或者“轻度”。这种观察者间的变异性(Inter-observer variability)导致了严重的临床困境:对于被标记为“重度”的患者,外科医生可能会挥动手术刀进行预防性切除,即便只有一半的概率会真正癌变;而对于“轻度”患者,医生往往选择“观察与等待”(Watch and Wait),却可能眼睁睁看着癌症在监测的盲区中悄然滋生。
现在,一场无声的革命正在打破这种僵局。罗格斯大学与匹兹堡大学的研究团队在 npj Digital Medicine 上发表的一项里程碑式研究,展示了人工智能如何通过模仿人类视觉的“变焦”机制,在预测口腔癌进展方面超越了传统方法。

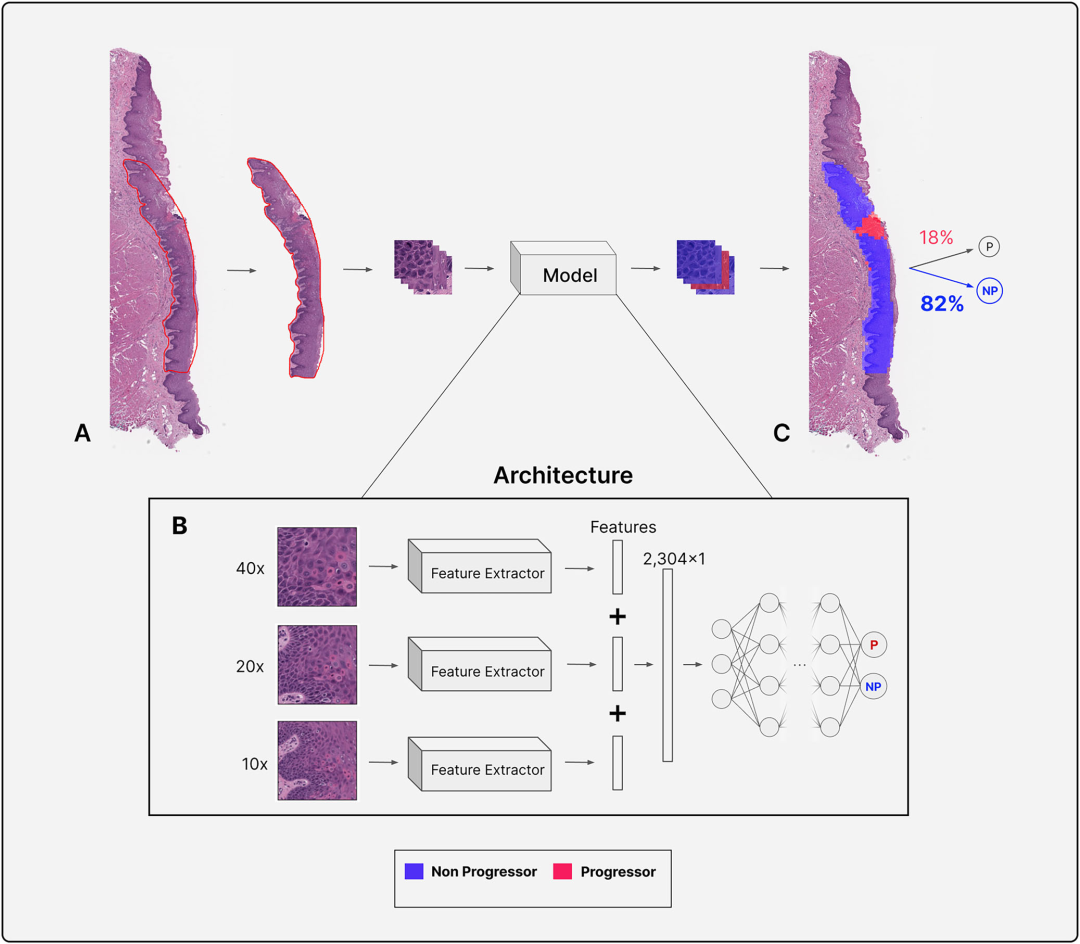
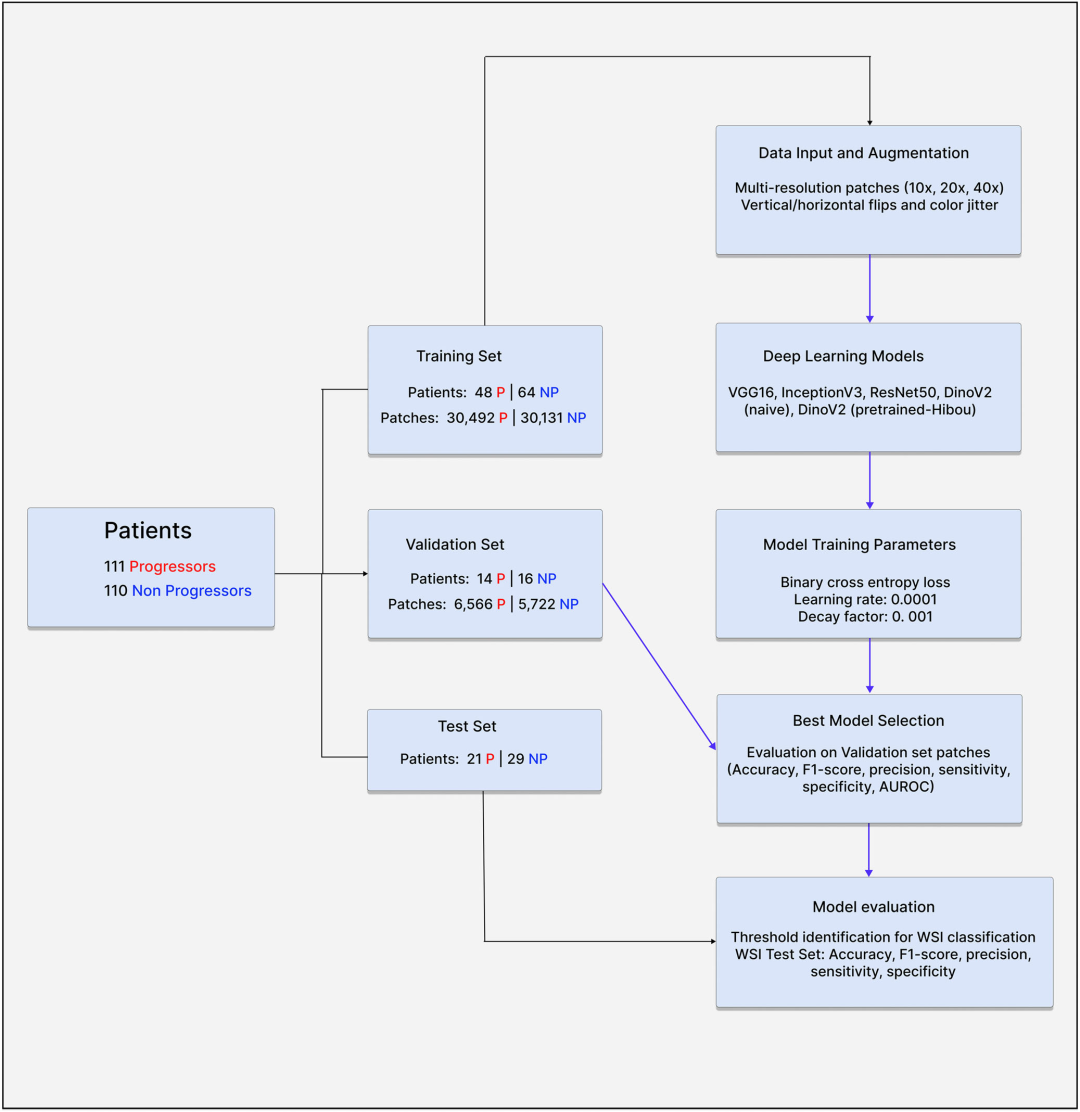
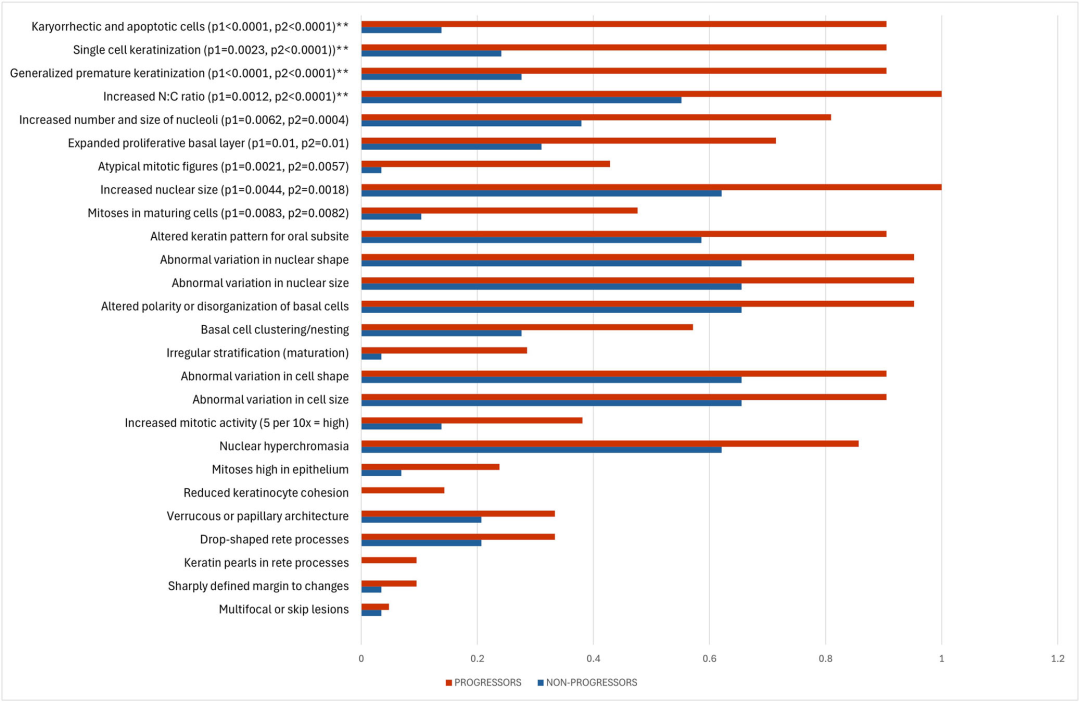
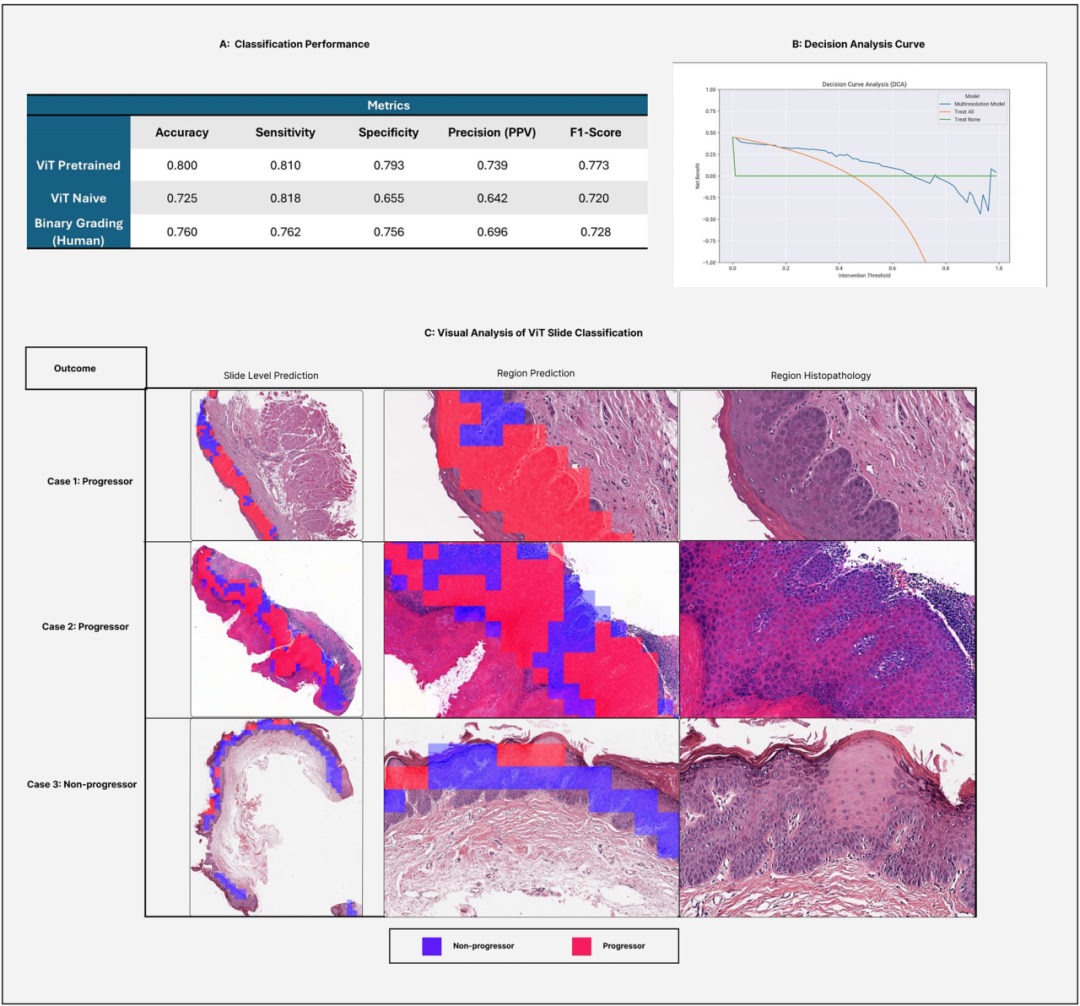
1.1 传统病理学的困境:主观性的迷宫 在深入探讨AI之前,我们必须先审视人类病理学家面临的挑战。口腔癌的发生是一个多步骤的过程,从基因突变到细胞克隆性扩增,最终表现为组织形态的改变。临床上,医生通过活检获取组织,病理学家在显微镜下寻找“异型增生”的迹象。然而,WHO的分级系统本质上是描述性的,它依赖于病理学家对细胞核异型性、角化异常和结构紊乱的综合感知。 研究指出,这种系统的主要缺陷在于其预测能力的匮乏。现有的三级评分系统在区分低风险与高风险进展者方面缺乏精确度。数据显示,约20-35%的重度异型增生和5-15%的轻中度异型增生会在未经治疗的情况下进展为癌症。这种不确定性使得临床管理陷入两难:过度治疗会导致不必要的面部毁容和功能丧失,而治疗不足则意味着错失挽救生命的最佳窗口。此外,病理学家之间的一致性(Kappa值)通常仅为0.41-0.5,这意味着两个专家对同一张切片的判断,有一半的时间可能是不一致的。 1.2 破局之道:多分辨率(Multiresolution)的哲学 为了解决这一问题,Liu-Swetz等人提出了一种全新的计算病理学框架。与以往仅仅依赖单一放大倍率(通常是20倍)的深度学习模型不同,该研究的核心创新在于“多分辨率”策略。 在病理诊断中,信息是分层级的。低倍镜(如10倍)展示了组织的宏观架构(Architecture),例如上皮层的厚度、基底膜的完整性以及上皮脚(Rete Ridges)的形态;中倍镜(如20倍)揭示了细胞间的排列关系;而高倍镜(如40倍)则暴露了细胞核内部的秘密,如核仁的大小、核分裂象的异常以及染色质的分布。人类病理学家在阅片时,会下意识地不断切换倍率,整合这些层级的信息。 该研究的AI模型完美复刻了这一过程。研究团队构建了一个多分辨率框架,同时摄取10x、20x和40x的图像切片(Patches)。这并非简单的数据堆砌,而是通过算法迫使模型学习不同尺度特征之间的非线性关联。 实验结果证实了这种策略的有效性。消融实验(Ablation Study)显示,随着分辨率主干网络(Backbones)数量的增加,模型的分类性能稳步提升。仅使用20倍镜时,准确率为67.6%;加入10倍镜后提升至70.2%;而当融合了10倍、20倍和40倍镜的数据时,准确率达到了最高值,F1分数也提升至73.2%。这有力地证明,就像人类需要结合宏观与微观视角一样,AI也需要“见树木亦见森林”。 1.3 架构之争:Vision Transformer (ViT) 对决 CNN 过去十年,卷积神经网络(CNN)如ResNet、VGG和Inception一直是医学图像分析的绝对统治者。然而,Liu-Swetz的研究揭示了CNN在病理学任务中的局限性。 CNN的核心机制是卷积操作,它具有平移不变性和局部感受野。这使得CNN非常擅长捕捉纹理和边缘特征,但在处理长距离依赖关系(Long-range dependencies)时显得力不从心。在全切片图像(WSI)中,一个切片可能包含数十万个像素,病变区域的基底细胞异常可能与远处的角化层变化存在内在联系。CNN受限于其局部感受野,往往难以捕捉这种跨越空间的全局关联。 Vision Transformer(ViT)的引入改变了游戏规则。ViT起源于自然语言处理(NLP),它将图像分割为一系列的“Token”(类似于句子中的单词),并通过自注意力机制(Self-Attention)计算每一个Token与其他所有Token之间的关系,无论它们在图像中的距离有多远。这种机制赋予了ViT天然的全局视野。 在本研究中,研究团队对比了VGG16、InceptionV3、ResNet50与基于DINOv2的ViT模型。结果显示,ViT模型(尤其是使用了Hibou预训练权重的版本)在几乎所有关键指标上都碾压了CNN模型。最令人震惊的差异体现在特异性(Specificity)上:CNN模型的特异性极低(约32%-44%),这意味着它们产生了大量的假阳性,容易将良性病变误判为高风险,从而导致过度治疗。相比之下,ViT模型的特异性高达64%以上,整体准确率达到80.0%,AUROC为0.798。 这一发现具有深远的理论意义:它暗示了在复杂的组织病理学图像中,全局的结构性特征(Architectural patterns)——那些需要长距离上下文才能理解的特征——对于预测恶性转化至关重要,而这正是ViT的杀手锏。 1.4 打开黑箱:AI眼中的癌症是什么样子? 为了让AI的预测具有临床说服力,必须解决“可解释性”问题。医生不能仅仅依赖一个黑箱输出的概率值,他们需要知道AI究竟看到了什么。研究团队进行了一项极具创新性的关联分析,将AI预测的高风险区域与人类病理学家识别的经典组织学特征进行对比。 三位病理学家对测试集进行了盲审,并对24种已知的异型增生特征进行了评分。结果令人振奋:AI预测为“高风险”的病例,与病理学家识别出的八大关键恶性特征高度重合(p<0.01)。其中,相关性最强的四大特征包括: 1.核破裂/凋亡细胞(Karyorrhectic/apoptotic cells): 代表细胞死亡和更新的异常加速。 2.单细胞角化(Single cell keratinization): 正常的角化应发生在上皮表层,单细胞在深层角化意味着分化程序的混乱。 3.过早角化(Premature keratinization): 同样是分化异常的标志。 4.核质比增加(Increased N:C ratio): 癌细胞的经典特征,细胞核增大,胞浆减少,反映了细胞增殖活性的增强 1。 这证明了AI并非在玩弄像素的概率游戏,而是在通过自监督学习,重新发现了病理学的核心规律。它不仅看到了人类能看到的特征,甚至可能捕捉到了人类肉眼难以量化的微微细变化(如基底细胞层的细微扩张或核形状的亚像素级变异)。 Liu-Swetz的研究虽然聚焦于口腔癌,但它实际上是整个计算病理学领域基础模型爆发的一个缩影。2024年至2025年,被称为病理学AI的“大模型元年”。正如GPT-4改变了自然语言处理,针对病理图像预训练的基础模型正在重塑癌症诊断。 2.1 从 ImageNet 到 DINOv2:预训练范式的跃迁 在过去,医学AI模型通常使用在自然图像数据集(如ImageNet,包含猫、狗、汽车等)上预训练的权重进行初始化(Transfer Learning)。然而,病理图像与自然图像存在本质区别:病理图像没有明确的前景与背景,纹理复杂,且旋转不变性(Rotation Invariance)要求极高(细胞无论朝向哪里都是细胞)。 DINOv2(由Meta AI开发)的出现改变了这一局面。它采用自监督学习(Self-Supervised Learning, SSL),不依赖人工标注,就能从海量无标签图像中学习到强大的视觉特征表示。Liu-Swetz的研究正是利用了DINOv2作为特征提取器,这使得模型能够在只有几百个标注病例的情况下,依然具备强大的泛化能力。 2.2 巨头争霸:Hibou, Virchow, UNI 与 H-Optimus-0 目前,全球顶尖的科研机构和科技巨头都在竞相发布自己的病理学基础模型,这场竞赛的核心指标是数据规模、多样性和下游任务性能。
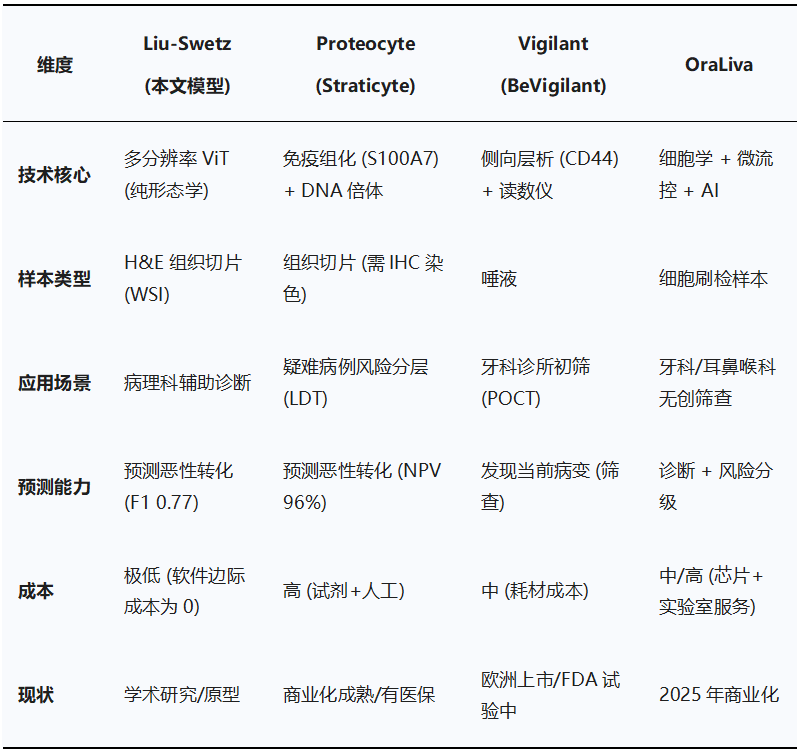
Liu-Swetz的研究虽然在学术界树立了标杆,但在商业化赛道上,已有多个成熟玩家布局了不同的技术路线。我们将口腔癌风险预测的竞争格局分为三大流派:生物标志物派、液体活检派和细胞学AI派。 3.1 生物标志物派:Proteocyte AI 与 Straticyte™ Proteocyte AI 是目前在该领域商业化进程最快的公司之一。他们没有选择纯形态学AI,而是通过分子生物学寻找更底层的证据。 ●技术原理: 其核心产品 Straticyte™ 是一种基于免疫组化(IHC)的风险分层测试。它检测关键生物标志物 S100A7 的表达水平,并结合图像细胞计数(Image Cytometry)分析DNA倍体(Ploidy)状态。S100A7在细胞核内的异常积聚被认为是上皮细胞恶性转化的早期预警信号。 ●临床性能: 临床验证数据显示,Straticyte在预测口腔潜在恶性病变进展方面的灵敏度高达96.2%,阴性预测值(NPV)为96.2%。这意味着它能极好地排除低风险患者,避免不必要的焦虑和手术。研究表明,Straticyte能够将65%被WHO分级为“轻度异型增生”的病例重新归类为高风险,这部分患者在5年内进展为癌症的概率是普通轻度患者的2.5倍。 ●商业壁垒: Proteocyte已获得UnitedHealthcare等主要保险公司的报销覆盖,并拥有多项核心专利。其“实验室自建项目”(LDT)的模式允许其在特定CLIA认证实验室提供服务,规避了部分FDA PMA审批的漫长周期。 3.2 液体活检派:Vigilant Biosciences 与 BeVigilant™ Vigilant Biosciences 选择了更为前端和便捷的赛道——唾液检测。 ●技术原理: 其产品 BeVigilant™ OraFusion™ System 利用侧向层析技术(类似新冠抗原试剂盒),检测唾液中的 CD44 和 总蛋白(Total Protein) 水平。CD44是一种跨膜糖蛋白,也是著名的肿瘤干细胞标志物,其可溶性形式在口腔癌患者唾液中显著升高。 ●产品形态: 这是一个椅旁(Point-of-Care)检测系统,只需15分钟即可出结果,通过简单的“监测”或“进一步检查”红绿灯信号指导牙医决策。 ●监管与市场: 该系统已获得FDA“突破性设备”(Breakthrough Device)认定,并依据IVDR法规在欧洲及部分亚洲市场(土耳其、马来西亚)获批上市。这使得Vigilant在初级筛查市场占据了先发优势。 3.3 细胞学AI派:OraLiva OraLiva 代表了最新的技术融合趋势,被称为“芯片上的细胞学”(Cytology-on-a-chip)。 ●技术原理: 与传统的切片活检不同,OraLiva使用无创的细胞刷(Brush Biopsy)收集口腔黏膜细胞。样本被送入基于微流控芯片的分析平台,利用AI算法分析数百万个单细胞的形态学特征(如核形态、生物标志物表达)。 ●优势: 相比切片活检,刷检无痛、无创,患者依从性极高。其AI模型在1300万个细胞图像上进行了训练,能够捕捉到单细胞级别的亚微观异型性。 ●商业进程: 公司计划于2025年Q4正式启动商业化,并正在推进FDA审批。 深度对比:Liu-Swetz 模型 vs. 竞品 结论: Liu-Swetz的模型凭借其基于标准H&E切片的低成本和高可及性,极有可能成为病理科的“标配”辅助工具,而Proteocyte和OraLiva则更多针对特定的高价值临床场景(如确诊困难或拒绝活检的患者)。
即使算法再完美,如果无法融入医生的工作流(Workflow),也只能是实验室里的玩具。Liu-Swetz的研究要真正走向临床,必须跨越数字化、监管和支付这三座大山。 4.1 数字化病理的基建赤字 虽然AI在飞速发展,但病理科的现实却相对骨感。截至2024年底,全球全面采用数字化病理(全切片扫描)的实验室比例仍不足30%,大部分仍停留在显微镜加玻璃切片的时代。 ●存储与算力的挑战: 一张40倍扫描的全切片图像(WSI)大小可达1-3GB。一家中型医院每年产生的病理数据量是PB级的,这对存储成本和传输带宽提出了巨大挑战。华为云EI Health 和腾讯AI Lab 等科技巨头正在通过开发极致无损压缩算法和分布式存储架构来解决这一痛点,力求实现1000+切片的秒级检索。 ●色彩归一化(Stain Normalization): 不同品牌的扫描仪(如Leica, Philips, Hamamatsu)以及不同实验室的染色工艺,会导致图像色彩存在显著差异。这种“域偏移”(Domain Shift)会严重影响AI模型的泛化能力。Liu-Swetz的研究中使用了OpenSlide进行标准化处理 1,但在真实多中心环境中,这依然是导致模型“水土不服”的主要原因。 4.2 FDA的监管风向:从“黑箱”到“透明” 美国食品药品监督管理局(FDA)对AI医疗器械的监管正处于快速演变中。 ●先例: 2021年,Paige Prostate 成为首个获得FDA批准(De Novo路径)的病理AI产品。这一里程碑事件为后续的病理AI确立了监管框架:FDA不仅关注模型的AUC值,更关注临床效用(Clinical Utility)——即AI是否真能帮助医生减少漏诊、提高一致性,且不增加诊断时间。 ●突破性认定: Viome和Vigilant均获得了FDA的“突破性设备”认定。这表明FDA高度重视口腔癌早期筛查技术,愿意为能显著改善预后的创新产品提供加速审评通道。Liu-Swetz的模型若要商业化,必须开展类似Vigilant正在进行的大规模多中心前瞻性临床试验,证明其在真实世界中的鲁棒性。 4.3 支付体系的破冰:CPT代码与报销 没有报销,就没有商业闭环。好消息是,美国医学会(AMA)和病理学家学会(CAP)正在积极推动数字病理的支付代码建设。 ●CPT Category III代码: 2024年,AMA新增了30个数字病理附加代码(0751T-0763T),用于报告数字化扫描相关的额外工作量。虽然III类代码通常不直接付费,但它们是收集成本数据、申请I类永久支付代码的必经之路。 ●价值导向支付: Proteocyte的Straticyte成功获得UnitedHealthcare报销是一个强烈的信号:支付方愿意为能“省钱”的技术买单。如果AI能证明通过精准分层,减少了不必要的手术(每次手术成本数万美元)和晚期癌症治疗费用,那么它就具备了极高的卫生经济学价值。
当AI学会了在显微镜下“变焦”,它看到的不仅是细胞,更是患者生命的延长线。从Liu-Swetz的多分辨率ViT模型,到HistAI的Hibou基础模型,再到Proteocyte和OraLiva的商业化探索,我们正处于口腔癌诊疗历史的一个转折点。 这是一场从“模糊”到“精准”,从“经验”到“计算”,从“切片”到“多模态”的范式转移。在这个过程中,AI不会取代病理学家,但正如那个著名的论断所言:“使用AI的病理学家,终将取代那些不使用AI的病理学家。”而对于患者而言,这意味着那个曾经令人战栗的“命运轮盘”,终于有了一丝被科学掌控的希望。
https://www.nature.com/articles/s41746-025-02014-1
END 撰文 | 赵亚军 编辑 | 余帆 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊,参与线上线下交流活动
推荐阅读
Nature Communications | “三维毛细血管CT”问世?新超声技术实现全器官微血管高清四维成像 点击关注医工学人
本篇文章来源于微信公众号: 医工学人