星标“医工学人”,第一时间获取医工交叉领域新闻动态~

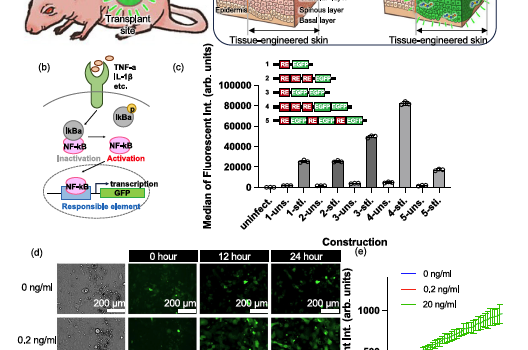
传统的生物标志物检测通常依赖于血液采样(有创且间断)或可穿戴设备(仅限汗液或间质液)。然而,生物体内的细胞本身就是极其灵敏和特异的“传感器”。近期,来自东京大学和理化学研究所(RIKEN)的研究团队在 Nature Communications 上发表了题为 “Living sensor display implanted on skin for long-term biomarker monitoring” 的研究论文。该研究提出了一种全新的概念——“活体传感器显示器”(Living Sensor Display)。通过将基因编辑后的角质形成细胞干细胞(KSCs)构建成组织工程皮肤并移植到宿主身上,这块皮肤不仅能长期存活,还能在检测到特定炎症因子(如TNF-α)时发出荧光,直接在体表“显示”体内的病理变化。
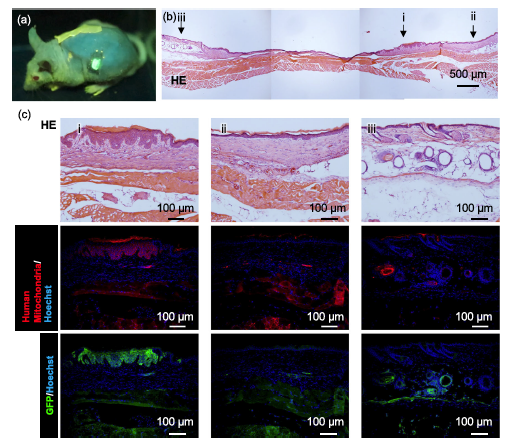
这项研究将合成生物学与组织工程相结合,创造了一种能够自我更新、长期维持且无需电池的生物监测系统。 研究团队利用了细胞内天然的信号通路。他们对人角质形成细胞(NHEK)进行了基因改造,插入了通过NF-κB信号通路调控的绿色荧光蛋白(EGFP)基因。 工作原理:当细胞膜表面的受体捕捉到炎症因子(如TNF-α)时,NF-κB信号通路被激活,进而启动EGFP的表达。 灵敏度与特异性:这种活体传感器利用了细胞膜蛋白的高亲和力,能够特异性地识别目标分子,并通过细胞内的转录翻译过程放大信号,实现了高灵敏度的检测。 图1:“活体传感器显示器”的概念与NF-κB信号通路响应机制 为了实现长期监测,研究人员利用这些改造后的细胞构建了组织工程皮肤,并将其移植到免疫缺陷小鼠背部。 长期存活:移植的皮肤成功通过了血管化过程,并实现了长达 200天以上 的稳定植入,且位置和大小保持恒定。 结构成熟:令人惊讶的是,移植后的组织工程皮肤在小鼠身上发育出了类似人类皮肤的真皮乳头结构(Papillary Structure),这是小鼠皮肤本身不具备的特征。这表明植入的干细胞在体内建立了自己的微环境(Niche),能够持续自我更新和分化,维持传感器的功能。 图2:移植后组织工程皮肤的长期存活与类人结构成熟 在活体实验中,这块“显示器”展示了卓越的监测能力。 实时响应:当向小鼠注射TNF-α或诱导炎症的脂多糖(LPS)后,移植部位的皮肤在24小时内显著发出绿色荧光,且荧光强度与炎症程度相关。 可逆与重复:炎症消退后,荧光逐渐消失;当再次给予刺激时,皮肤能再次发光。这种可逆性证明了它作为长期监测工具的潜力,能够捕捉慢性的或反复发作的炎症过程。 图3:移植皮肤对体内TNF-α刺激的反复荧光响应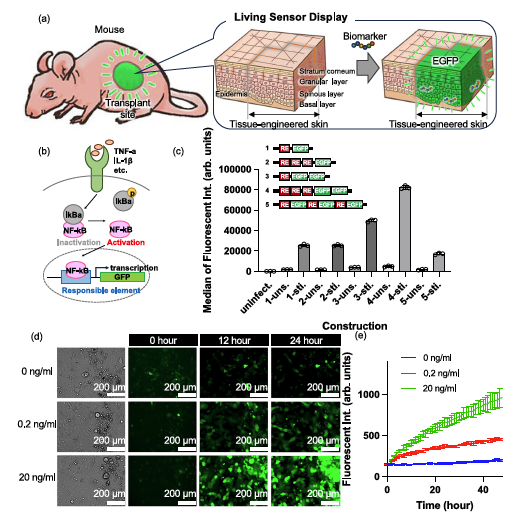
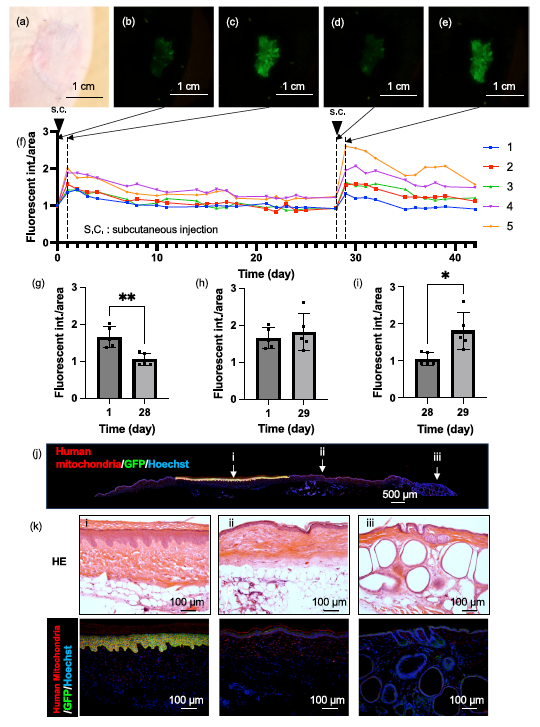
尽管“活体传感器显示器”展示了迷人的前景,但要真正应用于人类临床,还面临巨大的生物学和伦理挑战: 免疫排斥与安全性 目前的实验是在免疫缺陷小鼠(SCID)上进行的。在免疫健全的人体中,植入异体细胞或表达外源性蛋白(如EGFP)极易引发免疫排斥。未来可能需要使用患者自身的诱导多能干细胞(iPSC)来构建自体皮肤,并寻找低免疫原性的报告基因。 基因改造的伦理与监管 将基因修饰的细胞植入人体(特别是具有自我复制能力的干细胞),涉及复杂的伦理和监管问题。如何防止细胞逃逸、突变或通过生殖系传播,是必须解决的安全隐患。 检测的滞后性 荧光蛋白的表达需要经过转录和翻译过程,这导致从刺激到发光有数小时的延迟(实验中约为24小时达到峰值)。对于需要秒级响应的急性病症,这种机制可能不够及时。
东京大学团队开发的“活体传感器显示器”代表了生物监测领域的一个范式转变——从“佩戴机器”转向“植入生命”。 这种技术利用生命体自身的精密机制来感知环境,无需外部电源,且理论上可以伴随宿主终身工作。它不仅为糖尿病、自身免疫性疾病等慢性病的长期监测提供了新思路,也为兽医学中无法用语言表达痛苦的动物健康管理提供了极具潜力的工具。随着合成生物学和免疫学的进步,未来的皮肤可能不仅仅是屏障,更是我们读取体内健康的直接窗口。
END 撰文 | 张越青 排版 | 周宇茜 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊, 参与线上线下交流活动
推荐阅读
Nature Medicine | 仅凭一晚睡眠,预测130种疾病!斯坦福大学“睡眠AI”突破,是否颠覆了疾病预防体系?
Nature Machine Intelligence | 清华大学团队开发基于统一扩散Transformer框架的多模态心血管信号生成模型

点击关注医工学人
本篇文章来源于微信公众号: 医工学人