星标“医工学人”,第一时间获取医工交叉领域新闻动态~

近日,European heart journal发表了一篇探究心肌梗死后患者发生心力衰竭和再发心肌梗死的风险和预后的研究(European heart journal,2025, 22;46(16):1540-1550. doi:10.1093/eurheartj/ehae885, IF(2023):38.100; SCIE; Q1)
该研究分析了急性心肌梗死后患者发生心力衰竭和再发心肌梗死的风险。研究发现,在急性心肌梗死患者中,心力衰竭的发生率高于再发心肌梗死,即使在射血分数正常且出院时无心力衰竭的患者中也是如此。患有心力衰竭的患者死亡率和再住院率更高。这表明,即使在急性心肌梗死后心脏功能得到保留,仍有发生心力衰竭的较高风险,需要更好地了解其机制并开发针对心肌功能保护的新疗法。
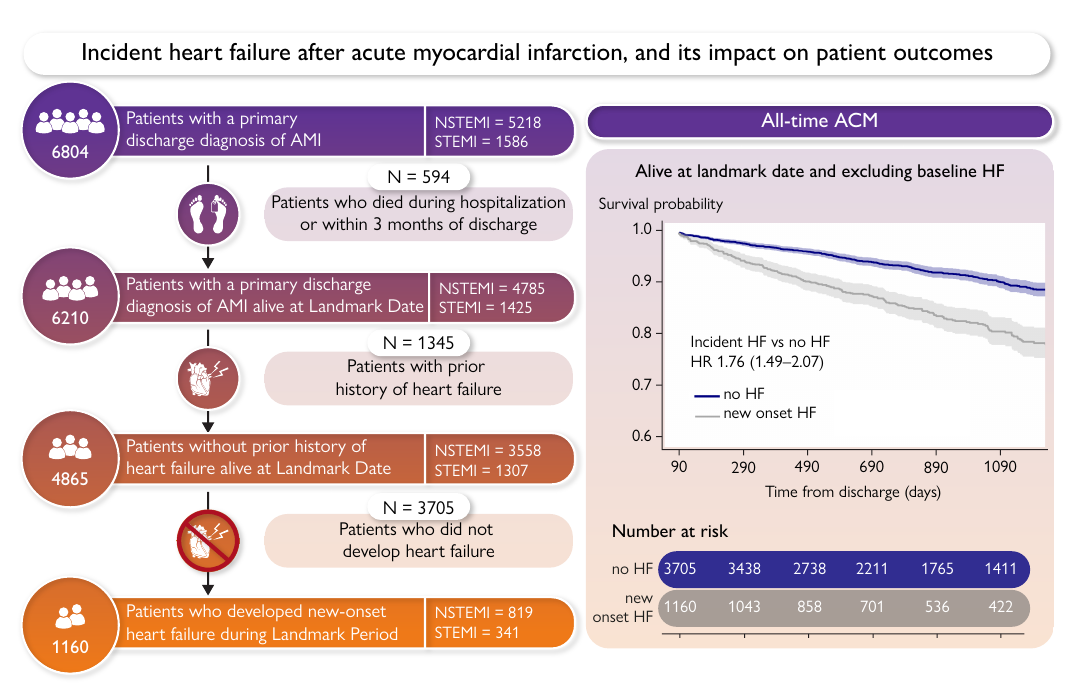
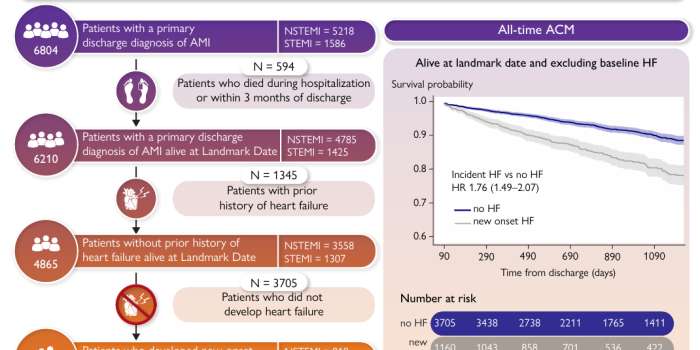
图1 急性心肌梗死后心力衰竭事件及其对患者预后的影响
01 研究背景 心梗后心力衰竭(Heart failure, HF)风险高,与死亡率、再住院率密切相关 降低心梗后复发缺血事件风险是主要治疗目标,现阶段研究已取得进展 新发HF是心梗的另一种不良后果,既往研究估计20%-25%的患者在心梗住院期间或出院后会出现HF 该研究利用医疗系统数据评估心梗后HF和复发心肌梗死(MI)的风险和结果,期望达到指导临床和研究重点的目的
02 研究核心与创新亮点 心梗后新发HF风险高: 即使在出院时EF正常且无HF病史的患者中,新发HF的风险也很大(11.8%),甚至高于复发MI的风险(3.5%) 新发HF预后差: 新发HF患者的死亡风险比无HF病史的患者高(HR 1.76),且不受EF类别的影响,说明心梗后HF的风险持续存在,需要新的治疗策略 强调正常EF患者的新发HF风险: 本研究突出了即使EF正常,心梗后新发HF的风险仍然很高,提示需要关注冠状动脉微血管功能障碍等潜在机制 呼吁开发新的治疗策略: 鉴于心梗后HF风险的持续存在,本研究呼吁开发新的HF风险降低策略,以更好地保护心肌功能并改善患者预后
图2 ST段抬高型和非ST段抬高型心肌梗死后的预后 图3 与心肌梗死后心力衰竭相关的死亡风险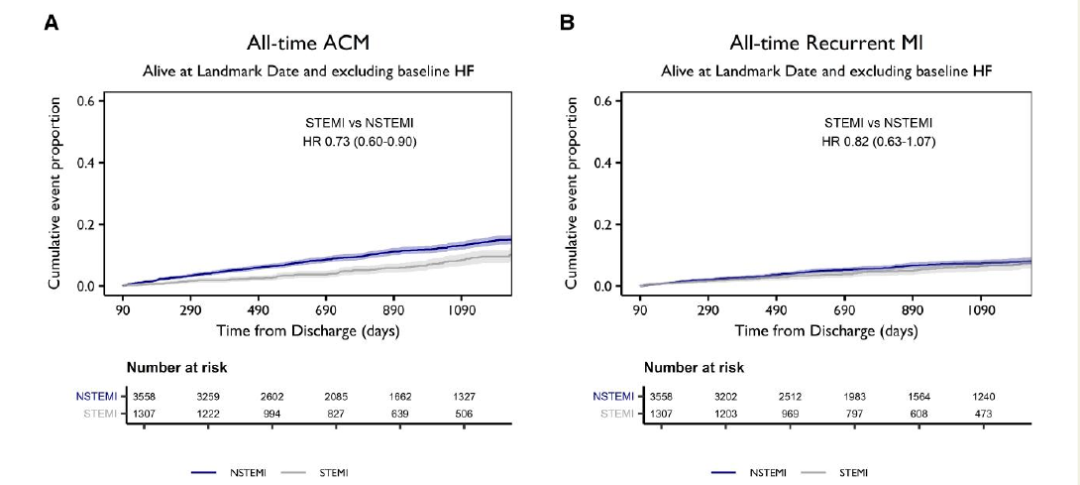
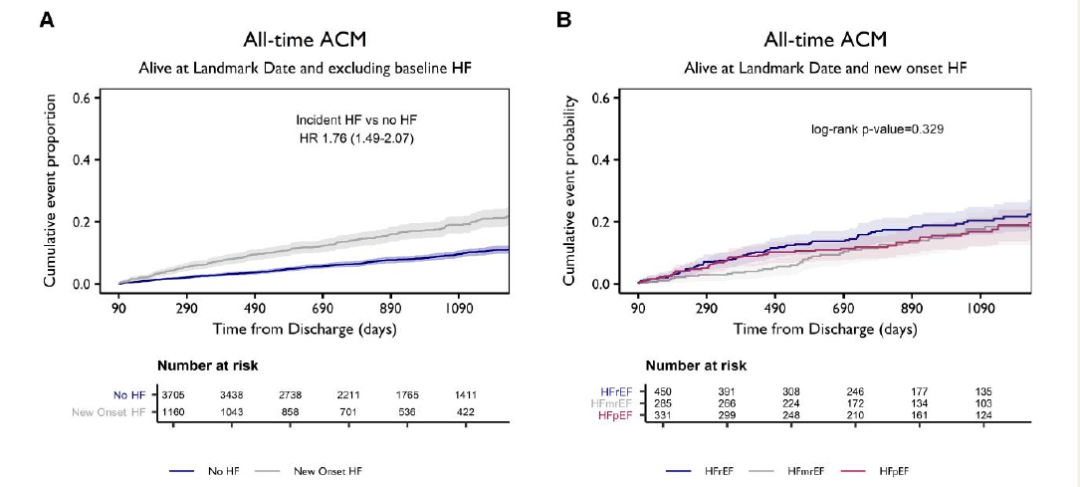
03 Q&A Question 1:研究提到,即使在没有既往心衰病史、入院时没有出现心衰并且出院时射血分数正常(≥50%)的患者中,在出院后 12 个月内发生心衰的比例仍然很高(11.8%)。这是为什么?除了冠脉微血管功能障碍外,还有哪些潜在机制可能导致这种情况? Answer:研究指出,心梗后心衰的发生机制可能更加复杂,除了冠状动脉微血管功能障碍外,还可能涉及以下潜在机制: 1. 慢性炎症和免疫反应:心梗后,心脏组织会受到损伤,引发炎症和免疫反应。这些反应可能导致心肌细胞死亡、纤维化、心肌重构,最终导致心功能下降和心衰。炎症和免疫反应也可能损伤冠状动脉微血管,导致微血管功能障碍。 2. 神经内分泌系统激活:心梗后,交感神经系统和肾素-血管紧张素-醛固酮系统(RAAS)会被激活。这些系统的激活会导致血管收缩、水钠潴留、心肌肥厚和纤维化,最终导致心功能下降和心衰。神经内分泌系统的激活也可能损伤冠状动脉微血管,导致微血管功能障碍。 3. 心肌细胞凋亡和坏死:心梗会导致心肌细胞死亡,包括凋亡和坏死。这些细胞死亡会导致心肌组织缺失、纤维化和重构,最终导致心功能下降和心衰。心肌细胞死亡也可能导致炎症和免疫反应的激活,进一步加重心肌损伤。 4. 心肌能量代谢障碍:心梗后,心肌能量代谢可能会发生障碍,导致心肌细胞功能障碍和死亡。心肌能量代谢障碍可能是由线粒体功能障碍、钙离子超载等因素引起的。心肌能量代谢障碍也可能导致炎症和免疫反应的激活,进一步加重心肌损伤。 5. 心脏瓣膜功能障碍:心梗后,心脏瓣膜功能可能会受到影响,导致心脏负荷增加和心功能下降。心脏瓣膜功能障碍可能是由心肌梗死、心肌重构等因素引起的。
Question 2:研究指出,与没有发生心衰的患者相比,发生心衰的患者死亡风险显著更高。然而,不同射血分数组之间的死亡率风险没有显著差异。这是否意味着射血分数在预测心衰患者的预后方面不再重要? Answer:射血分数(EF)仍然是预测心衰患者预后的重要指标,即使在不同射血分数组之间死亡率风险没有显著差异。研究中EF组别死亡率风险无差异的原因: 样本量限制: EF不同组别的患者数量可能相对较少,导致统计功效不足,无法检测到组间差异。 随访时间较短: 本研究随访时间仅为1年,可能不足以观察到EF对长期预后的影响。 新发心衰的普遍性: 本研究中新发心衰的患者比例较高,这可能导致EF在预测预后方面的作用被削弱。 那么,EF在预测心衰患者预后方面的作用: HFrEF: 射血分数降低的心衰(HFrEF)患者的死亡风险显著高于射血分数保留的心衰(HFpEF)患者。 HFpEF: 射血分数保留的心衰(HFpEF)患者的死亡风险虽然低于HFrEF患者,但仍高于正常人群。 HFmrEF: 射血分数轻度降低的心衰(HFmrEF)患者的死亡风险介于HFrEF和HFpEF之间。 EF与其他预后指标的关系: 年龄: 年龄越大,死亡风险越高。 性别: 女性患者死亡风险高于男性患者。 合并症: 合并症越多,死亡风险越高,例如糖尿病、慢性肾脏病等。
Question 3:研究强调了在 MI 后更好地理解心衰发展机制和开发新的治疗方法以降低 HF 风险的必要性。目前有哪些正在进行的研究或药物开发,旨在解决这一问题? Answer: 靶向冠状动脉微血管功能障碍: 血管生成药物: 促进新的血管生成,改善心肌血流灌注。 抗炎药物: 抑制炎症反应,减少心肌损伤。 抗氧化剂: 清除自由基,保护心肌细胞。 靶向神经内分泌系统: 肾素-血管紧张素-醛固酮系统(RAAS)抑制剂: 抑制RAAS系统的活性,降低血压,减少水钠潴留,改善心功能。 β受体阻滞剂: 减慢心率,降低心肌耗氧量,改善心功能。 血管紧张素受体-脑啡肽酶抑制剂(ARNI): 同时抑制RAAS系统和脑啡肽酶,扩张血管,降低血压,改善心功能。 靶向心肌细胞凋亡和坏死: 抗凋亡药物: 抑制心肌细胞凋亡,减少心肌损伤。 抗坏死药物: 抑制心肌细胞坏死,减少心肌损伤。 靶向心肌能量代谢障碍: 线粒体保护剂: 保护线粒体功能,改善心肌能量代谢。 钙离子通道阻滞剂: 降低钙离子内流,减少心肌耗氧量,改善心肌能量代谢。 靶向心脏瓣膜功能障碍: 经导管主动脉瓣置换术(TAVR): 用于治疗主动脉瓣狭窄,改善心脏负荷和心功能。 基因治疗和细胞治疗: 基因治疗: 通过基因修饰,改善心肌细胞功能和心脏重构。 细胞治疗: 通过移植干细胞,促进心肌细胞再生和修复。 数字健康技术: 远程监测: 通过可穿戴设备,实时监测患者的生理参数,及时发现病情变化。 移动医疗应用程序: 提供个性化的健康管理方案,帮助患者控制病情。
04 结论 1. HF是MI后最关键的并发症 其风险远超复发性MI,且独立于LVEF水平。 2. 射血分数正常并非“安全区” 即使LVEF≥50%,MI后HF风险仍不容忽视。 3. 临床启示 需重新定义MI后风险管理优先级,将HF预防置于与复发性MI同等甚至更高地位。
▼参考资料 Javed Butler, Kendall Hammonds, Khawaja M Talha, Ayman Alhamdow, Monica M Bennett, J Vee Anne Bomar, Jason A Ettlinger, Monica Martinez Traba, Elisa L Priest, Niklas Schmedt, Cecilia Zeballos, Courtney N Shaver, Aasim Afzal, Robert J Widmer, Robert L Gottlieb, Michael J Mack, Milton Packer; Incident heart failure and recurrent coronary events following acute myocardial infarction. European heart journal 2025 Apr 22;46(16):1540-1550 doi:10.1093/eurheartj/ehae885
END 撰文 | 孙峥 排版 | 王可豪 审核 | 医工学人理事会 扫码加入医工学人,进入综合及细分领域群聊,参与线上线下交流活动
推荐阅读
医工简报 | 中国加大脑芯片研发投入,助瘫痪者更好控制身体;用于中国分层医疗保健系统中公平诊断青光眼的三层 AI 解决方案
点击关注医工学人 最新直播

本篇文章来源于微信公众号: 医工学人